Stromectol (Ivermectin)

Dosierungen
Stromectol 3 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 10 | €4,25 | €42,53 | |
| 20 | €3,40 | €68,05 | |
| 30 | €3,12 | €93,57 | |
| 60 | €2,84 | €170,12 | |
| 90 | €2,65 | €238,17 | |
| 120 | €2,48 | €297,71 | |
| 180 | €2,36 | €425,30 | |
| 270 | €2,24 | €603,93 | |
| 360 | €2,01 | €723,01 |
Stromectol 6 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 10 | €5,10 | €51,04 | |
| 20 | €4,25 | €85,06 | |
| 30 | €3,69 | €110,58 | |
| 60 | €3,40 | €204,14 | |
| 90 | €3,21 | €289,20 | |
| 120 | €2,98 | €357,25 | |
| 180 | €2,84 | €510,36 | |
| 270 | €2,65 | €714,50 | |
| 360 | €2,24 | €808,07 |
Stromectol 12 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 10 | €5,95 | €59,54 | |
| 20 | €5,10 | €102,07 | |
| 30 | €4,82 | €144,60 | |
| 60 | €4,54 | €272,19 | |
| 90 | €4,44 | €399,78 | |
| 120 | €4,39 | €527,37 | |
| 180 | €4,16 | €748,53 | |
| 270 | €2,99 | €808,07 | |
| 360 | €2,36 | €850,60 |
Zahlung & Versand
Ihre Bestellung wird sorgfältig verpackt und innerhalb von 24 Stunden versendet. So sieht ein typisches Paket aus.
Die Sendung hat die Größe eines normalen privaten Briefes (24x11x0,7 cm), ohne Hinweis auf den Inhalt.



| Versandmethode | Voraussichtliche Lieferung |
|---|---|
| Express Kostenlos für Bestellungen über €300,00 | Voraussichtliche Lieferung nach Deutschland: 4-7 Tage |
| Standard Kostenlos für Bestellungen über €200,00 | Voraussichtliche Lieferung nach Deutschland: 14-21 Tage |











Rabattcoupons
- Neujahrstag - 1. Januar 2026 9% NEUJAHR9
- Heilige Drei Könige - 6. Januar 2026 5% DREIKOENIGE5
- Tag der Arbeit - 1. Mai 2026 6% ARBEIT6
- Tag der Deutschen Einheit - 3. Oktober 2026 8% EINHEIT8
- Allerheiligen - 1. November 2026 6% ALLERHEILIGEN6
- Heiligabend - 24. Dezember 2026 9% HEILIGABEND9
- Weihnachten - 25. Dezember 2026 10% WEIHNACHTEN10
- Zweiter Weihnachtstag - 26. Dezember 2026 9% ZWEITER9
- Silvester - 31. Dezember 2026 8% SILVESTER8
Markennamen
| Land | Markennamen |
|---|---|
 Argentinien Argentinien | Dermoper IV Dermopero Detebencil Ivertal Securo |
 Brasilien Brasilien | Ivermec Leverctin Revectina Vermectil |
 Frankreich Frankreich | Mectizan |
 Kanada Kanada | Mectizan |
 Mexiko Mexiko | Ivexterm |
 Vereinigte Staaten Vereinigte Staaten | Mectizan |
| Hersteller | Markennamen |
|---|---|
| John Lee | Iverjohn Ivermectol |
| Ochoa Laboratories Pvt. Ltd. | Iverjohn Ivermectol |
Beschreibung
Ivermectin, ein Dihydroavermectin B1, ist ein wirksames Mikrofilarizid zur Behandlung von Strongyloides, Krätze und allen Formen der Filariose außer Infektionen mit Dipalonema (Mansonella) perstans. In Deutschland kommt es vor allem in der Dermatologie und Reisemedizin zum Einsatz, insbesondere bei der Abklärung von Krätze oder parasitären Infektionen.
In den letzten Jahren hat Ivermectin bei der Behandlung der Onchozerkose sehr gute Ergebnisse gezeigt, sowohl in kontrollierten Studien als auch unter Alltagsbedingungen, einschließlich des von der Weltgesundheitsorganisation (WHO) unterstützten Behandlungsprogramms. Diese Erfahrungen haben ein umfassendes Bild der Nebenwirkungen geliefert. Die wirksame Dosierung beträgt 50-200 Mikrogramm/kg. Nach einer einmaligen oralen Dosis bleiben die Hautmikrofilarien bis zu neun Monate auf niedrigem Niveau.
Ivermectin: Beobachtungsstudien
Unter den veröffentlichten Studien haben einige gezielt versucht, das Muster der Nebenwirkungen genauer zu beschreiben. In einer solchen Studie wurde das Arzneimittel bei einigen Patienten zwar als Einzeldosis mit Diethylcarbamazin kombiniert, das Nebenwirkungsprofil wurde jedoch als ähnlich wie unter Ivermectin allein beschrieben. Inzwischen gibt es einige Situationen, in denen schon eine einzelne niedrige Dosis Ivermectin eine lang anhaltende Wirkung erzielen kann. Bei Loiasis führte zum Beispiel eine Dosis von 150 Mikrogramm/kg zu einer sehr starken Verringerung der Mikrofilarienzahl, die noch bis zu einem Jahr später anhielt, und schien den Befall bei mehr als der Hälfte der Anwender vollständig zu beseitigen. Wenn weitere Untersuchungen diesen Ansatz bestätigen, könnte das Problem der Nebenwirkungen geringer werden, da sich die wenigen Reaktionen bei diesen Dosierungen auf Haut und Gelenke beschränkten, auch wenn vereinzelt Calabar-ähnliche Schwellungen beobachtet wurden.
Brugia malayi
In einer offenen Studie aus Indien wurden 21 asymptomatische Mikrofilarienträger (mit Werten von 109-6934/ml Blut) mit einer einmaligen oralen Dosis Ivermectin 400 Mikrogramm/kg und einer einmaligen oralen Dosis Diethylcarbamazin 6 mg/kg zur Behandlung einer Brugia malayi-Infektion behandelt. Zwölf Stunden nach der Behandlung sanken die Mikrofilarienzahlen bei allen Patienten um 96-100 %, und 12 Patienten waren afilarämisch. Alle hatten Nebenwirkungen, die bis zu 48 Stunden nach der Behandlung anhielten: Fieber, Myalgie, Kopfschmerzen, Lethargie, Schüttelfrost, Schwitzen, Anorexie, Halsschmerzen und Rachenstauung, Arthralgie, Schwindel, Übelkeit und Erbrechen, Bauchschmerzen und Husten. Posturale Hypotonie, die einen Tag anhielt, wurde bei zwei Personen beobachtet. Vorübergehend erweiterte und schmerzhaft entzündete Lymphgefäße, die als Stränge sichtbar waren, wurden ebenfalls bei zwei Personen festgestellt. Die meisten Nebenwirkungen waren mild und klangen von selbst ab.
Loa loa
Die Anwendung von Ivermectin und die damit verbundenen Nebenwirkungen bei Patienten mit Loa loa wurden untersucht. Dabei zeigte sich, dass Ivermectin in einer Einzeldosis von 150-300 Mikrogramm/kg wirksam ist und die Mikrofilarienzahlen um über 90 % senkt, wobei die Zahl nach 1 Jahr weiterhin auf 25 % des Ausgangswerts unterdrückt war. Eine noch länger anhaltende Wirkung kann durch häufigere Dosierung erreicht werden. Es gibt außerdem Hinweise darauf, dass Ivermectin in höheren Dosen (400 Mikrogramm/kg zweimal jährlich) auch adulte Loa loa beeinflussen kann. Die Verträglichkeit von Ivermectin ist im Allgemeinen sehr gut, aber schwere Nebenwirkungen, insbesondere Enzephalopathie, können auftreten, vor allem bei stärker infizierten Personen.
Onchozerkose
Untersucht wurden die Auswirkungen von 5 Jahren jährlicher gemeinschaftlicher Behandlung mit Ivermectin auf die Prävalenz der Onchozerkose und die dadurch bedingte Krankheitslast im Dorf Gami (Zentralafrikanische Republik). Pruritus, onchozerkale Knoten und Sehstörungen wurden durch die jährliche Behandlung mit Ivermectin deutlich verringert.
In einer Studie zur Wirkung von Ivermectin auf adulte Onchocerca-Würmer wurden folgende Behandlungsschemata verglichen:
- 150 Mikrogramm/kg jährlich (Referenzgruppe);
- 400 Mikrogramm/kg, dann 800 Mikrogramm/kg jährlich;
- 150 Mikrogramm/kg alle 3 Monate;
- 400 Mikrogramm/kg, dann 800 Mikrogramm/kg alle 3 Monate.
Nach 3 Behandlungsjahren starben bei der 3-monatlichen Behandlung mehr weibliche Würmer als in der Referenzgruppe; außerdem waren die weiblichen Würmer weniger fruchtbar. Zwischen den beiden Gruppen mit jährlicher Behandlung gab es keinen Unterschied.
Es gab keine schweren unerwünschten Ereignisse, selbst bei hohen Dosen. Subjektive Beschwerden wie Sehstörungen, verschwommenes Sehen, Augenschmerzen oder Dyschromatopsie traten bei 800 Mikrogramm/kg jedoch häufiger auf als bei 150 Mikrogramm/kg; die Effekte dauerten weniger als eine Woche. Eine ausführliche augenärztliche Untersuchung zeigte keine Unterschiede zwischen den Patienten der Referenzgruppe und denen der drei anderen Gruppen.
Sarcoptes scabiei
In einer unkontrollierten offenen Studie wurden 101 Patienten mit Krätze mit einer einmaligen oralen Dosis Ivermectin 200 Mikrogramm/kg behandelt und dann an Tag 3 sowie nach 2 und 4 Wochen nachuntersucht. Zwei Wochen nach Behandlungsbeginn waren 89 Patienten vollständig krätzefrei, weitere drei hatten nur noch leichte Hautveränderungen und Juckreiz bei negativen Hautgeschabseln. Die übrigen neun Patienten hatten anhaltenden Juckreiz und neue Läsionen und wurden mit einer zweiten Dosis behandelt; nach 4 Wochen waren in allen Fällen die Beschwerden vollständig abgeheilt.
Zwölf Patienten berichteten über leichte Nebenwirkungen wie Müdigkeit, Arthralgie und Knochenschmerzen, Dyspnoe, Kopfschmerzen, Übelkeit und verschwommenes Sehen. Die Nebenwirkungen traten meist beim ersten Nachkontrolltermin auf und waren gut tolerierbar. Ivermectin scheint eine gut wirksame Behandlung der Krätze in einer Dosis von 200 Mikrogramm/kg zu sein, auch wenn bei einigen Patienten eine zweite Dosis für die vollständige Abheilung nötig ist.
Ein 11-jähriges Mädchen entwickelte eine schwere verkrustete norwegische Krätze. Gamma-Benzolhexachlorid-Lotion und topische Keratolytika zeigten keine nennenswerte Wirkung. Sie erhielt eine einmalige orale Dosis von Ivermectin 6 mg mit ausgeprägtem Behandlungserfolg. Der Juckreiz ließ nach 4 Stunden nach, und die Läsionen begannen sich 2 Tage später zu bessern. Nach 3 Wochen wurde eine zweite Dosis von 6 mg verabreicht, als keine Hautläsionen mehr vorhanden waren. Die einzige Nebenwirkung war nach der ersten Dosis ein Hautödem, das nach der zweiten Dosis nicht erneut auftrat. Dies deutet darauf hin, dass die Reaktion eher mit der Schwere der Infektion als mit dem Arzneimittel selbst zusammenhing.
Ausbrüche von Krätze bei älteren Menschen erfordern ein spezielles Vorgehen zur Krankheitskontrolle. Weil wiederholte, nicht abgestimmte Behandlungsmaßnahmen mit herkömmlichen äußerlich anzuwendenden Antikrätzemitteln häufig scheitern, sind gezielte Eindämmungsprogramme notwendig.
Das Management von Krätzeausbrüchen mit Allethrin, Permethrin und Ivermectin wurde untersucht. Gesunde befallene Personen wurden einmalig gleichzeitig mit einem äußerlich anzuwendenden Skabizid wie Allethrin oder Permethrin behandelt; dies war in 99 % der Fälle wirksam. Personen mit verkrusteter Krätze wurden stationär aufgenommen und systemisch mit Ivermectin oder Ivermectin plus Permethrin behandelt; sieben Patienten erhielten Ivermectin zweimal im Abstand von 8 Tagen, und einer erhielt Permethrin dreimal. Leider wurden keine Einzelheiten zu Nebenwirkungen angegeben.
Strongyloidiasis
Die Wirksamkeit und die Nebenwirkungen von Ivermectin 200 Mikrogramm/kg, nach 2 Wochen wiederholt, wurden bei 50 Patienten mit chronischer Strongyloidiasis im Alter von 30-79 Jahren untersucht. Die Eradikationsrate betrug 96 % 2 Wochen nach der ersten Dosis und 98 % nach der zweiten Dosis. Es gab keine Rückfälle bei einer Nachbeobachtungszeit von 4 Monaten. Ein Patient hatte 3 Stunden nach der ersten Dosis und erneut nach der zweiten Dosis Übelkeit und Erbrechen, die jedoch vorübergehend waren und keine Behandlung erforderten. Bei vier Patienten wurden leichte Laborveränderungen festgestellt (leichte Erhöhungen der Leberwerte bei zwei, mikroskopische Hämaturie bei einem und milde Leukopenie sowie Lymphozytose bei einem weiteren). 12 der 50 Patienten waren positiv für das humane T-lymphotrope Virus Typ 1.
Wuchereria bancrofti
Eine Frühphase der Elephantiasis aufgrund bancroftischer Filariose bei einem 27-jährigen Reisenden wurde mit einer oralen Einzeldosis-Kombination aus Ivermectin 24 mg plus Albendazol 400 mg behandelt, gefolgt von Albendazol 800 mg für 21 Tage. Um eine schwere Mazzotti-ähnliche Reaktion zu vermeiden, erhielt er 3 Tage lang orale Glukokortikoide und Antihistaminika. In den Tagen nach der Erstbehandlung entwickelte er vorübergehend einen Ausschlag, Pruritus und eine leichte Hypotonie, ansonsten blieb er wohlauf, und die Schwellung bildete sich zurück. Innerhalb eines Monats war er symptomfrei. Bei der letzten Nachuntersuchung 3 Jahre nach der Behandlung gab es keine klinischen oder laborchemischen Hinweise auf einen Rückfall. Die Autoren meinten, diese Behandlungsform sollte wegen der geringen Nebenwirkungen und der scheinbaren therapeutischen Wirksamkeit in größerem Maßstab untersucht werden.
Untersucht wurden außerdem die Wirksamkeit einer jährlichen Massenchemotherapie mit einer Kombination aus Diethylcarbamazin und Ivermectin bei bancroftischer Filariose im ländlichen Südindien sowie die ergänzende Rolle der Bekämpfung der Vektormücke Culex quinquefasciatus. Neun Dörfer wurden ausgewählt, die topografisch und ökologisch ähnlich, aber relativ isoliert voneinander waren, und in drei vergleichbare Gruppen mit je drei Dörfern eingeteilt.
Gruppe A erhielt Chemotherapie mit Diethylcarbamazin etwa 6 mg/kg und Ivermectin 400 Mikrogramm/kg. Gruppe B erhielt Chemotherapie und Vektorkontrolle. Die wichtigsten Brutstätten der Vektoren waren Versickerungsgruben, die mit expandierten Polystyrolperlen behandelt wurden. Kleinere Brutstätten wie häusliche oder Bewässerungsbrunnen wurden mit larvenfressenden Tilapia-Fischen oder einem kommerziellen Insektizid auf Bacillus sphaericus-Basis behandelt. Gruppe C erhielt keine Intervention.
Nach der ersten Behandlungsrunde führte die Kombinationstherapie allein zu einem 60%igen Rückgang des jährlichen filarialen Übertragungspotenzials, während die kombinierte Strategie das Übertragungspotenzial um 96 % reduzierte. Nach zwei Behandlungsrunden war die Reduktion des Übertragungspotenzials bei beiden Strategien ähnlich (etwa 91-96 %), während die Prävalenz der Mikrofilarämie um 88-92 % zurückging.
Nach der Kombinationstherapie traten bei 20 % der erstmals behandelten Patienten unerwünschte Ereignisse auf. Die Patienten mit Nebenwirkungen hatten erhöhte Mikrofilarienzahlen. Die häufigsten Nebenwirkungen waren Kopfschmerzen (72 % der Nebenwirkungen), Schwindel (67 %), Fieber und Schwäche. Bei der zweiten Behandlung mit der Kombinationstherapie war die Häufigkeit von Nebenwirkungen mit 5,5 % relativ gering.
Die Nebenwirkungen waren in der zweiten Runde auch weniger schwerwiegend als in der ersten. Als die antifilarielle Behandlung im dritten und letzten Studienjahr eingestellt wurde, setzte die Übertragung ohne Vektorkontrolle wieder ein, während in Dörfern mit Vektorkontrolle keine infektiösen weiblichen Mücken nachgewiesen wurden. Die Vektorkontrolle kann daher trotz fehlender kurzfristiger Kosteneffektivität eine wichtige ergänzende Rolle in einem integrierten Programm spielen, indem sie die Wiederaufnahme der Übertragung nach Abschluss der Chemotherapie verhindert.
Ivermectin: Vergleichsstudien
Sarcoptes scabiei
In einer randomisierten Studie wurde eine einmalige orale Dosis Ivermectin (200 Mikrogramm/kg) mit 1 % Gamma-Benzolhexachlorid-Lotion zum einmaligen nächtlichen Auftragen bei 200 Patienten mit Krätze verglichen. Die Patienten wurden nach 48 Stunden, 2 Wochen und 4 Wochen beurteilt. Nach 4 Wochen zeigten 83 % der mit Ivermectin Behandelten eine deutliche Verbesserung, verglichen mit 44 % der mit Gamma-Benzolhexachlorid Behandelten. Für Gamma-Benzolhexachlorid wurden keine unerwünschten Ereignisse berichtet. Kopfschmerzen wurden unter Ivermectin nur einmal beobachtet.
Bei 80 Kindern im Alter von 6 Monaten bis 14 Jahren wurde in einer randomisierten, kontrollierten Studie zur Behandlung der pädiatrischen Krätze eine einmalige Dosis Ivermectin 200 Mikrogramm/kg mit äußerlich angewendetem Benzylbenzoat verglichen. Ivermectin heilte 24 von 43 Patienten, während Benzylbenzoat 3 Wochen nach der Behandlung bei 19 von 37 Patienten wirksam war. Unter keiner der beiden Behandlungen traten schwere Nebenwirkungen auf, auch wenn Benzylbenzoat häufiger lokale Hautreaktionen verursachte. Diese Ergebnisse stimmen mit einer weiteren Studie überein, in der 18 Kinder im Alter von 14 Monaten bis 17 Jahren mit Krätze oder kutaner Larva migrans einmalig mit Ivermectin 150-200 Mikrogramm/kg behandelt wurden. Eine Einzeldosis heilte 15 Patienten, und drei Patienten mit verkrusteter Krätze benötigten eine zweite Dosis. Es traten keine nennenswerten Nebenwirkungen auf.
Wuchereria bancrofti
In einer Studie, in der bei Wuchereria bancrofti-Infektion Dosen von 200 oder 400 Mikrogramm verwendet wurden, mit oder ohne Diethylcarbamazin, wurde eine überdurchschnittlich hohe Häufigkeit von Reaktionen festgestellt (und eine höhere Häufigkeit unter Ivermectin als unter Diethylcarbamazin). Das könnte möglicherweise an den ungewöhnlich hohen Erfolgsraten oder an der Schwere der ursprünglichen Infektion gelegen haben. Aus ähnlichen Gründen zeigen wiederholte Behandlungszyklen tendenziell eine abnehmende Häufigkeit von Nebenwirkungen. Üblicherweise treten bei einer Erstbehandlung allgemeine Symptome wie Fieber, Schwäche, Anorexie, Unwohlsein und Schüttelfrost bei einem erheblichen Teil der Patienten auf, während mindestens ein Drittel Muskel- und/oder Gelenkschmerzen hat. Schwindel, Dyspnoe, Durchfall und Bauchbeschwerden betreffen einige wenige Patienten. Die Schwere der Nebenwirkungen korreliert nicht mit den Serumspiegeln des Medikaments, was wiederum darauf hindeutet, dass sie hauptsächlich Folge des Zerfalls der Parasiten und nicht toxische Effekte von Ivermectin sind.
Ivermectin: Placebokontrollierte Studien
Erbrechen, Ataxie und Mydriasis sind Leitsymptome einer Ivermectin-Toxizität. Sicherheit, Verträglichkeit und Pharmakokinetik ansteigender hoher Dosen wurden in einer randomisierten, doppelblinden, placebokontrollierten Studie an 68 gesunden Probanden mit folgenden Dosierungen untersucht:
- 30 mg nüchtern
- 60 mg nüchtern
- 90 mg nüchtern
- 120 mg nüchtern; 30 mg nach einer Mahlzeit
Ivermectin wurde generell gut vertragen. Die quantitative Pupillometrie schloss eine mydriatische Wirkung von Ivermectin aus. Es wurde bei oraler Gabe in keiner Dosis eine Toxizität des Nervensystems festgestellt. Es traten keine schweren klinischen oder laborchemischen Nebenwirkungen auf. Drei von 51 nüchternen Probanden, die Ivermectin erhielten, berichteten über leichte gastrointestinale Nebenwirkungen: Stuhlunregelmäßigkeiten, Übelkeit und Erbrechen; sechs berichteten über leichte neurologische Nebenwirkungen: Kopfschmerzen, Angstzustände und Schwindel. Bei den Probanden, die 120 mg Ivermectin erhielten, gab es keine Nebenwirkungen. Die Resorption von Ivermectin war nach einer fettreichen Mahlzeit etwa 2,5-fach erhöht.
Sarcoptes scabiei
In einem randomisierten, doppelblinden Vergleich der Wirksamkeit von oralem Ivermectin und topischem Gamma-Benzolhexachlorid wurden 53 Patienten randomisiert entweder einmalig mit oralem Ivermectin 150-200 Mikrogramm/kg und einer Placebo-Lösung oder einmalig mit 1 % Gamma-Benzolhexachlorid-Lösung und Placebo-Tabletten behandelt. Patienten, die innerhalb von 15 Tagen die Kriterien für eine klinische Heilung (das Fehlen von Pruritus und klinischen Läsionen oder eine Reduktion der Zeichen und Symptome auf ein mildes Ausmaß) nicht erfüllten, wiederholten die anfängliche Behandlung.
Von den 53 Patienten schlossen 43 die Studie ab (19 mit Ivermectin behandelt und 24 mit Gamma-Benzolhexachlorid). Nach 15 Tagen galten 74 % der mit Ivermectin und 54 % der mit Gamma-Benzolhexachlorid behandelten Patienten als geheilt. Nach 29 Tagen waren beide Behandlungen mit Heilungsraten von 95 % beziehungsweise 96 % gleich wirksam. Die Nebenwirkungen waren in beiden Gruppen mild und vorübergehend. Ein mit Ivermectin behandelter Patient hatte Hypotonie, einer Bauchschmerzen, einer Erbrechen und einer klagte über Kopfschmerzen. Es gab keine Auffälligkeiten in den routinemäßigen Laboruntersuchungen.
Wuchereria bancrofti
In einer doppelblinden, placebokontrollierten Studie in Ghana erhielten 1425 Personen mit Wuchereria bancrofti-Infektion Einzeldosen von Ivermectin 150-200 Mikrogramm/kg und Albendazol 400 mg, jeweils einzeln oder in Kombination. 340 davon waren vor der Behandlung mikrofilarienpositiv. Ivermectin und Ivermectin plus Albendazol führten beide bei der Nachuntersuchung zu statistisch signifikanten Reduktionen der mittleren Mikrofilarienzahlen; die Wirkung von Ivermectin hielt länger an. Albendazol führte zu einer nicht signifikanten Reduktion. Reaktionen waren selten und überwiegend mild, schwere Reaktionen gab es nicht.
Wirkmechanismus
Der Wirkmechanismus von Ivermectin wurde untersucht. Vorläufig wird er als Agonismus an Gamma-Aminobuttersäure-(GABA)-Rezeptoren beschrieben, verbunden mit einer Hemmung von Ionenkanälen, die bestimmte Verbindungen zwischen Nervenzellen steuern. Dadurch dürfte die Funktion der Chloridkanäle in den meisten Organismen verändert werden, was zur Lähmung und zum Tod der Parasiten führt. Es wurden mehrere Wirkorte vorgeschlagen:
- eine postsynaptische Agonisten-Bindungsstelle entweder am Rezeptor oder in seiner unmittelbaren Umgebung;
- eine präsynaptische Stelle zur Aktivierung der GABA-Freisetzung;
- eine Verstärkung der GABA-Bindung an ihren Rezeptor.
Ein weiterer Wirkmechanismus umfasst die Bindung von Ivermectin an P-Glykoprotein.
Laktation
Nur eine geringe Menge Ivermectin geht in die Muttermilch über, und es wurde vorgeschlagen, stillende Mütter nicht von der Massenchemotherapie mit Ivermectin auszuschließen.
Nebenwirkungen
Als Anthelminthikum gilt Ivermectin als relativ gut verträgliches Medikament und wird im Allgemeinen besser vertragen als Diethylcarbamazin. Klinische Erfahrungen zeigen häufig eine relativ geringe Toxizität, obwohl leichte Nebenwirkungen, vermutlich durch das Absterben der Mikrofilarien, bei mindestens einem Drittel der Patienten auftreten; einige Untersuchungen legen nahe, dass eine Aktivierung der Neutrophilen bei der Entstehung dieser Reaktionen eine Rolle spielen könnte. Auch in Kombinationen wurde es gut vertragen, zum Beispiel mit Albendazol zur Abtötung adulter Würmer (was mit Ivermectin allein nicht erreicht werden kann) oder mit Diethylcarbamazin bei bancroftischer Filariose.
Zu Beginn bestand vor allem die Sorge, dass Ivermectin eine lange Halbwertszeit hat und bei manchen Personen verzögert auftretende Effekte auslösen könnte. In frühen Phasen wurde empfohlen, Patienten in Gebieten, in denen das Medikament breit eingesetzt wurde, einschließlich durch Gesundheitsfachkräfte, noch eine Zeit lang weiter zu beobachten, falls Probleme auftreten. Tatsächlich wurden jedoch keine späten Komplikationen dokumentiert.
Allgemeine Nebenwirkungen
Akute Symptome, oft grippeähnlich oder an der Haut, hängen fast ausschließlich mit der Freisetzung toxischer Stoffe und Allergene aus den abgetöteten Filarien zusammen und können bis zu zwei Drittel der Patienten betreffen; unter Bedingungen, in denen diese Art von Reaktion nicht auftritt, könnte man vermuten, dass das Medikament unwirksam ist. Dieser Wirkmechanismus erklärt auch, warum die Reaktionen früh und manchmal nur kurz auftreten, nämlich unmittelbar nach dem Tod der Mikrofilarien. Aus ähnlichen Gründen sind diese Wirkungen bei Patienten mit hoher Mikrofilarienzahl am stärksten ausgeprägt.
Auch wenn Hautreaktionen manchmal vorübergehend und offenbar tolerierbar sind, können sie bei Patienten unter längerfristiger Behandlung anhalten und unter diesen Bedingungen die Therapietreue beeinträchtigen.
Untersucht wurden außerdem die Auswirkungen von Alter, Geschlecht, Behandlungsrunde, Tageszeit und Entfernung zum Pflegepersonal auf die Meldung von Nebenwirkungen bei der Massenbehandlung mit Ivermectin in Achi im Südosten Nigerias. Es gab einen signifikanten Anstieg der Meldungen mit zunehmendem Alter, jedoch nicht in Bezug auf das Geschlecht. Nach nächtlichem Behandlungsbeginn wurden weniger Nebenwirkungen berichtet als nach Behandlungsbeginn am Tag. Entfernungen bis zu 1 km hatten keinen signifikanten Einfluss auf die Meldung unerwünschter Ereignisse. Sowohl die Compliance als auch die Meldung von Nebenwirkungen waren nach der zweiten Behandlungsrunde geringer als nach der ersten. Diese Variablen sollten bei der Standardisierung von Nebenwirkungsmeldungen berücksichtigt werden.
Ivermectin-Nebenwirkungen bei der Behandlung der Onchozerkose
Obwohl Nebenwirkungen nach Ivermectin bei Onchozerkose in der Regel weniger schwer sind als nach Diethylcarbamazin, treten sie nach der ersten Dosis dennoch bei vielen Patienten auf. Bei weiteren Behandlungen kommen diese Reaktionen seltener vor und fallen meist milder aus. Die sogenannte Mazzotti-Reaktion, die häufig nach der Behandlung von Onchocerca volvulus mit Diethylcarbamazin oder Ivermectin beobachtet wird, ist gekennzeichnet durch Fieber, Tachykardie, Hypotonie, Adenitis, Pruritus, Arthralgie, einen papulösen oder urtikariellen Ausschlag und Lymphödeme. Sie gilt als entzündliche Wirtsreaktion auf das Abtöten der Mikrofilarien und ist bei Patienten mit höherer Parasitenlast tendenziell ausgeprägter. Die Rolle von Chemotaktika wie Eotaxin, RANTES und MCP-3 bei der Rekrutierung von Eosinophilen an den Ort des Parasitenabbaus wurde bei 13 Patienten mit Onchozerkose und zwei Kontrollpersonen vor und nach Ivermectin untersucht. Bei acht Patienten traten Nebenwirkungen auf, keine davon war schwerwiegend. Beobachtet wurden Fieber (54 %), Pruritus (62 %), Ausschlag (46 %) und Lymphödeme (46 %). Eine signifikante orthostatische Hypotonie wurde nicht festgestellt. Nach Ivermectin zeigte sich eine endotheliale Expression von RANTES und Eotaxin, was darauf hindeutet, dass diese Chemotaktika eine wichtige Rolle bei der Rekrutierung von Eosinophilen in die Haut während des Abtötens oder Absterbens der Parasiten spielen.
Es wurde vermutet, dass die Freisetzung bakterieller Endosymbionten von Wolbachia an der Entstehung der Mazzotti-Reaktion beteiligt ist. Nach der Behandlung mit Ivermectin oder Diethylcarbamazin zeigte sich eine gute Korrelation zwischen Wolbachia-DNA, Serum-TNF-Alpha sowie den antibakteriellen Peptiden Calprotectin und Calgranulin. Das stützt die Annahme, dass Wolbachia-Produkte an der Entzündungsreaktion beteiligt sind.
Es wurde eine epidemiologische Untersuchung zur Endemizität der humanen Onchozerkose und zu den Auswirkungen der anschließenden Massenverteilung von Ivermectin in Dörfern der Nzerem-Ikpem-Gemeinschaft in Nigeria durchgeführt. Von 1126 untersuchten Personen waren 527 in Hautproben mikrofilarienpositiv, 329 hatten Leopardenhaut (charakterisiert durch fokale Depigmentierung), 385 hatten Knötchen und 167 litten an Acrodermatitis. Bei 362 Patienten (19 %) traten Nebenwirkungen auf: Pruritus bei 13 %, Schwellungen der Gliedmaßen bei 8,5 %, Gesichtsschwellungen bei 2 %, Schwäche bei 4,8 %, Übelkeit und Erbrechen bei 3,4 %, Kopfschmerzen bei 5,8 %, Durchfall bei 3,4 % und Rheuma bei 3,5 %. Schwere Reaktionen traten nicht auf.
Nebenwirkungen von Ivermectin bei der Behandlung der Loa-loa-Enzephalopathie
Bei der großflächigen Behandlung von Loa-loa-Infektionen mit Ivermectin scheint die Enzephalopathie, die unter Diethylcarbamazin eine gefürchtete Komplikation war, vor allem bei stark infizierten oder älteren Menschen erneut aufzutreten.
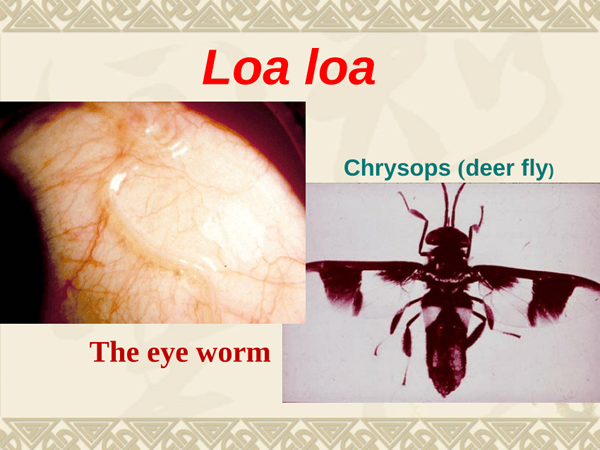
Aus diesem Grund wird der Masseneinsatz von Ivermectin in Gebieten, in denen Loa-loa-Infektionen endemisch sind, nicht mehr empfohlen. Ivermectin scheint den Übertritt von Loa-loa-Mikrofilarien in den Liquor cerebrospinalis zu begünstigen, mit einem Maximum nach 3-5 Tagen, gefolgt von einer intensiven allergischen Reaktion auf die absterbenden Mikrofilarien. Das Mectizan-Expertengremium definierte einen gesicherten Fall einer Loa-loa-Enzephalopathie im Zusammenhang mit Ivermectin durch das Erfüllen zweier Kriterien:
- Enzephalopathie mit mikroskopischem Nachweis einer Vaskulopathie im Gehirn, die mit Loa-loa-Mikrofilarien assoziiert ist;
- Beginn der Symptome einer gestörten Funktion des Nervensystems innerhalb von 5 Tagen nach der Behandlung mit Ivermectin, mit Fortschreiten bis zum Koma ohne Besserung.
Ein wahrscheinlicher Fall einer Loa-loa-Enzephalopathie wurde durch das Erfüllen von vier Kriterien definiert:
- Koma bei einem zuvor gesunden Menschen;
- Beginn von Symptomen des Nervensystems innerhalb von 5 Tagen nach der Behandlung mit Ivermectin mit Fortschreiten zum Koma;
- Eine anfängliche Mikrofilarämie von über 10.000/ml oder 1000/ml in einer Blutprobe, die innerhalb von 2 Monaten nach der Behandlung entnommen wurde;
- Nachweis von Loa-loa-Mikrofilarien im Liquor.
Klinisch treten bei diesem Zustand häufig Bewusstseinsstörungen auf, die 3-4 Tage nach der Behandlung beginnen und 2-3 Tage andauern.
Es gibt keinen Konsens über die richtige Behandlung der mit Ivermectin assoziierten Loa-loa-Enzephalopathie, und es ist unklar, ob die gleichzeitige Gabe von Glukokortikoiden hilfreich ist. Bei mehreren Patienten mit stärkeren Reaktionen wurden Konjunktivalblutungen beobachtet.
Eine systematische Untersuchung der Konjunktiven bei 1682 Patienten mit unerwünschten Reaktionen zeigte, dass diese Blutungen eng mit der Mikrofilarienzahl vor der Behandlung zusammenhingen. Dieses Zeichen kann 2 Tage nach der Behandlung auftreten und so Patienten erkennen lassen, die anfällig für eine Enzephalopathie sind und engmaschig überwacht werden sollten. Obwohl solche Fälle sehr selten sind (etwa 1 von 10.000 behandelten Patienten), stellt diese schwerwiegende Nebenwirkung die Massenbehandlung der Loa-loa-Infektion sowie die Massenbehandlung der Onchozerkose in Loa-loa-endemischen Gebieten vor Probleme. Zur Veranschaulichung wurden drei wahrscheinliche Fälle einer Loa-loa-Enzephalopathie nach Ivermectin-Behandlung der Onchozerkose beschrieben. Alle drei betrafen junge Männer, die im Rahmen einer Massenbehandlung mit 150 Mikrogramm/kg Ivermectin behandelt wurden.
- Ein 26-jähriger zuvor gesunder Mann entwickelte bis zum dritten Tag neurologische Symptome mit Unfähigkeit zu stehen oder zu essen und Nackensteifigkeit. Am vierten Tag hatte er Schluck- und Sprechstörungen. Am fünften Tag konnte er nicht sprechen und war urinkontinent. Er erhielt Dexamethason, Diazepam, Furosemid und Atropin. Am sechsten Tag fiel er ins Koma. Am neunten Tag entwickelte er hohes Fieber und erhielt Penicillin sowie Sondenernährung. Sein Zustand verschlechterte sich allmählich, und er starb am 21. Tag. Die Mikrofilarienzahl im Serum war am 13. Tag nach der Behandlung noch hoch (3600/ml), und im Liquor wurden lebende Loa-loa-Mikrofilarien (10/ml) gefunden.
- Ein 32-jähriger Mann mit Alkoholismus hatte vor der Behandlung eine sehr hohe Mikrofilarienzahl im Serum (50.000/ml). Nach Beginn der Ivermectin-Behandlung legte er sich ins Bett und sprach nicht mehr. Am dritten Tag entwickelte er Fieber, vermutlich durch Malaria bedingt, und wurde mit Chloroquin behandelt. Am vierten Tag konnte er nicht stehen und zeigte abwechselnd Unruhe und Schläfrigkeit; im Liquor wurden lebende Loa-loa-Mikrofilarien gefunden. Er wurde zunehmend verwirrt und unruhig und zeigte einen ausgeprägten Greifreflex. Später an diesem Tag entwickelte er eine spastische Hypertonie. Am fünften Tag wurde er inkontinent und sprach weiterhin nicht. In den folgenden Tagen besserte sich sein Zustand allmählich, und 4 Monate später zeigte sich keine neurologische Auffälligkeit mehr, obwohl seine Angehörigen eine Verhaltensänderung bemerkten und er deutlich ruhiger war als früher. Ein EEG am 15. Tag zeigte periodische diffuse Entladungen großer Amplitude während der Hyperventilation, am 146. Tag einen asymmetrischen Befund mit fokaler Aktivität im rechten parieto-okzipitalen Bereich, die sich bei Hyperventilation verschlechterte. Am 233. Tag war das EEG normal.
- Ein 18-jähriger zuvor gesunder Mann erhielt Ivermectin. Am zweiten Tag war er nicht arbeitsfähig und blieb zu Hause. Am dritten Tag wurde er bewusstlos im Bett aufgefunden, urin- und stuhlinkontinent. Am vierten Tag bewegte er sich nicht und zeigte keine Schmerzreaktion. In den Armen bestand Hypertonie mit ausgeprägtem Zahnradphänomen. Am fünften und sechsten Tag zeigten sich pendelnde horizontale Augenbewegungen, ansonsten besserte sich sein Zustand. Am siebten Tag konnte er mit Unterstützung sitzen und sprach einige Sätze. Er konnte langsame willkürliche Bewegungen ausführen, Muskelkraft und Sensibilität kehrten zurück, obwohl das Zahnradphänomen noch vorhanden war. In den folgenden Wochen kehrte er allmählich zum Normalzustand zurück. Nach 5 Monaten war die neurologische Untersuchung unauffällig, jedoch klagte er weiterhin über Kopfschmerzen und zeitweilige Amnesien. Die Mikrofilarienzahl im Serum vor der Behandlung war hoch (152.940/ml), und im am vierten Tag entnommenen Liquor wurden lebende Loa-loa-Mikrofilarien gefunden. Das EEG am 19. Tag zeigte eine verlangsamte, spontane, diffuse, paroxysmale, monomorphe Theta-Aktivität von 2-3 Sekunden Dauer. Das EEG am 105. Tag zeigte eine Besserung, jedoch bestanden fokale Auffälligkeiten im linken okzipitalen Bereich fort. Am 159. Tag waren alle zuvor aufgezeichneten Auffälligkeiten verschwunden.
Nebenwirkungen an Organen und Systemen
Kardiovaskulär
Im Liegen und bei Lagewechsel kann es zu Tachykardie mit orthostatischer Hypotonie kommen; in einer großen Studie traten solche Effekte bei drei von 40 Patienten auf. In einer anderen Studie wurde in 13 von 69 Fällen Hypotonie festgestellt, während diese Effekte in manchen Fallserien überhaupt nicht beobachtet wurden. Eine große Gemeinschaftsstudie in Ghana fand unter fast 15.000 behandelten Patienten nur 37 Fälle von Hypotonie. Vorübergehende EKG-Veränderungen werden manchmal beobachtet.
Respiratorisch
Bei der Behandlung der Wuchereria-bancrofti-Filariose wurde die Atemfunktion bei 23 Patienten nach Einzeldosen von bis zu 200 Mikrogramm/kg untersucht; 24 bis 30 Stunden nach der Gabe zeigte sich ein vorübergehender, aber signifikanter Abfall der Vitalkapazität, offenbar verursacht durch Bronchokonstriktion. In der oben genannten Studie trat in 2 % der Fälle ausgeprägte Dyspnoe auf. In anderen Studien entwickelten einige wenige Patienten vorübergehenden Husten, und in weiteren Untersuchungen wurden pneumonitische Herde im Röntgenbild des Thorax beobachtet.
Nervensystem
Kopfschmerzen und Schwindel sind sehr häufig und gehören sogar zu den typischen Symptomen der grippeähnlichen Reaktion auf Ivermectin.
Eine rätselhafte Reaktion wurde in einer kleinen deutschen Krankenhauspopulation älterer Patienten dokumentiert, die wegen Krätze mit einer Einzeldosis Ivermectin (150-200 Mikrogramm/kg) behandelt wurden. Innerhalb von 6 Monaten starben 15 der 47 Patienten. Alle Verstorbenen hatten vor dem Tod plötzlich Verhaltensänderungen mit Lethargie, Anorexie und Apathie entwickelt. Dieser Effekt könnte ein Artefakt mit anderer Ursache gewesen sein. Bemerkenswert ist, dass andere Gruppen, die diese Behandlung bei Krätze einsetzen, keine ähnlichen Reaktionen dokumentiert haben.
Sinnesorgane
Genaue augenärztliche Untersuchungen zeigen bei einem erheblichen Teil der Patienten eine auffällige Zunahme der Mikrofilarienzahl in der vorderen Augenkammer, und während der Behandlung kann in bereits geschädigten Netzhautarealen ein neues Entzündungsinfiltrat auftreten. Dauerhafte Folgen für die Augen wurden jedoch nicht dokumentiert. Die meisten anderen augenärztlichen Symptome, einschließlich Ödemen und lokalen Entzündungen, gehen auf die Primärinfektion zurück.
Konjunktivalblutungen wurden bei Patienten aus Loiasis-endemischen Gebieten beobachtet. Obwohl Ivermectin üblicherweise gut vertragen wird, zeigten diese Patienten nach der Einnahme von Ivermectin schwere Nebenwirkungen, darunter eine Enzephalopathie ähnlich der nach Behandlung mit Diethylcarbamazin. Rückblickend hatten alle diese Fälle eine hohe Loa-loa-Mikrofilarämie und Loa-loa-Mikrofilarien im Liquor. Die Autoren schlugen vor, dass Ivermectin den Übertritt von Loa-loa-Mikrofilarien in den Liquor ausgelöst haben könnte. In einer Folgestudie mit 1682 Patienten mit Loiasis, die mit 150 Mikrogramm/kg Ivermectin behandelt wurden, fanden sich bei 41 Patienten Konjunktivalblutungen; neun von ihnen hatten zuvor ein mikrofilarizides Medikament erhalten. Die anfängliche mittlere Mikrofilarienzahl betrug 14.900 Mikrofilarien/ml (Bereich 0-182.400) im Vergleich zu 14,5 Mikrofilarien/ml (Bereich 0-97.600) bei Patienten ohne Konjunktivalblutungen. Außerdem waren männliches Geschlecht und die Mikrofilarienzahl von Dipalonema perstans mit Konjunktivalblutungen assoziiert. Es bestand ein enger Zusammenhang zwischen Konjunktivalblutungen und Netzhautläsionen. Auf Grundlage von Beobachtungen bei drei Patienten, die alle nach Ivermectin ins Koma fielen, vermuteten die Autoren, dass Netzhautläsionen ein Spiegelbild der Vorgänge in der zerebralen Zirkulation bei Patienten mit hoher Loa-loa-Mikrofilarämie und neurologischen Problemen nach Ivermectin sein könnten.
Hämatologisch
Bei 28 sudanesischen Patienten, die wegen Onchozerkose mit einer Einzeldosis Ivermectin behandelt wurden, verlängerte sich die Prothrombinzeit, und sie nahm in den folgenden 4 Wochen noch weiter signifikant zu; andere Gerinnungsparameter zeigten keine Veränderungen. Nach einem Monat entwickelten zwei Patienten Hämatome, die sich über weitere 31 Tage vergrößerten. Beide hatten 150 Mikrogramm/kg Ivermectin erhalten. Einer erhielt eine Transfusion; bei beiden bildeten sich die Schwellungen innerhalb einer Woche zurück. Zeitweise wurde angenommen, dass die Veränderungen der Prothrombinzeit ein potenzielles Problem darstellen könnten. Neuere Studien zeigen jedoch, dass die Verlängerung des Prothrombin-Quotienten kaum über dem Placebo-Niveau liegt und dass Ivermectin nur einen milden Effekt auf den Vitamin-K-Stoffwechsel hat und die Gerinnung kaum beeinflusst. Allerdings wurde bei einigen Patienten Lymphadenitis beobachtet. In einer guatemaltekischen Untersuchung zur halbjährlichen Behandlung der Bevölkerung zur Ausrottung der Onchocerca-volvulus-Infektion wurde bei fast 20 % der erstmals behandelten Patienten eine Schwellung der oberen Gliedmaßen festgestellt.
Gastrointestinal
Im Spätstadium einer Strongyloides-Hyperinfektion kann ein Ileus entstehen, der die Aufnahme oral eingenommener Medikamente erschwert.
Ein 39-jähriger afrokaribischer Mann mit einem T-Zell-Lymphom im Stadium IVB infolge einer Infektion mit dem humanen T-lymphotropen Virus Typ 1 (HTLV-1) hatte eine invasive Strongyloides-Hyperinfektion, die wegen eines begleitenden Ileus nicht auf eine orale Behandlung mit Ivermectin plus Albendazol ansprach. Er wurde mit zwei subkutanen Dosen von jeweils 6 mg einer veterinärmedizinischen Ivermectin-Formulierung behandelt. Abgesehen von Schmerzen an der Injektionsstelle traten keine Nebenwirkungen auf.
Harnwege
Proteinurie ist ungewöhnlich, wurde aber beschrieben; sie wurde 14 Tage nach einer Einzeldosis festgestellt und verschwand im Verlauf der Nachbeobachtung.
Beobachtungen, dass Proteinurie und Hämaturie bei Patienten mit Wuchereria-bancrofti-Filariose und Loiasis auftreten können und sich nach der Behandlung mit Diethylcarbamazin oder Ivermectin verschlimmern können, führten zur Untersuchung der Nierenfunktion bei Patienten mit Onchozerkose vor und nach einer Ivermectin-Behandlung.
Das Auftreten von Nierenauffälligkeiten wurde in einer bevölkerungsbasierten Studie in einem mesoendemischen Dorf (40 % Mikrofilarienträger), in einer Patientengruppe mit generalisierter oder hyperreaktiver Form der Onchozerkose und bei 46 Patienten untersucht, die mit einer Einzeldosis von 150 Mikrogramm/kg Ivermectin behandelt wurden. Alle Personen aus allen drei Studiengruppen wurden klinisch untersucht, es wurden Hautschnittproben entnommen, serologische Tests auf Onchozerkose durchgeführt und gegebenenfalls eine Nodulektomie vorgenommen. Außerdem erfolgten Tests auf Malaria, Schistosomiasis, intestinale Nematoden und Hepatitis B sowie Bestimmungen von Serumglukose, Kreatinin, IgE und Elektrophorese.
Der Urin wurde auf Erythrozyten, Leukozyten, Protein, Nitrite, pH, Glukose, Ketonkörper, Urobilinogen und Kreatinin untersucht. Alle Patienten wurden per Nierensonographie untersucht. Es gab keinen Unterschied bei Nierenfunktion und Ultraschallbefunden zwischen Patienten mit und ohne Onchozerkose. Eine erhöhte Proteinurie (über 70 mg/g Kreatinin) war häufig und trat bei 47 % der Patienten mit Onchozerkose und bei 63 % der Patienten ohne Onchozerkose auf. Bei den 46 Patienten, die eine Einzeldosis von 150 Mikrogramm/kg erhalten hatten, gab es nach 2 und 5 Tagen einen leichten, aber statistisch signifikanten Anstieg der Gesamtproteinurie, besonders bei 16 Patienten mit hoher Mikrofilarienzahl vor der Behandlung. Die Auffälligkeiten waren gering und ohne klinische Relevanz. Weder die Onchozerkose selbst noch die Behandlung mit Ivermectin waren mit Störungen der Nierenfunktion assoziiert.
Haut
Ein gewisses Maß an Pruritus, Schmerzen oder Brennen ist unter Ivermectin üblich. Hautausschläge oder Hautödeme können auftreten, und bereits bestehende Beschwerden dieser Art können sich verschlimmern. Die Haut über Hämatomen kann verfärbt sein. Schwellungen der Gliedmaßen und des Gesichts, ähnlich den dermatologischen Symptomen, sind wahrscheinlich Reaktionen auf Abbauprodukte der Helminthen.
Patienten mit schwerer Hautbeteiligung ("Sowda") als Ausprägung ihrer Onchozerkose können eine vorübergehende Verschlimmerung erleben. Der Verlauf ist jedoch günstig, und bei späteren Behandlungen treten mit großer Wahrscheinlichkeit keine erneuten Probleme auf.
Ausschläge und Lymphknotenschwellungen scheinen bei Patienten mit erworbenem Immundefektsyndrom (AIDS), die Ivermectin einnehmen, häufiger aufzutreten.
Muskel-Skelett-System
Gelenk- oder Knochenschmerzen sind häufig, in der Regel jedoch mild; in einer Studie traten Myalgien bei 33 % und Arthralgien bei 33 % auf.
Fortpflanzungssystem
Orchitis oder Epididymitis mit Hodenschmerzen tritt bei einigen Patienten als Teil der akuten Reaktion auf das Absterben der Parasiten auf.