Diflucan (Fluconazol)

Dosierungen
Diflucan 50 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 60 | €0,81 | €48,48 | |
| 90 | €0,72 | €64,65 | |
| 120 | €0,67 | €80,81 | |
| 180 | €0,63 | €113,98 | |
| 270 | €0,61 | €164,17 | |
| 360 | €0,59 | €211,80 |
Diflucan 100 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 30 | €1,45 | €43,38 | |
| 60 | €1,09 | €65,50 | |
| 90 | €0,97 | €87,61 | |
| 120 | €0,91 | €109,73 | |
| 180 | €0,85 | €153,11 | |
| 270 | €0,81 | €218,60 |
Diflucan 150 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 30 | €1,84 | €55,29 | |
| 60 | €1,38 | €82,51 | |
| 90 | €1,22 | €109,73 | |
| 120 | €1,15 | €137,80 | |
| 180 | €1,07 | €192,24 | |
| 270 | €1,02 | €274,74 |
Diflucan 200 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 30 | €2,89 | €86,76 | |
| 60 | €2,10 | €125,89 | |
| 90 | €1,82 | €164,17 | |
| 120 | €1,69 | €203,29 | |
| 180 | €1,55 | €279,85 | |
| 270 | €1,47 | €397,23 |
Diflucan 400 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 30 | €4,82 | €144,60 | |
| 60 | €3,62 | €216,90 | |
| 90 | €3,22 | €290,05 | |
| 120 | €3,03 | €363,21 | |
| 180 | €2,83 | €508,66 | |
| 270 | €2,69 | €726,41 |
Zahlung & Versand
Ihre Bestellung wird sorgfältig verpackt und innerhalb von 24 Stunden versendet. So sieht ein typisches Paket aus.
Die Sendung hat die Größe eines normalen privaten Briefes (24x11x0,7 cm), ohne Hinweis auf den Inhalt.



| Versandmethode | Voraussichtliche Lieferung |
|---|---|
| Express Kostenlos für Bestellungen über €300,00 | Voraussichtliche Lieferung nach Deutschland: 4-7 Tage |
| Standard Kostenlos für Bestellungen über €200,00 | Voraussichtliche Lieferung nach Deutschland: 14-21 Tage |











Rabattcoupons
- Neujahrstag - 1. Januar 2026 9% NEUJAHR9
- Heilige Drei Könige - 6. Januar 2026 5% DREIKOENIGE5
- Tag der Arbeit - 1. Mai 2026 6% ARBEIT6
- Tag der Deutschen Einheit - 3. Oktober 2026 8% EINHEIT8
- Allerheiligen - 1. November 2026 6% ALLERHEILIGEN6
- Heiligabend - 24. Dezember 2026 9% HEILIGABEND9
- Weihnachten - 25. Dezember 2026 10% WEIHNACHTEN10
- Zweiter Weihnachtstag - 26. Dezember 2026 9% ZWEITER9
- Silvester - 31. Dezember 2026 8% SILVESTER8
Markennamen
| Land | Markennamen |
|---|---|
 Argentinien Argentinien | Candimicol Damicol Femixol Flucoginkan Fluconovag Fluzol Fungicil Fungocina Fungototal Honguil Plus Klonarizol Klonazol Micolis Novo Mutum Naxo C Nifurtox Niofen Periplum Ponaris Proseda F Triflucan |
 Australien Australien | Dizole Fluzole Ozole |
 Belgien Belgien | Candizole Fungimed |
 Brasilien Brasilien | Candix Candizol Celozol Farmazol Floltec Flucanil Flucanol Flucazol Flucocin Flucodan Flucoltrix Flucomed Fluconal Fluconax Fluconeo Fluconid Flucozen Flucozix Flunal Flunazol Fluotec Flusan Flutec Fungnon Glyflucan Helmicin Lertus Monipax Pantec Pronazol Riconazol Teczol Triazol Unizol Zelix Zolanix Zolmic Zolstatin Zoltec Zoltren |
 Deutschland Deutschland | Canex Canifug Fluco Fluc Flucobeta Flucoderm FlucoLich Flunazul Fungata |
 Dänemark Dänemark | Conasol Fungal |
 Frankreich Frankreich | Beagyne Triflucan |
 Griechenland Griechenland | Azoflu Azzol-S Dalrich Falipan Farviron Figalol Flucalit Flucocaps Flucodrug Flucofin Fluconapen Flucoran Flucozol Flukatril Flusenil Fluzomic Fumecal Funadel Fungo Fungram Fungustatin Fungusteril Fuxilidin Gynosant Hadlinol Medoflucon Mycazole Neomycol Opumyk Rifagen Stabilanol Tierlite Varmec Zidonil |
 Italien Italien | Biozolene Elazor Flumicon Lefunzol Riflax Winch |
 Malaysia Malaysia | Avezol Biozole Flucon Fluconol Flucoric Flugal Fukole Medoflucon Odaft Stalene Zolstan |
 Mexiko Mexiko | Afungil Bioxel Candizol Difusel Fectrin Fharder Fleridux Flucoxan Fludisol Fluhexal Flukenol Flukezol Fluxes Fluxicap Fluzor Funser Lanfluzol Menifar Neofomiral Ongicil Oxifungol Ranflu Solarisol Terplex Waynazol Zilrin Zoldicam Zonal |
 Neuseeland Neuseeland | Canesten Fluconazole Flucazole |
 Niederlande Niederlande | Flucoderm |
 Polen Polen | Flucofast FlucoLEK Fluconazin Flumycon Mycomax Mycosyst |
 Portugal Portugal | Azoflune Fludocel Maxflin Reforce Supremase |
 Spanien Spanien | Citiges Lavisa Loitin Nesporac Solacap |
 Tschechien Tschechien | Diflazon Fluco Forcan Mycomax Mycosyst Mykohexal |
 Türkei Türkei | Biocanol Candidin Flucan Fluzole Fungan Kandizol Lumen Triflucan Trizol Zolax |
 Ungarn Ungarn | Dermyc Diflazon Flucohexal Flucoric Mycosyst Nofung |
| Hersteller | Markennamen |
|---|---|
| Cipla Limited | FCN Flucalup Forcan FZ |
| Inc. | FCN Flucalup Forcan FZ |
| Intas Pharmaceuticals Ltd. | FCN Flucalup Forcan FZ |
| Lupin Pharmaceuticals | FCN Flucalup Forcan FZ |
| Zenlabs Pharmaceutical Inc. | FCN Flucalup Forcan FZ |
Beschreibung
Fluconazol ist ein häufig eingesetztes Antimykotikum zur Behandlung von Hefe- und anderen Pilzinfektionen. Es hemmt das Wachstum der Pilze im Körper. In Deutschland wird es oft verschrieben, wenn eine wirksame und unkomplizierte orale Behandlung gebraucht wird, unter anderem in der hausärztlichen Versorgung und in der Dermatologie. Es ist in verschiedenen Stärken erhältlich.
Anwendungsgebiete
Lesen Sie vor dem Online-Kauf von Fluconazol wichtige Informationen zu diesem Arzneimittel.
Fluconazol wird zur Behandlung von oropharyngealer, ösophagealer oder vulvovaginaler Candidiasis sowie anderer schwerer systemischer Candida-Infektionen eingesetzt, zum Beispiel Harnwegsinfektionen, Peritonitis, Candidämie, disseminierte Candidiasis, Meningitis und Pneumonie. Außerdem wird es zur Behandlung von Meningitis durch Cryptococcus neoformans sowie von Blastomykose, Kokkidioidomykose und Histoplasmose angewendet.

Fluconazol wurde auch bei weniger schweren Infektionen angewendet, etwa bei oberflächlichen Pilzinfektionen, Dermatophytosen und Onychomykose. Darüber hinaus wird es zur Vorbeugung schwerer Pilzinfektionen, zum Beispiel Kokkidioidomykose, Kryptokokkose und mukokutaner Candidiasis, bei Patienten mit HIV-Infektion sowie bei anderen immungeschwächten Personen eingesetzt, etwa bei Krebspatienten oder nach Knochenmarktransplantation.
Vor Beginn der Behandlung mit Fluconazol sollten geeignete Proben für Pilzkulturen und andere relevante Labortests, zum Beispiel Serologie und Histopathologie, entnommen werden, um den verursachenden Erreger zu isolieren und zu identifizieren. Die Behandlung kann bereits begonnen werden, während die Ergebnisse dieser In-vitro-Tests noch ausstehen; sobald die Befunde vorliegen, sollte die Therapie entsprechend angepasst werden. Wenn In-vitro-Empfindlichkeitstests für Fluconazol durchgeführt werden, sollten die Ergebnisse vorsichtig beurteilt werden, da die derzeit verfügbaren Tests die In-vivo-Wirkung von Fluconazol möglicherweise nicht genau widerspiegeln.
Candida-Infektionen
Oropharyngeale und ösophageale Candidiasis
Fluconazol zum Einnehmen oder als intravenöse Behandlung wird zur Therapie der oropharyngealen Candidiasis bei immungeschwächten Erwachsenen mit erworbenem Immunschwächesyndrom (AIDS), fortgeschrittenem AIDS-assoziiertem Komplex (ARC), malignen Erkrankungen oder anderen schweren Grunderkrankungen eingesetzt. Es wird ebenfalls oral oder intravenös zur Behandlung der ösophagealen Candidiasis bei Erwachsenen mit AIDS, malignen Erkrankungen oder anderen schweren Grunderkrankungen verwendet, einschließlich progressiver systemischer Sklerose.
Fluconazol scheint mindestens ebenso wirksam zu sein wie andere Antimykotika, die zur Erstbehandlung oropharyngealer und/oder ösophagealer Candida-Infektionen eingesetzt werden, und ist in manchen Fällen wirksamer. Es gilt als Mittel der Wahl bei diesen Infektionen.
Fluconazol führte bei 79-100 % der Patienten mit oropharyngealer Candidiasis zu einer klinischen Abheilung der Symptome und Krankheitszeichen; mikrobiologische Heilungen wurden jedoch in der Regel nur bei 44-87 % der Patienten erreicht. Die Rückfallrate kann besonders bei Neutropenikern hoch sein. Bei Erwachsenen mit endoskopisch gesicherter ösophagealer Candidiasis erreichte Fluconazol bei etwa 61-93 % der Patienten eine klinische Besserung der Symptome. In einer Studie mit Erwachsenen mit ösophagealer Candidiasis und progressiver systemischer Sklerose wurde bei etwa 93 % der Patienten innerhalb von 2-4 Wochen eine mykologische Heilung erzielt. Dennoch lag die Rückfallrate innerhalb von 3 Monaten nach Absetzen der Behandlung bei nahezu 100 %.
HIV-infizierte Patienten mit schweren oder wiederkehrenden Episoden einer oropharyngealen oder ösophagealen Candidiasis können von einer langfristigen unterdrückenden oder Erhaltungstherapie zur Vorbeugung von Rückfällen profitieren.
Einige Kliniker sehen eine lokale Behandlung mit oralem Clotrimazol oder oralem Nystatin als Mittel der Wahl bei unkomplizierter oropharyngealer Candidiasis bei HIV-Infizierten an und empfehlen systemische Antimykotika, etwa orales Fluconazol, orales Itraconazol oder orales Ketoconazol, für Fälle, die auf lokale Mittel nicht ansprechen, sowie für schwere Verläufe mit Beteiligung der Speiseröhre. Andere Kliniker bevorzugen dagegen ein orales Azol-Antimykotikum als Erstbehandlung.
Orales Fluconazol oder Itraconazol als orale Lösung sind mindestens ebenso wirksam wie lokale Therapien. In einer Studie mit HIV-infizierten Erwachsenen mit oropharyngealer Candidiasis lagen die Ansprechraten und mykologischen Ausheilungsraten nach 14 Tagen Behandlung bei 100 % beziehungsweise 75 % unter oralem Fluconazol (100 mg einmal täglich) und bei 65 % beziehungsweise 20 % unter lokalem Clotrimazol (10-mg-Lutschtablette 5-mal täglich). In einer weiteren Studie war eine 14-tägige Behandlung mit oralem Fluconazol (100 mg einmal täglich als orale Suspension) wirksamer als 14 Tage lokales Nystatin (500.000 Einheiten als orale Suspension 4-mal täglich). Die mykologische Heilungsrate betrug 60 % in der Fluconazol-Gruppe und 6 % in der Nystatin-Gruppe; die Rückfallrate an Tag 42 lag bei 27 % beziehungsweise 11 %. Für Aussagen zur langfristigen Vergleichswirksamkeit von Fluconazol und anderen Antimykotika werden noch Langzeitdaten benötigt.
Zur Behandlung einer ösophagealen Candidiasis ist eine systemische antiinfektive Therapie notwendig. Einige Kliniker geben an, dass eine 14- bis 21-tägige Behandlung mit oralem Fluconazol (100 mg einmal täglich) oder oraler Itraconazol-Lösung (200 mg einmal täglich) sehr wirksam ist, während orales Ketoconazol weniger wirksam ist. Bei fehlendem Ansprechen auf orales Fluconazol empfehlen diese Kliniker eine orale Itraconazol-Lösung. Bei therapierefraktären Verläufen kann intravenöses Amphotericin B eingesetzt werden. In einer randomisierten, multizentrischen, doppelblinden Studie bei Erwachsenen mit AIDS und endoskopisch bestätigter ösophagealer Candidiasis wurde eine orale Fluconazoltherapie (initial 100 mg täglich, Steigerung auf 200 mg täglich bei fehlender Besserung innerhalb von 1-2 Wochen) mit oralem Ketoconazol (initial 200 mg täglich, Steigerung auf 400 mg täglich bei fehlender Besserung innerhalb von 1-2 Wochen) über bis zu 8 Wochen verglichen. Dabei wurden eine endoskopische Heilung und ein Abklingen der Symptome bei 91 % beziehungsweise 85 % der mit Fluconazol Behandelten erreicht, gegenüber 52 % beziehungsweise 65 % der Patienten unter Ketoconazol. Ergebnisse einer weiteren Studie deuten darauf hin, dass Patienten unter Fluconazol möglicherweise eine kürzere Initialtherapie benötigen als unter Ketoconazol.
Vulvovaginale Candidiasis
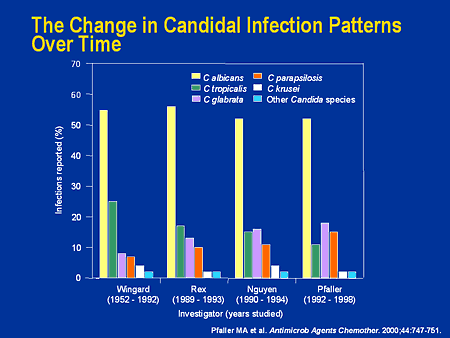
Orales Fluconazol wird zur Behandlung unkomplizierter vulvovaginaler Candidiasis und zur Behandlung komplizierter vulvovaginaler Candidiasis bei nicht schwangeren Frauen eingesetzt. Vor Beginn einer antimykotischen Therapie bei einer Frau mit Anzeichen und Symptomen einer unkomplizierten vulvovaginalen Candidiasis sollte die Diagnose entweder durch den Nachweis von Hefen oder Pseudohyphen in der direkten mikroskopischen Untersuchung des Vaginalsekrets (10 % Kaliumhydroxid [KOH]-Nasspräparat oder Gram-Färbung) oder durch eine Kultur bestätigt werden. Der kulturelle Nachweis von Candida ohne Symptome rechtfertigt keine antimykotische Behandlung, da etwa 10-20 % der Frauen vaginal mit Candida oder anderen Hefen besiedelt sind. Bei Frauen mit wiederkehrender vulvovaginaler Candidiasis sollten Vaginalkulturen angelegt werden, um die Diagnose zu sichern und ungewöhnliche Candida-Arten, zum Beispiel C. glabrata, zu identifizieren.
Unkomplizierte vulvovaginale Candidiasis
Orales Fluconazol behandelt eine unkomplizierte vulvovaginale Candidiasis wirksam, wenn es als Einzeldosis gegeben wird. Eine orale Einzeldosis von 150 mg führt bei nicht schwangeren Frauen mit unkomplizierter vulvovaginaler Candidiasis in etwa 90-100 % der Fälle innerhalb von 5-16 Tagen zu einer klinischen Heilung, also zum Fehlen von vulvovaginalem Brennen, Juckreiz, Schwellung, Erythem, Exkoriationen, Dyspareunie und/oder Ulzerationen sowie zu einer deutlichen Verringerung des vaginalen Ausflusses, und in etwa 77-100 % zu einer mykologischen Heilung. Nach 27-62 Tagen liegen die klinischen und mykologischen Heilungsraten bei 61-90 %, und die Rate von Rezidiv, Reinfektion oder Rekolonisation beträgt etwa 23 %. Mehrere Studien deuten darauf hin, dass eine orale Einzeldosis von 150 mg bei diesem Krankheitsbild ebenso wirksam ist wie mehrfache intravaginale Anwendungen von Clotrimazol, Econazol, Miconazol oder Terconazol. Außerdem ist eine Einzeldosis orales Fluconazol ebenso wirksam wie orale Behandlungen mit Itraconazol oder Ketoconazol.
In kontrollierten Studien bei Patientinnen mit vulvovaginaler Candidiasis waren die klinischen und mykologischen Heilungsraten nach 14 und 30-35 Tagen bei Patientinnen, die eine orale Einzeldosis Fluconazol (150 mg) erhielten, ähnlich wie bei Patientinnen, die intravaginal Clotrimazol (100 mg Vaginaltablette einmal täglich über 7 Tage) oder Miconazol (100 mg Vaginalcreme einmal täglich über 7 Tage) erhielten. Nach 14 Tagen lag die klinische Heilungsrate unter Fluconazol bei etwa 95-96 % und unter Clotrimazol oder Miconazol bei 95-97 %; die mykologische Heilungsrate betrug 77-80 % unter Fluconazol und 72-82 % unter Clotrimazol oder Miconazol. Nach 30-35 Tagen lagen die klinischen Heilungsraten bei etwa 69-75 % unter Fluconazol und 72-80 % unter Clotrimazol oder Miconazol; die mykologischen Heilungsraten betrugen 61-63 % unter Fluconazol beziehungsweise 57-63 % unter Clotrimazol oder Miconazol.
In Deutschland wird unkomplizierte vulvovaginale Candidiasis, also eine leichte bis mittelschwere, sporadische oder seltene Infektion, die sehr wahrscheinlich durch C. albicans verursacht wird und bei immunkompetenten Frauen auftritt, in der Regel mit einem intravaginalen Azol-Antimykotikum behandelt, zum Beispiel Butoconazol, Clotrimazol, Miconazol, Terconazol oder Tioconazol, entweder als Einzeldosis oder als Kurzzeittherapie. Alternativ kommt eine einmalige orale Dosis Fluconazol infrage. Diese Behandlungen gehen bei ansonsten gesunden, nicht schwangeren Frauen mit unkomplizierten Infektionen üblicherweise mit klinischen und mykologischen Heilungsraten von 80-90 % einher. Einige Kliniker sehen die orale Einzeldosis Fluconazol als Vorteil gegenüber der herkömmlichen intravaginalen Behandlung, weil sie die Therapietreue verbessern und gleichzeitig eine mögliche rektale Infektion als Infektionsquelle verringern oder beseitigen könnte. Bei der Abwägung zwischen oraler und intravaginaler Behandlung sollten jedoch die potenzielle Toxizität, zum Beispiel Hepatotoxizität, und das Risiko von Arzneimittelwechselwirkungen unter der oralen Therapie berücksichtigt werden. Auch treten unerwünschte Wirkungen nach einer oralen Einzeldosis häufiger auf als unter intravaginaler Behandlung, was ebenfalls bedacht werden sollte.
Komplizierte und rezidivierende vulvovaginale Candidiasis
Orales Fluconazol wird zur Behandlung komplizierter vulvovaginaler Candidiasis eingesetzt, einschließlich wiederkehrender und schwerer Infektionen. Von komplizierter vulvovaginaler Candidiasis spricht man bei wiederkehrenden oder schweren Infektionen, bei Infektionen durch Candida-Arten außer C. albicans oder wenn sie bei Schwangeren beziehungsweise bei Frauen mit Grunderkrankungen wie schlecht eingestelltem Diabetes, Schwächezuständen oder Immunsuppression auftreten.
Optimale Behandlungsschemata für wiederkehrende vulvovaginale Candidiasis, in der Regel definiert als 4 oder mehr Episoden symptomatischer vulvovaginaler Candidiasis pro Jahr, sind noch nicht abschließend festgelegt. Zwar spricht jede durch C. albicans verursachte Episode auf die übliche orale Einzeldosis Fluconazol oder auf eine Kurzzeitbehandlung mit intravaginalen Antimykotika an, für eine mykologische Remission kann jedoch eine längere Initialtherapie nötig sein, und zur Vorbeugung weiterer Rückfälle kann eine langfristige Erhaltungstherapie erforderlich werden. In Deutschland verwenden Kliniker üblicherweise zunächst ein intensiveres Schema mit 7-14 Tagen intravaginaler Azol-Therapie oder ein 2-Dosis-Schema mit oralem Fluconazol (150 mg, Wiederholung nach 3 Tagen), gefolgt von einer Erhaltungstherapie über 6 Monate. Für die Erhaltungstherapie kommen intravaginales Clotrimazol (500 mg einmal wöchentlich), orales Ketoconazol (100 mg einmal täglich), orales Fluconazol (100-150 mg einmal wöchentlich) oder orales Itraconazol (400 mg einmal monatlich oder 100 mg einmal täglich) infrage. Diese Erhaltungstherapien verringern Rückfälle wirksam; dennoch erkranken 30-40 % der Frauen erneut, sobald die Behandlung beendet wird.
Die Ansprechrate auf eine Kurzzeittherapie mit Antimykotika ist bei Patientinnen mit schwerer vulvovaginaler Candidiasis, also bei ausgeprägtem vulvärem Erythem, Ödemen, Exkoriationen und Fissuren, geringer. Für diese Infektionen wird entweder ein 2-Dosis-Schema mit oralem Fluconazol (150 mg, Wiederholung nach 3 Tagen) oder eine 7-14-tägige intravaginale Azol-Therapie empfohlen. Solche längeren Behandlungen können auch bei Frauen mit Grunderkrankungen notwendig sein, die mit einer Schwächung einhergehen, zum Beispiel schlecht eingestelltem Diabetes oder einer Kortikosteroidtherapie. Vulvovaginale Candidiasis tritt bei Frauen mit HIV-Infektion häufiger und schwerer auf als bei Frauen ohne HIV. Diese Infektionen gelten bei Frauen als frühes Anzeichen des erworbenen Immunschwächesyndroms (AIDS). Obwohl die optimale Therapie für wiederkehrende vulvovaginale Candidiasis bei HIV-infizierten Frauen noch nicht festgelegt ist, gibt es derzeit keine Hinweise darauf, dass die üblicherweise empfohlenen intravaginalen oder oralen Antimykotika bei HIV-Infizierten schlechter ansprechen. Daher empfehlen die Zentren für Krankheitskontrolle und -prävention (CDC) und andere Fachleute, vulvovaginale Candidiasis bei HIV-infizierten Frauen genauso zu behandeln wie bei Frauen ohne HIV-Infektion.
Wiederkehrende vulvovaginale Candidiasis kann selten durch resistente Stämme von C. albicans und häufiger durch andere Candida-Arten mit verminderter Empfindlichkeit gegenüber Azol-Antimykotika, zum Beispiel C. glabrata, verursacht werden. Es wird vermutet, dass die wiederholte Behandlung rezidivierender vulvovaginaler Candidiasis mit intravaginalen Azolen und der weit verbreitete, unsachgemäße Gebrauch dieser Mittel zur Selbstmedikation zur Auswahl azolresistenter Candida beitragen können. Optimale Therapieoptionen für vulvovaginale Candidiasis durch Candida mit verminderter Empfindlichkeit gegenüber Azolen sind noch nicht klar definiert. In Deutschland wird vulvovaginale Candidiasis durch andere Candida-Arten als C. albicans in der Regel 7-14 Tage lang mit einem anderen Antimykotikum als Fluconazol behandelt; bei Rückfällen kann eine intravaginale Behandlung mit Borsäure-Kapseln (600 mg einmal täglich über 2 Wochen) erwogen werden. Eine Überweisung an Spezialisten wird empfohlen.
Candidämie und andere Candida-Infektionen
Fluconazol wurde wirksam zur Behandlung schwerer Candida-Infektionen der Harnwege, von Peritonitis und von Pneumonie eingesetzt. Es ist auch wirksam bei chronischer mukokutaner Candidiasis, Candidämie, chronischer disseminierter Candidiasis (hepatosplenische Candidiasis), Candida-Endokarditis, Candida-Meningitis, Candida-Osteomyelitis und anderen schweren systemischen Candida-Infektionen. Bei einigen Candida-Infektionen, die nicht auf Amphotericin B angesprochen hatten, war es ebenfalls wirksam. Fluconazol zeigte gute Ergebnisse bei lebensbedrohlichen Candida-Infektionen bei Organtransplantatempfängern unter Immunsuppression. Bei einigen nierentransplantierten Patienten konnten Pilzinfektionen beseitigt werden, ohne die immunsuppressive Therapie zu reduzieren oder abzusetzen.
Sowohl intravenöses Amphotericin B als auch intravenöses oder orales Fluconazol gelten als Mittel der Wahl bei systemischer invasiver Candidiasis; das optimale Behandlungsschema ist jedoch schwer festzulegen, und beide Optionen haben Nachteile. Obwohl Fluconazol oft besser verträglich und einfacher anzuwenden ist als intravenöses Amphotericin B, werden zunehmend Fluconazol-resistente C. albicans-Stämme isoliert, insbesondere bei Patienten mit vorausgegangener Fluconazol-Behandlung, vor allem bei HIV-Patienten. Einige Candida-Infektionen, zum Beispiel Candidämie, werden zudem zunehmend durch Candida-Stämme verursacht, die von Natur aus gegen Fluconazol resistent sind, etwa C. krusei, oder wahrscheinlich resistent sind, etwa C. glabrata. Bei der Wahl des Antimykotikums für die initiale Behandlung invasiver Candida-Infektionen sollten lokale oder einrichtungsspezifische epidemiologische Daten zur Häufigkeit verschiedener Candida-Stämme und ihrer Resistenzmuster, der Kolonisationsstatus, Schwere und Dauer einer Neutropenie oder Immunsuppression sowie eine frühere Fluconazol-Behandlung berücksichtigt werden. Die meisten Kliniker empfehlen intravenöses Amphotericin B, wenn der Erreger bekannt oder vermutlich C. krusei ist; bei Infektionen mit C. lusitaniae wird Fluconazol bevorzugt.
Da eine Candidämie mit erheblicher Morbidität und dem Risiko anhaltender Folgeerkrankungen verbunden ist, wird in der Regel bei allen Patienten mit Candidämie eine antimykotische Therapie empfohlen, unabhängig davon, ob eine Neutropenie vorliegt oder nicht. Zusätzlich sollten vorhandene intravenöse Katheter entfernt und/oder gewechselt werden. Es wird angenommen, dass bei nicht neutropenen Patienten orales Fluconazol einer intravenösen Behandlung mit Amphotericin B vorzuziehen ist, sofern keine Hinweise auf Fluconazol-resistente Erreger vorliegen, der Patient zuvor nicht mit Fluconazol behandelt wurde und eine klinisch stabile Situation besteht. Intravenöses Amphotericin B wird im Allgemeinen bei schwerer Candidämie bevorzugt, insbesondere bei Patienten mit Infektionen durch potenziell Fluconazol-resistente Erreger wie C. krusei oder C. glabrata, bei Patienten mit kürzlich erfolgter Fluconazol-Behandlung sowie bei immungeschwächten Patienten, etwa bei HIV-Infektion. In einer kontrollierten Studie mit immunkompetenten Patienten mit normaler Neutrophilenzahl war die Ansprechrate unter einer konventionellen intravenösen Amphotericin-B-Therapie (über 7 Tage, anschließend dreimal wöchentlich für weitere 10 Tage) und unter Fluconazol (400 mg täglich intravenös über 7 Tage, anschließend weitere 11 Tage oral) vergleichbar. Beide Behandlungsschemata waren ähnlich wirksam. Eine prospektive, randomisierte Studie mit nicht neutropenen und neutropenen Patienten mit dokumentierter oder vermuteter invasiver Candidose zeigte ebenfalls vergleichbare Gesamterfolgsraten unter Amphotericin B und Fluconazol. Weitere Untersuchungen sind jedoch erforderlich, um die Wirksamkeit von Amphotericin B und Fluconazol bei immungeschwächten oder schwer erkrankten Patienten besser beurteilen zu können.
Orales Fluconazol oder intravenöses Amphotericin B werden empfohlen, wenn eine Behandlung der Candidurie angezeigt ist, zum Beispiel bei symptomatischen oder neutropenen Patienten, Frühgeborenen mit niedrigem Geburtsgewicht, Patienten mit Nierentransplantaten oder Patienten mit geplanter urologischer Intervention. Fluconazol wird bevorzugt, sofern die Infektion nicht durch C. krusei oder C. glabrata verursacht wird. Eine Blasenspülung mit konventionellem Amphotericin B wurde ebenfalls angewendet. In einer randomisierten Studie bei hospitalisierten geriatrischen Patienten mit Pilzinfektionen durch C. albicans, C. tropicalis oder C. glabrata beseitigte eine 5-tägige Blasenspülung mit konventionellem Amphotericin B (25 mg Amphotericin B in 500 ml 5 %iger Dextrose-Infusion, verabreicht über einen Blasenkatheter mit 42 ml/h) oder eine 5-tägige orale Fluconazol-Behandlung (initial 200 mg, dann 100 mg täglich für 4 weitere Tage) die Fungurie in 83 % beziehungsweise 66 % der Fälle.
Fluconazol wird auch vorbeugend eingesetzt, um die Häufigkeit von Candidiasis bei Patienten nach Knochenmarktransplantation unter Chemotherapie oder Strahlentherapie zu verringern. Es wurde außerdem als primäre Prophylaxe gegen Pilzinfektionen einschließlich Candidiasis bei einer begrenzten Zahl von Hochrisikopatienten angewendet, zum Beispiel bei neutropenen Krebspatienten, bei Patienten mit Candida-Kolonisation und/oder Kortikosteroidtherapie sowie bei bestimmten AIDS-Patienten.
Fluconazol wurde bei einigen Patienten mit durch Candida verursachter Endophthalmitis mit guten Ergebnissen eingesetzt. Es wurden jedoch auch Behandlungsmisserfolge berichtet, und die Rolle des Arzneimittels bei dieser Infektion ist noch nicht abschließend geklärt. Studien an Kaninchen zeigen, dass Fluconazol ins Auge verteilt wird und das Wachstum von C. albicans im Chorioidea-Retina-Gewebe und im Glaskörper von Kaninchen hemmt, wenn die intravenöse Behandlung innerhalb von 24 Stunden nach der Infektion begonnen wurde. Wurde die Behandlung dagegen erst 7 Tage nach der Infektion begonnen, als die Infektion bereits etabliert war, wurde das Wachstum der Erreger nicht wirksam gehemmt.
Kryptokokken-Infektionen
Fluconazol zum Einnehmen oder als intravenöse Behandlung wird bei immunkompetenten oder immungeschwächten Erwachsenen zur Behandlung von Meningitis durch C. neoformans eingesetzt. Das Medikament war bei der Erstbehandlung der akuten kryptokokkalen Meningitis bei HIV-positiven und HIV-negativen Erwachsenen wirksam und führte bei etwa 34-75 % dieser Patienten zu einer klinischen Besserung der Krankheitszeichen und Symptome. Obwohl Amphotericin B, mit oder ohne zusätzliche Gabe von Flucytosin, als Ersttherapie der kryptokokkalen Meningitis gilt, ist Fluconazol bei Patienten mit weniger schwerer Erkrankung eine Alternative, da es in der Regel gut verträglich ist und hohe Konzentrationen im Liquor erreicht. Die Erfahrung bei Kindern ist begrenzt, aber Fluconazol kann auch in dieser Altersgruppe als Alternative zu Amphotericin B in Betracht gezogen werden.
Fluconazol war bei einigen Patienten wirksam zur Behandlung einer akuten kryptokokkalen Meningitis, wenn diese auf eine Therapie mit Amphotericin B nicht angesprochen hatten. Es gibt jedoch Hinweise darauf, dass Fluconazol in der frühen Behandlung der akuten kryptokokkalen Meningitis bei AIDS-Patienten weniger wirksam sein könnte als Amphotericin B und den Liquor langsamer sterilisiert. In einer randomisierten multizentrischen Studie bei AIDS-Patienten mit kryptokokkaler Meningitis wurde Amphotericin B (mittlere Dosierung 0,4-0,5 mg/kg/Tag über 10 Wochen mit oder ohne gleichzeitige Gabe von Flucytosin) mit oralem Fluconazol (400 mg am ersten Tag, danach 200-400 mg über 10 Wochen) verglichen. Die Behandlung war bei 40 % der mit Amphotericin B behandelten Patienten und bei 34 % der mit Fluconazol behandelten Patienten wirksam. Obwohl die Gesamtsterblichkeit in beiden Gruppen ähnlich war (14 % unter Amphotericin B versus 18 % unter Fluconazol), war die Sterblichkeit in den ersten 2 Therapiewochen unter Fluconazol höher (15 % gegenüber 8 % unter Amphotericin B). Die Liquorkulturen blieben unter Amphotericin B im Mittel etwa 42 Tage positiv, unter Fluconazol etwa 64 Tage. In einer weiteren Studie bei einer begrenzten Anzahl von AIDS-Patienten mit kryptokokkaler Meningitis wurde Amphotericin B (0,7 mg/kg/Tag für 1 Woche, danach diese Dosis 3-mal wöchentlich für 9 Wochen in Kombination mit Flucytosin 150 mg/kg/Tag) mit oralem Fluconazol (400 mg/Tag über 10 Wochen) verglichen. Die Initialtherapie war bei allen Patienten unter Amphotericin B wirksam, aber nur bei 43 % der Patienten unter Fluconazol; die Liquorkulturen waren im Mittel etwa 16 beziehungsweise 41 Tage positiv. Obwohl die Patientengruppen in dieser Studie hinsichtlich des Schweregrads der kryptokokkalen Infektion vergleichbar waren, war die Zahl der Helfer/Induktor-(CD4+, T4+)-T-Zellen in der Fluconazol-Gruppe niedriger, was die Interpretation erschwert.
Viele Kliniker empfehlen, die Behandlung der kryptokokkalen Meningitis bei HIV-infizierten Patienten mit einem intravenösen Amphotericin-B-Regime zusammen mit Flucytosin für mindestens 2 Wochen zu beginnen oder bis sich der Zustand des Patienten stabilisiert hat. Anschließend folgt in der Regel eine orale Behandlung mit Fluconazol oder Itraconazol für mindestens weitere 8-10 Wochen oder länger. Bis mehr Daten und Erfahrungen vorliegen, halten einige Kliniker eine Initialtherapie mit intravenösem Amphotericin B mit oder ohne Flucytosin, gefolgt von einer Fluconazol-Erhaltungstherapie, zumindest bei Patienten mit schwererer Erkrankung und bei Hochrisikopatienten für besonders sinnvoll. Eine primäre Behandlung mit Fluconazol sollte ihrer Ansicht nach eher Patienten vorbehalten bleiben, die auf Amphotericin B nicht ausreichend ansprechen oder es nicht vertragen, sowie Patienten mit weniger schwerer Erkrankung, zum Beispiel ohne neurologische Manifestationen und mit niedrigen Liquor-Kryptokokken-Antigen-Titern.
Die relative Wirksamkeit einer Initialtherapie mit konventionellem intravenösem Amphotericin B in Kombination mit Flucytosin (100 mg/kg/Tag) oder Placebo über 2 Wochen, gefolgt von oralem Fluconazol (800 mg/Tag für 2 Tage, anschließend 400 mg/Tag für 8 Wochen) oder oralem Itraconazol (600 mg/Tag für 3 Tage, anschließend 400 mg/Tag für 8 Wochen), wurde in einer doppelblinden multizentrischen Studie bei AIDS-Patienten mit kryptokokkenbedingter Meningitis untersucht. Nach 2 Wochen waren die Liquorkulturen bei 60 % der mit Amphotericin B und Flucytosin behandelten Patienten und bei 51 % der Patienten unter Amphotericin B allein negativ. Das klinische Ansprechen auf die anschließende orale Behandlung mit Fluconazol oder Itraconazol war vergleichbar. Die Rate der Liquorsterilisation nach 10 Wochen war jedoch bei den mit Fluconazol behandelten Patienten (72 %) höher als bei den mit Itraconazol behandelten Patienten (60 %).
Ein Behandlungsschema mit oralem Fluconazol (400 mg/Tag bei pulmonalen Infektionen oder 400-800 mg/Tag bei ZNS-Infektionen) und oralem Flucytosin (100-150 mg/kg/Tag) wurde bei einer begrenzten Anzahl von Patienten als alternatives Regime zur Behandlung pulmonaler oder zerebrospinaler kryptokokkaler Infektionen eingesetzt. Obwohl Fluconazol in Kombination mit Flucytosin bei der Behandlung leichter bis mittelschwerer pulmonaler kryptokokkaler Infektionen wirksam sein kann, war dieses Regime bei einigen Patienten mit kryptokokkaler Meningitis nicht wirksam. Für die Erstbehandlung solcher Infektionen wird es daher nicht empfohlen. Außerdem wurde bei HIV-Infizierten unter Fluconazol und Flucytosin zur Behandlung der kryptokokkalen Meningitis eine hohe Häufigkeit von Nebenwirkungen beobachtet, sodass Flucytosin bei 28 % der Patienten abgesetzt werden musste.
Die Sterblichkeitsrate bei AIDS-Patienten während der ersten Episode einer kryptokokkalen Meningitis lag trotz Behandlung mit Amphotericin B bei etwa 25-58 %. Bei AIDS-Patienten, die auf die initiale antimykotische Therapie ansprechen, beträgt die Rückfallrate der kryptokokkalen Infektion 35-65 %. Eine langfristige Erhaltungs- oder Suppressionstherapie mit Antimykotika wird nach der Erstbehandlung in der Regel als notwendig angesehen, sofern es nicht durch eine wirksame antiretrovirale Therapie zu einer Immunerholung gekommen ist.
Orales Fluconazol war wirksam, wenn es zur langfristigen Erhaltungstherapie zur Vorbeugung von Rückfällen der kryptokokkalen Meningitis bei AIDS-Patienten eingesetzt wurde. Ergebnisse einer multizentrischen Studie, in der orales Fluconazol (200 mg einmal täglich) mit intravenösem Amphotericin B (1 mg/kg einmal wöchentlich) zur Rückfallprophylaxe bei AIDS-Patienten mit negativem kryptokokkalem Kulturstatus nach ausreichender initialer Therapie mit Amphotericin B verglichen wurde, zeigen, dass das Fluconazol-Regime wirksamer war, bezogen auf die Verhinderung von Rückfällen einer kulturpositiven Meningitis, und besser vertragen wurde als das Amphotericin-B-Regime. In einer weiteren multizentrischen Studie, in der eine orale Fluconazol-Erhaltungstherapie (100-200 mg/Tag) mit Placebo bei solchen Patienten verglichen wurde, lag das berechnete kumulative Risiko eines kryptokokkalen Rezidivs an irgendeinem Ort nach 1 Jahr täglicher Fluconazol-Therapie bei 5 % gegenüber 100 % unter Placebo.
Die Wirksamkeit einer Fluconazol-Erhaltungstherapie zur Verhinderung eines kryptokokkalen Rückfalls scheint bei Patienten mit persistierender Prostata-Infektion nach primärer antimykotischer Therapie geringer zu sein als bei Patienten insgesamt. Diese verminderte Wirksamkeit kann jedoch zumindest teilweise durch eine Dosiserhöhung ausgeglichen werden. Bei einer begrenzten Anzahl erwachsener AIDS-Patienten mit persistierender Harnwegs-Kryptokokkose einschließlich Prostata-Infektionen nach adäquater primärer Therapie mit Amphotericin B mit oder ohne Flucytosin wegen kryptokokkaler Meningitis führte die orale Fluconazol-Erhaltungstherapie bei den meisten Patienten zu einer mykologischen Heilung. Bei den übrigen Patienten kam es dagegen während der Fluconazol-Erhaltungstherapie zu Rückfällen der Kryptokokkose nach Prostatamassage und/oder zu systemischen Infektionen.
Die Ansprechraten, also eine anhaltende Unterdrückung des durch Prostatamassage ausgelösten Nachweises von Kryptokokken ohne Nachweis eines systemischen oder ZNS-Rückfalls, scheinen bei solchen Patienten dosisabhängig zu sein. Dafür sind in der Regel orale Fluconazol-Dosen von 200-600 mg/Tag und mehrere Wochen bis Monate Erhaltungstherapie erforderlich, bevor sich ein Effekt zeigt. In einer Studie wurde die Wahrscheinlichkeit eines Ansprechens nach 4 Wochen auf 36 % und nach 27 Wochen auf 59 % geschätzt. Relativ hohe Dosierungen, zum Beispiel 600 mg oder mehr täglich, können bei einigen Patienten multiple große prostatitisähnliche Abszesse wirksam sterilisieren. Welche Faktoren ein Ansprechen vorhersagen und welche antimykotische Therapie bei diesen Patienten optimal ist, ist allerdings noch nicht vollständig geklärt. Wegen des Rückfallrisikos weisen einige Kliniker außerdem darauf hin, dass bei allen männlichen Patienten, für die eine niedrig dosierte Fluconazol-Erhaltungstherapie erwogen wird, eine mögliche Prostata als Infektionsherd sorgfältig ausgeschlossen werden sollte.
Orales Fluconazol war bei einer begrenzten Anzahl von Patienten wirksam zur Behandlung kutaner oder subkutaner Kryptokokkosen. Das Medikament wurde auch zur Behandlung der kryptokokkalen Pneumonie bei einigen Patienten eingesetzt, obwohl bei manchen Patienten eine chirurgische Entfernung des Infektionsherdes notwendig war. Dabei sollte berücksichtigt werden, dass eine kryptokokkale Pneumonie Ausdruck einer disseminierten Infektion sein kann.
Kokzidioidomykose
Orales Fluconazol wurde erfolgreich zur Behandlung der durch Coccidioides immitis verursachten Kokzidioidomykose eingesetzt, zum Beispiel bei Meningitis, pulmonalen Infektionen und disseminierten Infektionen einschließlich Weichteil-, Knochen- oder Gelenkbeteiligung. Bei Erwachsenen mit kokzidioidaler Meningitis hat Fluconazol klinische und/oder laborchemische Besserung gezeigt, sowohl allein als auch in Kombination mit einer Therapie mit Amphotericin B. Orales Fluconazol wurde zur Behandlung der kokzidioidalen Meningitis sowohl bei HIV-Positiven als auch bei HIV-negativen Personen eingesetzt. Da Fluconazol im Allgemeinen gut verträglich ist und günstige pharmakokinetische Eigenschaften hat, zum Beispiel hohe Konzentrationen im Liquor nach oraler oder intravenöser Gabe, gilt es bei der Behandlung der kokzidioidalen Meningitis und anderer persistierender kokzidioidaler Infektionen als weniger toxische Alternative zu Amphotericin B. Das gilt vor allem deshalb, weil bei diesen Infektionen meist eine Langzeittherapie erforderlich ist. Fluconazol gilt als Mittel der Wahl zur Behandlung der Kokzidioidomykose; intravenöses Amphotericin B wird jedoch meist für die Initialtherapie schwerer Verläufe bevorzugt, insbesondere bei immungeschwächten Patienten, einschließlich HIV-Infizierter. Weitere Studien sind nötig, um die Wirksamkeit genauer zu beurteilen, die optimale orale Fluconazol-Dosis bei Kokzidioidomykose festzulegen und zu klären, ob das Medikament Morbidität und Mortalität deutlich senkt. Einige Daten deuten darauf hin, dass höhere Fluconazol-Dosen, also 400 mg täglich oder mehr, die Ansprechraten verbessern können. Es wird vermutet, dass relativ niedrige Dosen, zum Beispiel 50-100 mg täglich, das Risiko für ein Rezidiv erhöhen.
Blastomykose
Orales Fluconazol wurde zur Behandlung der durch Blastomyces dermatitidis verursachten Blastomykose eingesetzt, obwohl diese Infektion in Deutschland selten ist und in der Regel Patienten mit entsprechender Reise- oder Expositionsanamnese betrifft. Während orales Itraconazol oder intravenöses Amphotericin B allgemein als Therapie der Wahl bei Blastomykose gelten, können oral angewendetes Fluconazol oder Ketoconazol als Alternativen eingesetzt werden. Intravenöses Amphotericin B wird allgemein bei schweren Infektionen bevorzugt, insbesondere bei Beteiligung des ZNS sowie für die Erstbehandlung einer vermuteten Blastomykose bei immungeschwächten Patienten, einschließlich Menschen mit HIV.
Es gibt Hinweise darauf, dass orales Itraconazol bei der Behandlung der Blastomykose wirksamer sein kann als orales Fluconazol oder Ketoconazol. Viele Kliniker betrachten Itraconazol als das bevorzugte Azol-Antimykotikum zur Behandlung nicht meningealer, nicht lebensbedrohlicher Blastomykosen und empfehlen es auch als Folgetherapie bei Patienten mit schwereren Infektionen nach anfänglicher Besserung unter intravenösem Amphotericin B. Bei der Wahl eines Antimykotikums sollte berücksichtigt werden, dass bei Patienten mit kutaner oder pulmonaler Blastomykose unter einem oralen Antimykotikum, zum Beispiel Ketoconazol, Therapieversagen berichtet wurde, obwohl zum Zeitpunkt der Erstdiagnose eine asymptomatische oder subklinische ZNS-Beteiligung bestand.
Histoplasmose
Orales Fluconazol wurde mit einigem Erfolg zur Behandlung der durch Histoplasma capsulatum verursachten Histoplasmose eingesetzt. Während intravenöses Amphotericin B oder orales Itraconazol als Mittel der Wahl zur Behandlung der Histoplasmose gelten, werden orales Fluconazol oder Ketoconazol als alternative Wirkstoffe angesehen. Orales Fluconazol (400-800 mg/Tag) war bei einer begrenzten Anzahl HIV-infizierter Patienten mit leichter bis mittelschwerer disseminierter Histoplasmose wirksam. Intravenöses Amphotericin B wird jedoch in der Regel für die Erstbehandlung einer schweren, lebensbedrohlichen Histoplasmose bevorzugt, insbesondere bei immungeschwächten Patienten wie HIV-Infizierten. Außerdem gilt orales Itraconazol allgemein als bevorzugtes Azol-Antimykotikum bei leichter bis mittelschwerer Histoplasmose oder als Folgetherapie bei schwereren Infektionen nach Besserung unter Amphotericin B.
Sporotrichose
Fluconazol wird als alternatives Mittel zur Behandlung der Sporotrichose eingesetzt. Intravenöses Amphotericin B gilt üblicherweise als Mittel der Wahl für die Erstbehandlung schwerer, lebensbedrohlicher Infektionen und bei ZNS-Beteiligung. Orales Itraconazol gilt als Mittel der Wahl zur Behandlung kutaner, lymphokutaner oder leichter pulmonaler beziehungsweise osteoartikulärer Sporotrichose sowie als Folgetherapie bei schwereren Infektionen nach Ansprechen auf intravenöses Amphotericin B. Fluconazol wird als Zweitlinientherapie zur Behandlung kutaner, lymphokutaner oder osteoartikulärer Sporotrichose angesehen und sollte nur eingesetzt werden, wenn der Patient Itraconazol nicht verträgt, da es möglicherweise weniger wirksam ist. Einige Kliniker sind zudem der Ansicht, dass Fluconazol bei pulmonaler Sporotrichose nicht wirksam ist und deshalb nicht eingesetzt werden sollte.
Aspergillose
Fluconazol wurde bei einigen Erwachsenen oral, intravenös oder als intrakavitäre Infusion zur Behandlung von Pneumonien oder anderen Atemwegsinfektionen durch Aspergillus fumigatus, A. niger oder A. terreus eingesetzt. In einer Studie zeigte Fluconazol bei Aspergillus-Infektionen eine klinische Wirksamkeit von 23-53 % und bei Infektionen mit A. fumigatus eine mykologische Heilungsrate von etwa 50 %. Insgesamt ergaben sich unter Fluconazol bei der Behandlung von Aspergillus-Infektionen unterschiedliche Resultate. Intravenöses Amphotericin B gilt allgemein als Mittel der Wahl, und Itraconazol ist in der Regel die bevorzugte Alternative zur Behandlung der Aspergillose.
Dermatophytosen
Orales Fluconazol war wirksam bei der Behandlung bestimmter Dermatophytosen, zum Beispiel Tinea capitis, Tinea corporis, Tinea cruris und Tinea pedis, verursacht durch Epidermophyton, Microsporum oder Trichophyton. Orales Fluconazol war auch wirksam bei der Behandlung von Pityriasis (Tinea) versicolor und Onychomykose.
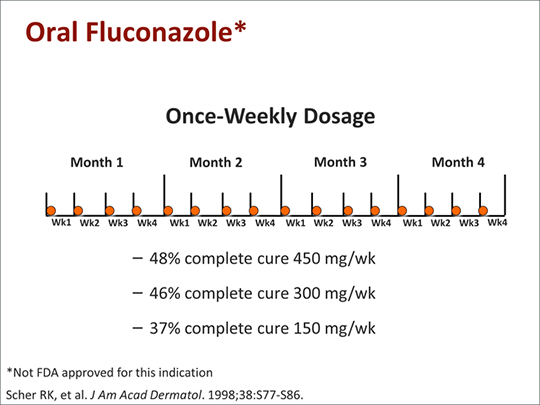
Orales Fluconazol (3-6 mg/kg/Tag für 2-6 Wochen) behandelte Tinea capitis bei Kindern im Alter von 1,5-16 Jahren wirksam und führte bei etwa 88-90 % der Patienten zu einer klinischen und mykologischen Heilung. Zur Behandlung von Tinea corporis, Tinea cruris oder Tinea pedis bei Erwachsenen war orales Fluconazol in einem einmal wöchentlichen Regime wirksam (150 mg einmal wöchentlich für 2-6 Wochen). Es gibt Hinweise darauf, dass dieses einmal wöchentlich verabreichte Regime ebenso wirksam ist wie ein einmal täglich verabreichtes Regime (50 mg/Tag) zur Behandlung dieser Infektionen. Ergebnisse einer randomisierten Studie zeigen, dass die Eradikationsrate am Ende der Behandlung bei Patienten mit Tinea corporis oder Tinea cruris bei 82-88 % unter einmal wöchentlicher Gabe und bei 94-100 % unter einmal täglicher Gabe lag; nach 1 Monat Nachbeobachtung betrugen die Eradikationsraten insgesamt 91-100 % beziehungsweise 91-94 %. Obwohl das optimale Dosierungsschema von oralem Fluconazol zur Behandlung der Onychomykose noch nicht abschließend festgelegt ist, war ein einmal wöchentliches Regime mit oralem Fluconazol (150-450 mg einmal wöchentlich über 3-12 Monate) bei einer begrenzten Anzahl Erwachsener mit Onychomykose der Zehennägel wirksam. Weitere Studien sind jedoch erforderlich, und es gibt Hinweise darauf, dass Fluconazol bei der Behandlung der Onychomykose weniger wirksam sein könnte als orales Itraconazol oder orales Terbinafin.
Tinea corporis und Tinea cruris lassen sich im Allgemeinen gut mit topischen Antimykotika behandeln. Eine orale antimykotische Therapie kann jedoch nötig sein, wenn die Erkrankung ausgeprägt ist, eine Dermatophyten-Follikulitis vorliegt, die Infektion chronisch ist oder nicht auf eine topische Therapie anspricht oder wenn der Patient immungeschwächt ist oder eine Begleiterkrankung vorliegt. Tinea capitis und Tinea barbae werden im Allgemeinen mit einer oralen antimykotischen Therapie behandelt. Während topische Antimykotika bei unkomplizierter Tinea manuum und Tinea pedis meist ausreichen, ist eine orale antimykotische Therapie üblicherweise bei hyperkeratotischen Arealen an Handflächen und Fußsohlen, bei chronischer mokassinartiger trockener Tinea pedis sowie bei Tinea unguium (Onychomykose) erforderlich.
Prävention von Pilzinfektionen bei HIV-Infizierten
Fluconazol wurde bei HIV-Infizierten zur Primärprophylaxe gegen schwere Pilzinfektionen, zum Beispiel Kryptokokkose, sowie zur langfristigen Suppressions- oder Erhaltungstherapie (sekundäre Prophylaxe) zur Verhinderung eines Wiederauftretens oder Rezidivs bestimmter Pilzinfektionen, zum Beispiel Kokzidioidomykose, Kryptokokkose und mukokutane Kandidose, eingesetzt.
In Deutschland orientiert sich die Prävention opportunistischer Infektionen bei HIV-positiven Menschen im Allgemeinen an europäischen und nationalen HIV-Leitlinien. Dazu gehören Empfehlungen zum Schutz vor einer Exposition gegenüber opportunistischen Erregern, zur Verhinderung erster Erkrankungsereignisse und zur Verhinderung von Rückfällen. Diese Empfehlungen raten nicht zu einer primären Prophylaxe, um erste Episoden mukokutaner Kandidosen bei HIV-infizierten Erwachsenen, Jugendlichen, Säuglingen und Kindern zu verhindern. Auch eine routinemäßige primäre Prophylaxe zur Verhinderung erster Episoden von Kokzidioidomykose, Kryptokokkose oder Histoplasmose wird in der Regel nicht empfohlen, auch wenn eine Prophylaxe gegen Kryptokokkose oder Histoplasmose bei ausgewählten Personen erwogen werden kann. HIV-infizierte Erwachsene, Jugendliche, Säuglinge und Kinder, die eine Initialtherapie einer dokumentierten Kokzidioidomykose, Kryptokokkose oder Histoplasmose abgeschlossen haben, sollten in der Regel eine langfristige Suppressions- oder Erhaltungstherapie (sekundäre Prophylaxe) erhalten, um ein Rezidiv zu verhindern. Zusätzlich können HIV-positive Personen mit häufigen oder schweren Rückfällen mukokutaner Kandidosen (oropharyngeal, ösophageal, vaginal) von einer langfristigen Suppressions- oder Erhaltungstherapie profitieren.
Wegen Bedenken hinsichtlich der Anwendung oraler Azol-Antimykotika in der Schwangerschaft sollte Fluconazol bei Schwangeren nicht zur Primärprophylaxe oder zur chronischen Suppressions- beziehungsweise Erhaltungstherapie eingesetzt werden. Wenn eine Frau während einer Fluconazol-Prophylaxe schwanger wird und die Schwangerschaft fortführen möchte, sollte die Prophylaxe beendet werden. Bei allen HIV-infizierten Frauen, die eine orale Azol-Antimykotikatherapie zur Suppression erhalten, werden wirksame Verhütungsmaßnahmen empfohlen. Konventionelles intravenöses Amphotericin B kann bevorzugt werden, wenn bei einer HIV-infizierten Schwangeren eine langfristige Suppressions- oder Erhaltungstherapie gegen Kokzidioidomykose, Kryptokokkose oder Histoplasmose angezeigt ist, insbesondere im ersten Trimenon.
Primärprophylaxe
Kokzidioidomykose
Die aktuellen HIV- und Infektionsleitlinien in Deutschland empfehlen keine routinemäßige primäre Prophylaxe gegen Kokzidioidomykose bei HIV-Infizierten, da die Infektion in Deutschland nicht endemisch ist und vor allem nach Reisen oder Aufenthalten in endemischen Gebieten relevant wird. Einige Kliniker ziehen bei HIV-Infizierten mit positiver CF-Serologie, aber ohne aktive Erkrankung eine primäre Prophylaxe in Betracht, wobei unklar bleibt, ob dies einen Vorteil bringt. Aktive Kokzidioidomykose wurde bei HIV-Infizierten unter einer Azoltherapie wegen anderer Erkrankungen beobachtet. Routinemäßige Hauttests bei asymptomatischen HIV-Patienten werden generell nicht empfohlen, und selbst serologische Tests erfolgen meist nur bei entsprechender Expositionsanamnese oder klinischem Verdacht, nicht routinemäßig.
Kryptokokkose
In Deutschland wird eine routinemäßige primäre Prophylaxe gegen Kryptokokkose in der Regel nicht empfohlen; sie kann jedoch bei HIV-positiven Erwachsenen und Jugendlichen mit CD4+-T-Zellzahlen unter 50/mm3 sowie bei Säuglingen und Kindern mit schwerer Immunsuppression nach altersangepassten Kriterien in Betracht gezogen werden. Auf eine routinemäßige Prophylaxe wird meist verzichtet, weil kryptokokkale Erkrankungen insgesamt relativ selten sind, kein klarer Überlebensvorteil belegt ist und Bedenken hinsichtlich Arzneimittelinteraktionen, Resistenzentwicklung und Kosten bestehen. Dabei sollte auch der mögliche Bedarf an einer primären Prophylaxe oder Suppressionsbehandlung gegen andere Pilzinfektionen wie Kokzidioidomykose, Histoplasmose oder mukokutane Kandidosen berücksichtigt werden. Routinemäßige Serum-Kryptokokken-Antigentests bei asymptomatischen Personen werden generell nicht empfohlen, wenn das Ergebnis die Behandlung nicht verändern würde. HIV-Infizierte können eine Exposition gegenüber Cryptococcus neoformans nicht vollständig vermeiden, und es gibt keine eindeutigen Hinweise darauf, dass nur der Kontakt mit Taubenkot das Risiko für eine Kryptokokkose erhöht.
Orales Fluconazol ist das Mittel der Wahl zur primären Prophylaxe gegen Kryptokokkose bei HIV-infizierten Erwachsenen, Jugendlichen, Säuglingen und Kindern; Itraconazol in Kapselform gilt als Alternative.
Histoplasmose
In Deutschland wird eine primäre Prophylaxe gegen Histoplasmose nur in Ausnahmefällen bei HIV-infizierten Erwachsenen oder Jugendlichen mit CD4+-T-Zellzahlen unter 100/mm3 erwogen, die einem besonders hohen Expositionsrisiko gegenüber Histoplasma capsulatum ausgesetzt sind, zum Beispiel durch berufliche Exposition oder längere Aufenthalte in endemischen Gebieten. Ebenso kann sie bei HIV-infizierten Säuglingen oder Kindern mit schwerer Immunsuppression und relevanter Exposition in endemischen Gebieten in Betracht gezogen werden. Bei einer solchen Entscheidung sollten Kliniker das zu erwartende Expositionsrisiko, die lokale Epidemiologie, mögliche Arzneimittelinteraktionen, Toxizität, Resistenzentwicklung, Kosten sowie den Bedarf an Prophylaxe gegen andere Pilzinfektionen wie Kandidosen oder Kryptokokkosen mit berücksichtigen.
Das Mittel der ersten Wahl zur primären Prophylaxe gegen Histoplasmose bei HIV-infizierten Erwachsenen, Jugendlichen und Kindern ist orales Itraconazol in Kapselform; die USPHS/IDSA nennen keine Alternative zu Itraconazol. Es gibt Hinweise darauf, dass orales Fluconazol zur Verhinderung erster Histoplasmose-Episoden möglicherweise nicht wirksam ist.
Mukokutane Kandidose
Die USPHS/IDSA empfehlen keine primäre Prophylaxe zur Verhinderung erster Episoden einer mukokutanen Kandidose (ösophageal, oropharyngeal, vaginal) bei HIV-infizierten Erwachsenen, Jugendlichen, Säuglingen oder Kindern. Akute mukokutane Kandidosen sind in der Regel gut behandelbar und selten lebensbedrohlich. Hinzu kommen mögliche Resistenzen von Candida, potenzielle Arzneimittelwechselwirkungen und die Kosten einer antimykotischen Prophylaxe.
Prävention eines Rezidivs
Coccidioidomykose
Für HIV-infizierte Personen in Deutschland, die eine Initialtherapie einer dokumentierten Coccidioidomykose abgeschlossen haben, wird in der Regel eine langfristige suppressive oder Erhaltungstherapie (sekundäre Prophylaxe) empfohlen, um das Risiko für Rückfälle oder Rezidive zu senken. Orales Fluconazol wird meist bevorzugt; intravenöses Amphotericin B und Itraconazol-Kapseln zum Einnehmen kommen als Alternativen infrage. In der Praxis wird die langfristige suppressive Therapie bei Erwachsenen, Jugendlichen, Säuglingen und Kindern oft lebenslang fortgeführt. Obwohl das Rückfallrisiko bei wirksamer kombinierter antiretroviraler Therapie mit einem Anstieg der CD4+-T-Zellzahl auf über 100/mm3 sinken kann, ist die Evidenz begrenzt. Ein Absetzen der Prophylaxe sollte daher nur vorsichtig und individuell erwogen werden.
Cryptokokkose
Bei HIV-Infizierten, die eine Initialtherapie einer dokumentierten Cryptokokkose abgeschlossen haben, wird allgemein eine langfristige suppressive oder Erhaltungstherapie (sekundäre Prophylaxe) empfohlen, um Rückfälle oder Rezidive zu verhindern, sofern keine Immunerholung durch eine wirksame Kombination antiretroviraler Therapie erreicht wurde. Orales Fluconazol ist in der Regel das Mittel der Wahl; intravenöses Amphotericin B und Itraconazol-Kapseln zum Einnehmen sind Alternativen. Evidenz aus einer randomisierten, doppelblinden kontrollierten Studie bei HIV-Infizierten mit ausreichend behandelter kryptokokkenbedingter Meningitis deutet darauf hin, dass orales Fluconazol (200 mg einmal täglich) zur suppressiven Therapie wirksamer ist als oral verabreichtes Itraconazol (200 mg einmal täglich), mit kulturnachgewiesenen Rezidivraten von 4 % gegenüber 23 %.

Die suppressive oder Erhaltungstherapie zur Verhinderung eines Rückfalls oder Rezidivs der Cryptokokkose bei HIV-Infizierten wird in der Regel lebenslang fortgeführt, sofern keine Immunerholung durch eine wirksame Kombination antiretroviraler Therapie eingetreten ist. Begrenzte Daten deuten darauf hin, dass das Absetzen der suppressiven oder Erhaltungstherapie bei HIV-infizierten Erwachsenen und Jugendlichen mit niedrigem Rezidivrisiko verbunden sein kann, wenn sie eine Initialtherapie der Cryptokokkose abgeschlossen haben, keine Symptome mehr zeigen und als Reaktion auf die antiretrovirale Therapie über mindestens 6 Monate dauerhaft CD4+-T-Zellzahlen von mehr als 100-200/mm3 aufweisen. Auf dieser Grundlage und in Übereinstimmung mit weiteren Erfahrungen bei anderen opportunistischen Infektionen kann das Absetzen bei sorgfältig ausgewählten Patienten erwogen werden. Ein Rezidiv ist jedoch weiterhin möglich, und die suppressive Therapie sollte wieder aufgenommen werden, wenn die CD4+-T-Zellzahl unter 100-200/mm3 fällt. Die Sicherheit des Absetzens der suppressiven Therapie bei HIV-infizierten Säuglingen und Kindern ist nicht belegt; Kinder sollten nach einer Episode von Cryptokokkose daher lebenslang suppressiv behandelt werden.
Histoplasmose
Für die langfristige suppressive Therapie bei HIV-infizierten Patienten mit dokumentierter, ausreichend behandelter Histoplasmose nennen die USPHS/IDSA orale Itraconazol-Kapseln als Mittel der Wahl; intravenöses Amphotericin B ist eine Alternative.
Mukokutane Candidiasis
In Deutschland sollte bei Erwachsenen und Jugendlichen mit dokumentierter Ösophagus-Candidiasis in der Vorgeschichte, besonders bei mehreren Episoden, eine langfristige suppressive oder Erhaltungstherapie erwogen werden. Dabei muss das Risiko der Selektion resistenter Candida-Stämme berücksichtigt werden. Eine suppressive Therapie sollte auch bei Säuglingen und Kindern mit schwerer, wiederkehrender mukokutaner Candidiasis in Betracht gezogen werden, insbesondere wenn eine Ösophagus-Candidiasis vorliegt. Obwohl viele Behandelnde aus denselben Gründen, aus denen eine routinemäßige Primärprophylaxe nicht empfohlen wird, auch keine routinemäßige Langzeitprophylaxe gegen wiederkehrende oropharyngeale oder vulvovaginale Candidiasis bei HIV-Infizierten empfehlen, kann eine suppressive Therapie bei häufigen oder schweren Rückfällen sinnvoll sein. Dabei sollten Auswirkungen auf Wohlbefinden und Lebensqualität, der Bedarf an Prophylaxe gegen andere Pilzinfektionen, Kosten, Toxizität, Arzneimittelwechselwirkungen sowie mögliche Resistenzen bei Candida und anderen Pilzen sorgfältig gegeneinander abgewogen werden.
Wenn bei HIV-infizierten Erwachsenen, Jugendlichen, Säuglingen oder Kindern mit häufigen oder schweren Rezidiven einer oropharyngealen, ösophagealen oder vaginalen Candidiasis eine langfristige suppressive Therapie zur Prophylaxe angezeigt ist, empfehlen die USPHS/IDSA orales Fluconazol als Mittel der Wahl und Itraconazol als orale Lösung als Alternative.
Die langfristige suppressive Therapie zur Verhinderung von Rückfällen oder Rezidiven pilzlicher Infektionen bei HIV-infizierten Patienten wird häufig lebenslang fortgeführt. Allerdings führte das Absetzen der suppressiven Behandlung bei einigen Patienten, die unter wirksamer kombinierter antiretroviraler Therapie über durchschnittlich 18 Monate (Bereich 4-98 Monate) orales Fluconazol zur Vorbeugung rezidivierender oropharyngealer Candidiasis erhalten hatten, nur bei 10 % innerhalb von 6-11 Monaten zu einem Rückfall. Obwohl das Rezidivrisiko bei Patienten mit einem Anstieg der CD4+-T-Zellzahlen auf über 100/mm3 unter wirksamer antiretroviraler Therapie niedrig sein kann, reichen die bisherigen Daten nicht aus, um das Absetzen der Prophylaxe generell für alle diese Patienten zu empfehlen.
Prävention von Pilzinfektionen bei Transplantationspatienten und Krebspatienten
Fluconazol wird prophylaktisch eingesetzt, um das Auftreten von Candidiasis bei Patienten zu verringern, die sich einer Knochenmarktransplantation (BMT) unterziehen und eine Chemotherapie oder Strahlentherapie erhalten. Das Medikament wird auch zur Prophylaxe pilzlicher Infektionen bei Patienten nach Lebertransplantation sowie bei Krebspatienten eingesetzt, die ein Risiko für Neutropenie und Pilzinfektionen haben. Es gibt Hinweise darauf, dass eine Fluconazol-Prophylaxe bei Transplantations- und Krebspatienten die Häufigkeit oropharyngealer und/oder systemischer Candidiasis vor der Erholung der Neutrophilen senken kann. Außerdem kann sie den Bedarf an einer empirischen antimykotischen Therapie bei diesen Patienten reduzieren. Die Wirksamkeit von oralem Fluconazol (400 mg einmal täglich) zur Prophylaxe pilzlicher Infektionen bei neutropenischen Patienten wurde in einer randomisierten, placebokontrollierten Studie mit 274 Krebspatienten im Alter von 18-80 Jahren untersucht, die eine zytotoxische Chemotherapie oder Konditionierungstherapie für eine BMT erhielten. Während der Anteil der Patienten, die keine empirische Therapie mit intravenösem Amphotericin B benötigten, in beiden Gruppen ähnlich war (57 % der Fluconazol-Empfänger und 50 % der Placebogruppe), wurde ein vollständiger Erfolg ohne Pilzkolonisation bei 37 % der Fluconazol-Empfänger und bei 20 % der Placeboempfänger erreicht. Zudem war die Häufigkeit oberflächlicher Pilzinfektionen bei Fluconazol-Empfängern (7 %) geringer als unter Placebo (18 %), und nur 3 % der Fluconazol-Empfänger entwickelten eindeutige invasive Pilzinfektionen im Vergleich zu 17 % der Placeboempfänger. Obwohl die Fluconazol-Prophylaxe die Gesamtsterblichkeit nicht beeinflusste, zeigt die Intent-to-treat-Analyse, dass in der Fluconazol-Gruppe weniger Todesfälle auf eindeutige invasive Pilzinfektionen zurückzuführen waren (1 von 15) als in der Placebogruppe (6 von 15).
Der Einsatz einer primären antimykotischen Prophylaxe bei Krebspatienten unter myelosuppressiver Therapie oder bei Patienten nach BMT oder solider Organtransplantation ist weiterhin umstritten, insbesondere weil diese Prophylaxe das Risiko einer Kolonisation mit resistenten Pilzen und/oder das Auftreten hochresistenter Organismen fördern kann. Retrospektive Studien haben bei BMT-Empfängern und neutropenischen Patienten unter Fluconazol-Prophylaxe ein erhöhtes Risiko für eine Kolonisation mit Candida krusei gezeigt; in einer Studie lag die Kolonisationsrate bei etwa 41 % der Fluconazol-Empfänger gegenüber 17 % der Patienten ohne Fluconazol-Prophylaxe. Daher empfehlen die meisten Behandelnden eine primäre prophylaktische antimykotische Therapie nur bei sorgfältig ausgewählten Hochrisikopatienten, bei denen der potenzielle Nutzen die möglichen Risiken überwiegt. Viele Experten betonen jedoch, dass kontrollierte, randomisierte Studien den Einsatz von Fluconazol zur Prävention pilzlicher Infektionen bei Krebspatienten und BMT-Empfängern weiter untersuchen sollten.
Dosierung und Anwendung
Fluconazol ist ein Triazol-Antimykotikum zur Behandlung oberflächlicher Schleimhautinfektionen (oropharyngeale, ösophageale oder vaginale Candidiasis) und pilzlicher Hautinfektionen. Es wird auch bei systemischen Infektionen eingesetzt, darunter systemische Candidiasis, Kokzidioidomykose und Cryptokokkose. Außerdem wurde es bei Blastomykose, Histoplasmose und Sporotrichose erprobt.
Fluconazol wird oral oder intravenös in ähnlichen Dosierungen verabreicht. Für die intravenöse Infusion wird es als Lösung mit 2 mg/mL mit einer Geschwindigkeit von 5 bis 10 mL pro Minute (300 bis 600 mL/Stunde) gegeben. In Deutschland sollte die Infusionsgeschwindigkeit gemäß der zugelassenen Fachinformation für die jeweils verwendete Zubereitung gewählt werden.
Bei oberflächlicher Schleimhaut-Candidiasis (außer genitaler Candidiasis) beträgt die übliche Fluconazol-Dosis in Deutschland 50 mg einmal täglich zum Einnehmen. Falls erforderlich, können auch 100 mg einmal täglich verabreicht werden.
Die Behandlung dauert bei oropharyngealer Candidiasis üblicherweise 7 bis 14 Tage (außer bei schwer immungeschwächten Patienten), bei atrophischer oraler Candidiasis im Zusammenhang mit Zahnersatz 14 Tage und bei anderen mukösen Candida-Infektionen einschließlich Ösophagitis 14 bis 30 Tage. In den USA werden höhere Dosierungen empfohlen: eine Anfangsdosis von 200 mg Fluconazol, gefolgt von 100 mg einmal täglich. Die Mindestbehandlungsdauer beträgt bei oropharyngealen Infektionen 14 Tage und bei ösophagealen Infektionen mindestens 21 Tage; außerdem sollte die Behandlung mindestens 14 Tage nach Abklingen der Symptome fortgesetzt werden. Bei ösophagealer Candidiasis können bei Bedarf Dosen bis zu 400 mg einmal täglich gegeben werden.
Orale Anwendung
Fluconazol kann unabhängig von den Mahlzeiten eingenommen werden. Fluconazol-Pulver zur Herstellung einer Suspension sollte bei der Abgabe frisch zubereitet werden, indem 24 mL destilliertes oder gereinigtes Wasser in den Behälter mit 0,35 oder 1,4 g Wirkstoff gegeben werden, um eine Suspension mit 50 beziehungsweise 200 mg/5 mL zu erhalten. Die Flasche sollte kräftig geschüttelt werden, damit sich das Pulver verteilt; vor jeder Anwendung ist die Suspension erneut gut zu schütteln.
Intravenöse Anwendung
Intravenöse Infusionen von Fluconazol sollten einmal täglich mit einer Geschwindigkeit von nicht mehr als 200 mg pro Stunde verabreicht werden. Fluconazol-Injektionen zur intravenösen Infusion sind vor der Anwendung visuell auf Verfärbungen und Schwebstoffe zu prüfen, sofern Lösung und Behälter dies zulassen. Die Injektion ist zu verwerfen, wenn die Lösung trüb ist oder Ausfällungen zeigt oder wenn die Versiegelung nicht intakt ist. Viaflex® Plus Behälter mit Fluconazol sollten durch festes Zusammendrücken des Beutels auf kleinste Undichtigkeiten überprüft werden. Die Injektion sollte verworfen werden, wenn die Behälterversiegelung nicht intakt ist, Undichtigkeiten festgestellt werden oder die Lösung trüb ist oder Ausfällungen enthält. Zusätze dürfen nicht in den Kunststoffinjektionsbehälter eingebracht werden. Die Injektion in Kunststoffbehältern darf nicht in Reihenschaltung mit anderen Kunststoffbehältern verwendet werden, da sonst vor Abschluss der Gabe aus dem Sekundärbehälter eine Luftembolie durch Restluft aus dem Primärbehälter entstehen könnte.
Fluconazol 150 mg als orale Einzeldosis kann bei genitaler Candidose, einschließlich vaginaler Candidose oder Candida-Balanitis, angewendet werden. Dermatophytosen, Pityriasis versicolor und kutane Candida-Infektionen können mit 50 mg Fluconazol einmal täglich oral über einen Zeitraum von bis zu sechs Wochen behandelt werden.
Systemische Candidiasis, kryptokokkenbedingte Meningitis und andere kryptokokkale Infektionen können oral oder als intravenöse Infusion mit Fluconazol behandelt werden. Die Anfangsdosis beträgt 400 mg, gefolgt von 200 bis 400 mg einmal täglich. Die Behandlungsdauer richtet sich nach dem klinischen und mykologischen Ansprechen, beträgt aber üblicherweise mindestens 6 bis 8 Wochen. In Deutschland wird die Behandlung der kryptokokkenbedingten Meningitis im Allgemeinen 10 bis 12 Wochen nach negativen Liquorkulturen fortgeführt.
Fluconazol kann auch einmal täglich in Dosen von 100 bis 200 mg oral oder intravenös zur Rückfallprophylaxe nach einer primären antimykotischen Behandlung der akuten kryptokokkenbedingten Meningitis bei AIDS-Patienten eingesetzt werden. Bei immungeschwächten Patienten mit Risiko für Pilzinfektionen kann Fluconazol prophylaktisch oral oder intravenös in Dosen von 50 bis 400 mg einmal täglich gegeben werden. Allerdings ist eine Langzeitprophylaxe mit dem Auftreten resistenter Organismen verbunden. Die Dosierung für Kinder über 4 Wochen beträgt 3 mg/kg/Tag bei oberflächlichen Infektionen (bei Bedarf kann am ersten Tag eine Lade- bzw. Anfangsdosis von 6 mg/kg verwendet werden) und 6 bis 12 mg/kg/Tag bei systemischen Infektionen. Zur Prophylaxe bei immungeschwächten Kindern können 3 bis 12 mg/kg/Tag gegeben werden. Bei Säuglingen unter 2 Wochen sollten alle diese Dosen alle 72 Stunden verabreicht werden. Bei Säuglingen im Alter von 2 bis 4 Wochen sollten die Dosen alle 48 Stunden gegeben werden.
Bei Kindern sollte eine Maximaldosis von 400 mg einmal täglich nicht überschritten werden; bei Säuglingen gilt zusätzlich eine Obergrenze von 12 mg/kg in den jeweils angegebenen Intervallen. Bei Patienten mit Niereninsuffizienz kann eine Dosisreduktion erforderlich sein.
Hohe Dosierungen
Patienten mit lebensbedrohlichen Infektionen durch Candida spp., Cryptococcus neoformans und Coccidioides immitis wurden mit höheren Dosen behandelt, als in der zugelassenen Fachinformation zu Fluconazol empfohlen werden.
Dosisfindungsstudien haben gezeigt, dass tägliche Dosen von 800 bis 1000 mg Fluconazol wirksam und gut verträglich sind. In einer Studie mit 11 HIV-infizierten Patienten, die 3 Wochen lang 800 bis 1000 mg Fluconazol täglich intravenös und anschließend bis zur negativen Liquorkultur oral erhielten, wurden 6 Patienten nach 10 Wochen als Responder eingestuft, weitere 2 Patienten zeigten eine klinische Besserung. Dosen bis zu 800 mg täglich wurden bei Blastomykose und Kokzidioidomykose eingesetzt, und Dosen von 10 mg/kg/Tag wurden bei disseminierter Candidiasis versucht.
Intermittierende Dosierungen
Es gibt Bedenken wegen der zunehmenden Anwendung von Fluconazol, besonders im Hinblick auf die Auswirkungen einer kontinuierlichen Fluconazoltherapie bei immungeschwächten Patienten auf die Entwicklung von Resistenzen. Dennoch bleibt Fluconazol für die primäre und sekundäre Prophylaxe weit verbreitet. Einige Untersucher haben intermittierende Dosierungen vorgeschlagen, obwohl dies das Risiko für Infektionen mit resistenten Organismen weiter erhöhen kann. Eine einmal wöchentliche Behandlung mit Fluconazol wurde bei Onychomykose und Tinea capitis erprobt.
Verabreichung bei Niereninsuffizienz
Patienten mit Niereninsuffizienz benötigen möglicherweise eine Dosisreduktion. Normale Lade- oder Anfangsdosen von Fluconazol sollten am ersten Behandlungstag verabreicht werden; die folgenden Dosen sollten entsprechend der Kreatinin-Clearance (CC) angepasst werden:
- CC über 50 mL/min: 100 % der empfohlenen Standarddosis;
- CC unter 50 mL/min und keine Dialyse: 50 % der empfohlenen Standarddosis;
- Patienten unter regelmäßiger Hämodialyse: 100 % der empfohlenen Standarddosis nach jeder Dialysesitzung. Bei Einmaldosierungen ist keine Dosisanpassung erforderlich.
Dosierung für Erwachsene
Oropharyngeale und ösophageale Candidiasis
Zur Behandlung einer oropharyngealen oder ösophagealen Candidiasis beträgt die übliche Erwachsenendosis von Fluconazol am ersten Behandlungstag 200 mg als Einzeldosis, gefolgt von 100 mg oder 200 mg einmal täglich. Je nach Ansprechen des Patienten können Dosen bis zu 400 mg einmal täglich verwendet werden. Obwohl die klinischen Anzeichen einer oropharyngealen Candidiasis in der Regel innerhalb weniger Tage nach Beginn der Fluconazoltherapie abklingen, empfehlen die Hersteller und einige Behandelnde, das Arzneimittel mindestens 2 Wochen weiterzugeben, um das Rückfallrisiko zu verringern.

Andere Behandelnde bezweifeln jedoch, dass bei dieser Infektion eine verlängerte Therapie notwendig ist. Patienten mit ösophagealer Candidiasis sollten Fluconazol mindestens 3 Wochen und mindestens 2 Wochen nach Abklingen der Symptome erhalten. Die optimale Dosierung für die Erhaltungstherapie bei Patienten mit oropharyngealer Candidiasis ist nicht gesichert. Orale Dosen von 50-100 mg einmal täglich wurden allgemein als wirksam für die Erhaltungstherapie angesehen; gelegentlich wurden Dosen bis zu 200 mg einmal täglich eingesetzt.
Vulvovaginale Candidiasis
Zur Behandlung einer unkomplizierten vulvovaginalen Candidiasis bei nicht schwangeren Frauen beträgt die übliche orale Fluconazol-Dosis 150 mg als Einmalgabe. Bei der Behandlung rezidivierender vulvovaginaler Candidiasis bei nicht schwangeren Frauen sollten zur mykologischen Remission zwei orale Dosen zu je 150 mg im Abstand von 3 Tagen verabreicht werden. Anschließend sollte zur Rezidivprophylaxe eine Erhaltungstherapie mit 100-150 mg einmal wöchentlich über 6 Monate erfolgen. Ein Regime mit zwei Dosen (zwei Dosen zu je 150 mg im Abstand von 3 Tagen) wird auch zur Behandlung einer schweren vulvovaginalen Candidiasis bei nicht schwangeren Frauen empfohlen.
Leishmaniose
Fluconazol wurde zur Behandlung der kutanen Leishmaniose durch Leishmania major erprobt. In einer randomisierten, doppelblinden, placebokontrollierten Studie erhielten 80 Patienten 6 Wochen lang 200 mg Fluconazol einmal täglich oral; 63 von ihnen zeigten nach 3 Monaten eine vollständige Abheilung der Läsionen, verglichen mit 22 von 65 Patienten in der Placebogruppe. Andere Berichte beschreiben jedoch Ansprechraten, die sich nicht signifikant von Placebo unterschieden.
Andere Candida-Infektionen
Zur Behandlung systemischer Candidiasis beträgt die übliche Erwachsenendosis von Fluconazol 400 mg als Einzeldosis am ersten Behandlungstag, gefolgt von 200 mg einmal täglich. Bei einigen Patienten mit candidaler Harnwegsinfektion und Peritonitis wurden Dosen von 50-200 mg einmal täglich verwendet. Die optimale Dosierung und Behandlungsdauer bei Patienten mit Candidämie, disseminierter Candidiasis und Pneumonie sind nicht etabliert; eine begrenzte Zahl solcher Patienten erhielt jedoch Fluconazol-Dosen von bis zu 400 mg einmal täglich. Einige Behandelnde empfehlen bei invasiver Candidiasis tägliche Fluconazol-Dosen von 400-800 mg. Die Therapie sollte mindestens 4 Wochen und mindestens 2 Wochen nach Abklingen der Symptome fortgeführt werden.
Cryptokokkale Infektionen
Zur Behandlung der kryptokokkenbedingten Meningitis beträgt die übliche Erwachsenendosis von Fluconazol am ersten Behandlungstag 400 mg als Einzeldosis, gefolgt von 200 bis 400 mg einmal täglich. Es gibt Hinweise darauf, dass die 400-mg-Dosis bei dieser Infektion wirksamer ist als niedrigere Dosierungen. Eine höhere Fluconazol-Dosis (800-1000 mg einmal täglich) wurde bei einigen Patienten mit HIV-Infektion zur Behandlung der kryptokokkenbedingten Meningitis eingesetzt. Bei der Initialtherapie der kryptokokkenbedingten Meningitis wird Fluconazol üblicherweise 10-12 Wochen nach Sterilität des Liquors weitergegeben.

Kokzidioidomykose
Zur Behandlung der kokzidioidalen Meningitis bei Erwachsenen werden Fluconazol-Dosen von 200-800 mg einmal täglich empfohlen. Bei AIDS-Patienten mit kokzidioidaler Meningitis werden 400-800 mg Fluconazol täglich empfohlen. Bei einigen Patienten wurde zusätzlich Amphotericin B intrazisternal, intraventrikulär oder intrathekal angewendet.
Blastomykose oder Histoplasmose
Wenn Fluconazol zur Behandlung einer Blastomykose oder Histoplasmose eingesetzt wird, wird eine tägliche Dosis von 400-800 mg empfohlen.
Prävention von Pilzinfektionen bei HIV-Infizierten
Zur Primärprophylaxe gegen Kryptokokkose bei Erwachsenen oder Jugendlichen mit HIV-Infektion und CD4+-T-Zellzahlen unter 50/mm3 kann in Deutschland in ausgewählten Fällen eine orale Fluconazol-Dosis von 100-200 mg einmal täglich in Erwägung gezogen werden.
Es gibt zwar Hinweise darauf, dass Fluconazol 400 mg einmal wöchentlich zur Primärprophylaxe von Pilzinfektionen bei HIV-infizierten Personen wirksam sein kann, dieses Schema ist jedoch nicht Teil der aktuellen USPHS/IDSA-Leitlinien. Weitere Studien sind nötig, um die Wirksamkeit anderer Anwendungsschemata als der täglichen Gabe in der Primärprophylaxe zu beurteilen.
Zur langfristigen suppressiven oder Erhaltungstherapie (sekundäre Prophylaxe) der Kokzidioidomykose bei HIV-infizierten Erwachsenen oder Jugendlichen mit dokumentierter, angemessen behandelter Infektion werden allgemein 400 mg Fluconazol einmal täglich empfohlen. Zur suppressiven oder Erhaltungstherapie zur Verhinderung eines Rückfalls oder Rezidivs der Kryptokokkose bei HIV-infizierten Erwachsenen oder Jugendlichen nach dokumentierter, angemessen behandelter Infektion beträgt die übliche orale Fluconazol-Dosis 200 mg einmal täglich.
Einige Behandelnde empfehlen zur langfristigen suppressiven Therapie gegen Kryptokokkose in den ersten 4 Wochen 400 mg Fluconazol täglich, gefolgt von 200 mg täglich. Wird orales Fluconazol zur langfristigen suppressiven oder Erhaltungstherapie (sekundäre Prophylaxe) zur Verhinderung von Rückfällen oder Rezidiven einer mukokutanen Candidiasis (oropharyngeal, vaginal, ösophageal) bei HIV-infizierten Erwachsenen oder Jugendlichen mit häufigen oder schweren Episoden dieser Candida-Infektionen eingesetzt, empfiehlt das USPHS/IDSA eine Dosis von 100-200 mg einmal täglich.
Obwohl Fluconazol 200 mg einmal wöchentlich zur langfristigen suppressiven Therapie bei HIV-infizierten Frauen mit oropharyngealer oder vaginaler Candidiasis in der Vorgeschichte angewendet wurde, ist dieses Schema in Deutschland keine Routineempfehlung. Es gibt Bedenken, dass eine solche Behandlung zur Entstehung Fluconazol-resistenter Candida-Stämme führen kann. Die langfristige suppressive oder Erhaltungstherapie zur Verhinderung von Rückfällen oder Rezidiven von Pilzinfektionen bei HIV-infizierten Patienten wird im Allgemeinen lebenslang fortgeführt. Bei sorgfältig ausgewählten Erwachsenen und Jugendlichen mit Kryptokokkose, die unter einer wirksamen antiretroviralen Kombinationstherapie eine Immunrekonstitution erreicht haben, kann es jedoch sinnvoll sein, die suppressive oder Erhaltungstherapie zu beenden.
Prävention von Pilzinfektionen bei Transplantationspatienten und Krebspatienten
Zur Vorbeugung einer Candidiasis bei Empfängern von Knochenmarktransplantaten beträgt die empfohlene Fluconazol-Dosis 400 mg einmal täglich. Bei Patienten, bei denen eine schwere Granulozytopenie (Neutrophilenzahl unter 500/mm3) zu erwarten ist, sollte die Behandlung mit Fluconazol einige Tage vor dem erwarteten Beginn der Neutropenie begonnen werden. Sie sollte 7 Tage lang fortgesetzt werden, nachdem die Neutrophilenzahl über 1000/mm3 angestiegen ist.
Dosierung bei Kindern
Die übliche Dosierung von Fluconazol bei Kindern liegt bei 3-12 mg/kg einmal täglich; Dosen über 600 mg täglich werden nicht empfohlen. Der Hersteller gibt an, dass eine Dosierung von 3, 6 oder 12 mg/kg täglich bei Kindern einer Tagesdosis von 100, 200 bzw. 400 mg bei Erwachsenen entspricht. Einige ältere Kinder können Fluconazol ähnlich schnell ausscheiden wie Erwachsene.
Zur Behandlung von Meningitis oder Septikämie durch empfindliche Candida-Arten haben Neugeborene und Säuglinge bis zu einem Alter von 3 Monaten Fluconazol in einer Dosierung von 5-6 mg/kg einmal täglich erhalten, entweder oral oder als intravenöse Infusion über 1 Stunde. Bei einigen Neugeborenen und Säuglingen mit Septikämie wurde eine initiale Aufsättigungsdosis von 10 mg/kg gegeben, gefolgt von 5 mg/kg einmal täglich. Auf Grundlage verfügbarer pharmakokinetischer Daten zu Fluconazol bei Frühgeborenen empfiehlt der Hersteller, dass Neugeborene bis zu einem Alter von 2 Wochen dieselbe Tagesdosis wie ältere Kinder erhalten, jedoch nur alle 72 Stunden.
Oropharyngeale und ösophageale Candidiasis
Zur Behandlung der oropharyngealen oder ösophagealen Candidiasis empfiehlt der Hersteller für Kinder am ersten Tag 6 mg/kg Fluconazol, gefolgt von 3 mg/kg einmal täglich. Bei ösophagealer Candidiasis kann die Dosis je nach Zustand des Patienten und Ansprechen auf die Behandlung bei Bedarf auf bis zu 12 mg/kg täglich erhöht werden. Die Behandlung der oropharyngealen Candidiasis sollte mindestens 2 Wochen fortgesetzt werden, um das Rückfallrisiko zu verringern. Die Behandlung der ösophagealen Candidiasis sollte mindestens 3 Wochen dauern und noch mindestens 2 Wochen nach dem Abklingen der Symptome fortgeführt werden.
Andere Pilzinfektionen
Fluconazol wurde zur Behandlung systemischer Candida-Infektionen bei Kindern in einer Dosierung von 6-12 mg/kg täglich verabreicht. Der Hersteller empfiehlt zur Behandlung der Kryptokokkenmeningitis bei Kindern eine initiale Dosis von 12 mg/kg am ersten Tag, gefolgt von 6 mg/kg einmal täglich. Falls erforderlich, kann die Dosis je nach Zustand und Ansprechen des Patienten auf bis zu 12 mg/kg täglich erhöht werden. Fluconazol sollte 10-12 Wochen nach negativer Liquorkultur weitergegeben werden.
Prophylaxe von Pilzinfektionen bei HIV-infizierten Personen
Die empfohlene orale Fluconazol-Dosis zur Primärprophylaxe gegen Kryptokokkose bei HIV-infizierten Säuglingen und Kindern mit schwerer Immunsuppression beträgt 3-6 mg/kg einmal täglich. Wird orales Fluconazol zur langfristigen suppressiven oder Erhaltungstherapie eingesetzt, um vor einem Rezidiv oder Rückfall einer Kryptokokkose oder mukokutanen Candidiasis (oropharyngeal, ösophageal) bei HIV-infizierten Säuglingen und Kindern zu schützen, beträgt die empfohlene Dosis 3-6 mg/kg einmal täglich. Eine Dosis von 6 mg/kg einmal täglich wird zur Prophylaxe gegen Rezidiv oder Rückfall einer Kokzidioidomykose bei diesen pädiatrischen Patienten empfohlen.
Wechselwirkungen
Insgesamt treten mit Fluconazol weniger Wechselwirkungen auf als mit Itraconazol oder Ketoconazol. Die gleichzeitige Anwendung von Rifampicin und Fluconazol senkt die Plasmakonzentrationen von Fluconazol. Hydrochlorothiazid zusammen mit Fluconazol führte zu klinisch nicht relevanten Erhöhungen der Fluconazol-Plasmaspiegel.
Fluconazol kann den Stoffwechsel einiger anderer Medikamente beeinflussen, vor allem durch Hemmung der Cytochrom-P450-Isoenzyme CYP3A4 und CYP2C9. Das kann die berichteten Anstiege der Plasmakonzentrationen von Bosentan, Ciclosporin, Midazolam, Nevirapin, Amitriptylin, Nortriptylin, Phenytoin, Rifabutin, Sulfonylharnstoffen und Nateglinid, selektiven Cyclooxygenase-2-Hemmern wie Celecoxib und Parecoxib, Tacrolimus, Triazolam, Warfarin und Zidovudin erklären. Fluconazol kann die Bildung eines toxischen Metaboliten von Sulfamethoxazol hemmen. Erhöhte Terfenadin-Konzentrationen nach hohen Fluconazol-Dosen wurden mit EKG-Veränderungen in Verbindung gebracht.
Ein ähnlicher Effekt wird auch bei Astemizol erwartet. Die gleichzeitige Anwendung von Fluconazol und Cisaprid kann jedoch zu erhöhten Cisaprid-Konzentrationen und damit verbundener Toxizität führen und sollte daher vermieden werden. Auch die Anwendung von Fluconazol zusammen mit Astemizol, Cisaprid oder Terfenadin sollte wegen des Risikos von Herzrhythmusstörungen vermieden werden. Synkopen wurden auf erhöhte Amitriptylin-Konzentrationen zurückgeführt, die unter gleichzeitiger Gabe von Amitriptylin und Fluconazol auftraten.
Fluconazol kann auch die Clearance von Theophyllin verringern. Unter Fluconazol wurden sowohl erhöhte als auch erniedrigte Konzentrationen von Verhütungssteroiden berichtet, sodass die Wirksamkeit oraler Kontrazeptiva beeinträchtigt sein kann. Weitere Informationen zu Wechselwirkungen zwischen Medikamenten, die über das Cytochrom-P450-Isoenzym CYP3A verstoffwechselt werden, und Azolen finden sich unter Itraconazol.
Fluorchinolone
Sowohl Levofloxacin als auch Fluconazol können das QT-Intervall verlängern. Die gleichzeitige Anwendung von intravenösem Levofloxacin und Fluconazol führte bei einem Hämodialysepatienten zu einer Episode von Torsade de Pointes.

Mikrobiologische Wechselwirkungen
In vitro wurde gegen Stämme von Candida albicans ein synergistischer antimykotischer Effekt von Terbinafin und Fluconazol beobachtet.
Resistenz
Die Entstehung von Candida-Stämmen, die gegen Fluconazol resistent sind, gewinnt vor allem bei immungeschwächten Patienten, die eine Langzeitprophylaxe mit Fluconazol erhalten, zunehmend an Bedeutung. Neben Resistenzen bei Candida albicans wurden bei diesen Patienten auch Infektionen mit Candida dubliniensis, Candida glabrata und Candida krusei beobachtet, die möglicherweise alle weniger empfindlich gegenüber Fluconazol sind als Candida albicans. Eine sekundäre Resistenz von Candida glabrata wurde während der Fluconazol-Therapie berichtet.
Resistenzen gegen Fluconazol wurden häufiger berichtet als gegen Ketoconazol oder Itraconazol, was mit der breiten Anwendung des Medikaments zusammenhängen könnte. Kreuzresistenzen mit anderen Azolen und mit Amphotericin B wurden ebenfalls beschrieben.
Fluconazol-Resistenz wurde auch bei Cryptococcus neoformans und Histoplasma capsulatum festgestellt. Bei einem HIV-Patienten entwickelte sich während der Behandlung mit Fluconazol eine Histoplasmose. Fluconazol-resistentes C. neoformans wurde bei einem immunkompetenten Patienten ohne vorherige Exposition gegenüber Azol-Antimykotika isoliert.
Fluconazol-Wechselwirkungen mit anderen Arzneimitteln
Alfentanil
In einer randomisierten, doppelblinden, placebokontrollierten Crossover-Studie mit neun Probanden verringerte Fluconazol 400 mg die Clearance von Alfentanil 20 Mikrogramm/kg um 55 % und verstärkte die subjektiven Effekte von Alfentanil.
Amitriptylin
Über eine Wechselwirkung zwischen Fluconazol und Amitriptylin wurde berichtet.
- Ein 12-jähriger Junge mit prostatischem Rhabdomyosarkom hatte über 7 Monate wiederholt Synkopen, während er Fluconazol wegen chemotherapieinduzierter Mukositis einnahm. Fluconazol hatte er zuvor ohne Probleme vertragen, er nahm jedoch zusätzlich eine stabile Dosis Amitriptylin gegen neuropathische Schmerzen ein. Nach dem Absetzen von Amitriptylin traten keine weiteren Episoden mehr auf. Der Zusammenhang wurde durch erneute Gabe bestätigt.
Die gleichzeitige Gabe von Fluconazol erhöht wahrscheinlich die Exposition gegenüber Amitriptylin. Drei Berichte bei Erwachsenen zeigten erhöhte Amitriptylin-Plasmaspiegel unter gleichzeitiger Fluconazol-Gabe; bei einer 57-jährigen Frau verlängerte sich das QT-Intervall, und es kam zu Torsade de Pointes.
Amphotericin
In-vitro-Studien und Tierversuche zeigten widersprüchliche Ergebnisse in Bezug auf einen möglichen Antagonismus zwischen den Wirkungen von Fluconazol und Amphotericin bei Candida-Arten. Große randomisierte, doppelblinde Vergleiche von Fluconazol mit und ohne Amphotericin über 5 Tage bei nicht neutropenischen Patienten mit Candidämie zeigten jedoch keinen Antagonismus, sondern eine schnellere Elimination des Erregers aus dem Blut und einen Trend zu einem besseren Verlauf unter der Kombinationstherapie.
Antazida
Die Aufnahme von Fluconazol nach oraler Gabe wird durch den Magen-pH nicht beeinflusst; daher beeinträchtigen Antazida wie Co-Magaldrox die Absorption nicht.
Antihistaminika
Die gleichzeitige Anwendung von Terfenadin mit Fluconazol kann zu gefährlich hohen Terfenadin-Konzentrationen und kardialer Toxizität führen. Ein ähnlicher Effekt wird auch bei Astemizol vermutet.
Benzodiazepine
Zwölf gesunde Männer wurden in einer randomisierten, doppelblinden Crossover-Studie mit vier Phasen untersucht, um die Wechselwirkung von Fluconazol mit Bromazepam zu bestimmen. Sie erhielten einzelne orale oder rektale Dosen Bromazepam (3 mg) nach einer viertägigen Vorbehandlung mit oralem Fluconazol (100 mg/Tag) oder Placebo. Fluconazol verursachte keine signifikanten Veränderungen der Pharmakokinetik oder Pharmakodynamik von oralem oder rektalem Bromazepam.
Fluconazol erhöhte die Blutkonzentrationen von Midazolam und Triazolam.
Die Effekte von Fluconazol (400 mg Aufsättigungsdosis, gefolgt von 200 mg/Tag) auf die Kinetik von Midazolam wurden bei 10 mechanisch beatmeten Erwachsenen untersucht, die eine stabile Midazolam-Infusion erhielten. Nach Beginn der Fluconazol-Therapie stiegen die Midazolam-Konzentrationen auf das bis zu Vierfache an; diese Veränderungen waren bei Patienten mit Niereninsuffizienz am stärksten. Während der Studie sank das Verhältnis von a-Hydroxy-Midazolam zu Midazolam fortlaufend. Die Autoren schlossen daraus, dass bei Intensivpatienten unter Fluconazol die Midazolam-Dosis reduziert werden sollte, wenn die Sedierung zunimmt.
In einer Studie zur Pharmakokinetik und Pharmakodynamik von oralem Midazolam 7,5-15 mg führte der Wechsel von der Hemmung des Metabolismus durch Itraconazol 200 mg/Tag zur Induktion durch Rifampicin 600 mg/Tag zu einer bis zu 400-fachen Änderung der AUC von oralem Midazolam.
Calciumkanalblocker
Fluconazol verstärkte die blutdrucksenkenden Effekte von Nifedipin durch Erhöhung der Plasmakonzentrationen bei einem 16-jährigen Patienten mit malignem Phäochromozytom, der wegen arterieller Hypertonie dauerhaft Nifedipin einnahm und Fluconazol zur Behandlung einer Candida-Septikämie erhielt.
Carbamazepin
Fluconazol kann vermutlich durch Hemmung von CYP3A4 eine Carbamazepin-Toxizität verursachen.
- Ein 33-jähriger Mann unter stabiler Therapie mit Carbamazepin (400 mg dreimal täglich) wegen eines Anfallsleidens wurde nach 3 Tagen mit Fluconazol 150 mg/Tag aufgrund einer Carbamazepin-Toxizität stuporös. Das Absetzen beider Medikamente führte zu einem Abfall der Carbamazepin-Konzentrationen (maximal 25 µg/ml) und zur Rückkehr zum Ausgangszustand. Carbamazepin wurde später erneut eingenommen, ohne weitere unerwünschte Ereignisse.
- Die Serumkonzentrationen von Carbamazepin stiegen unter gleichzeitiger Gabe von Fluconazol (400 mg/Tag) bei einem 38-jährigen Mann an.
Ciclosporin
Fluconazol kann die Ciclosporin-Konzentrationen durch Hemmung von CYP3A4 erhöhen. In einigen Studien wurden nur geringe oder keine Effekte festgestellt, in anderen erhöhte Fluconazol jedoch die Ciclosporin-Konzentrationen. Unterschiede in Dosis und Behandlungsdauer könnten diese Inkonsistenzen erklären. So zeigte sich bei einer Dosis von 100 mg/Tag keine Wechselwirkung, während hohe Fluconazol-Dosen (400 mg/Tag oder mehr) die Blutkonzentrationen von Ciclosporin und Tacrolimus erhöhten.
Die Wechselwirkung zwischen Ciclosporin und Fluconazol wurde retrospektiv bei 19 Nieren- und Pankreas-Nieren-Transplantatempfängern untersucht. Sowohl intravenöses als auch orales Fluconazol veränderte die Blutkonzentration von Ciclosporin. Bei fünf Probanden wurde keine signifikante Wechselwirkung festgestellt, bei 15 jedoch schon. Keiner der Patienten zeigte eine Nephrotoxizität oder Transplantatabstoßung im Zusammenhang mit der antimykotischen Therapie.
Die Wirkung höherer Fluconazol-Dosen auf die Ciclosporin-Immunsuppression wurde in einer prospektiven, offenen Crossover-Studie mit sechs Nierentransplantatpatienten untersucht. Ausgangswerte der Nierenfunktion sowie Ciclosporin-AUC, Cmax, Cmm, fmax und Clearance wurden mit den Werten an den Tagen 2, 4 und 7 nach Beginn einer oralen Fluconazol-Gabe von 200 mg/Tag verglichen. Ab Tag 8 wurde die Ciclosporin-Dosis um 50 % reduziert, und diese Parameter wurden am Tag 14 erneut bestimmt. Die Ergebnisse sind in Tabelle 1 dargestellt. In der Varianzanalyse waren nur die AUC und Cmax an Tag 4 unter Fluconazol signifikant höher als an Tag 0. Bei Clearance und fmax wurden keine signifikanten Änderungen festgestellt. Die Autoren schlossen, dass Veränderungen im Cmin möglicherweise nicht empfindlich genug sind, um die beschriebene Wechselwirkung zu erkennen, und empfahlen, die AUC etwa an Tag 4 der Behandlung zur Dosisanpassung von Ciclosporin bei gleichzeitiger Fluconazol-Gabe zu überwachen.
Cimetidin
Die Absorption von Fluconazol nach oraler Gabe wird nicht durch den Magen-pH beeinflusst, daher hat Cimetidin keinen Effekt.
Clarithromycin
Die Effekte von Fluconazol und Clarithromycin auf die Pharmakokinetik von Rifabutin und 25-O-Desacetylrifabutin wurden bei 10 HIV-infizierten Patienten untersucht, die Rifabutin 300 mg viermal täglich zusätzlich zu Fluconazol 200 mg viermal täglich und Clarithromycin 500 mg viermal täglich erhielten. Es kam zu einer 76%igen Erhöhung der AUC von Rifabutin im Plasma bei Gabe von Fluconazol oder Clarithromycin allein und zu einer 152%igen Erhöhung bei gleichzeitiger Gabe beider Medikamente. Die Autoren empfahlen, Patienten bei gleichzeitiger Gabe von Fluconazol oder Clarithromycin auf Nebenwirkungen von Rifabutin zu überwachen.
Cyclophosphamid
Cyclophosphamid ist ein Prodrug, das durch CYP450-Enzyme zu alkylierenden, zytotoxischen Spezies metabolisiert wird. Das Ausmaß des Cyclophosphamid-Metabolismus korreliert mit Wirksamkeit und Toxizität der Behandlung. In-vitro-Studien mit sechs humanen Lebermikrosomen zeigten, dass die IC50 von Fluconazol für die Reduktion der Produktion von 4-Hydroxycyclophosphamid zwischen 9-80 µmol/l lag.
Eine retrospektive Studie bei 22 krebskranken Kindern untersuchte eine mögliche Wechselwirkung zwischen Fluconazol und Cyclophosphamid. Ausgewählt wurden Kinder mit bekanntem Metabolismusprofil für Cyclophosphamid, die keine weiteren Arzneimittel erhielten, welche den Stoffwechsel beeinflussen konnten; 9 erhielten Fluconazol, 13 dienten als Kontrollgruppe. Die Plasmaclearance war bei den Patienten unter Fluconazol signifikant niedriger (2,4 vs. 4,2 l/Stunde/… ). Es ist unklar, ob diese Wechselwirkung die therapeutische Wirksamkeit von Cyclophosphamid verringert.
Doxorubicin
Die Wirkung von Fluconazol auf die Pharmakokinetik von Doxorubicin im Plasma wurde in einer randomisierten Crossover-Studie bei nichtmenschlichen Primaten untersucht. Fluconazol (10 mg/kg/Tag) wurde 4 Tage lang intravenös vor Doxorubicin (2,0 mg/kg intravenös) verabreicht. Die Vorbehandlung mit Fluconazol beeinflusste die Pharmakokinetik von Doxorubicin nicht, und die Inzidenz schwerer Neutropenie (absolute Neutrophilenzahl unter 0,5 x 109/l) war bei alleiniger Doxorubicin-Gabe höher als bei der Kombinationstherapie. Somit scheint Fluconazol nicht zu den knochenmarksuppressiven Effekten von Doxorubicin beizutragen.
Flucytosin
Die gleichzeitige Anwendung von Fluconazol und Flucytosin kann einen additiven Effekt haben. Diese Kombination könnte zur Behandlung der Kryptokokkenmeningitis hilfreich sein.
HIV-Proteaseinhibitoren
Die pharmakokinetische Wechselwirkung von Fluconazol 400 mg einmal täglich und Indinavir 1000 mg zweimal täglich wurde in einer 8-tägigen placebokontrollierten Crossover-Studie untersucht; es zeigte sich keine signifikante Wechselwirkung.
Die Wirkung von Fluconazol auf die Steady-State-Pharmakokinetik von Ritonavir und Saquinavir wurde bei HIV-1-infizierten Patienten untersucht. Sie erhielten den Proteaseinhibitor (Saquinavir 1200 mg dreimal täglich, n = 5, oder Ritonavir 600 mg zweimal täglich) am Tag 1 allein, dann zusammen mit Fluconazol 400 mg am Tag 2 und 200 mg an den Tagen 3-8. Die mittlere Erhöhung der Saquinavir-AUC betrug 50 % und die der Cmax 56 %. Fluconazol beeinflusste dagegen die Verteilung von Ritonavir nicht.
Methadon
Über eine Wechselwirkung zwischen Fluconazol und Methadon (ein Substrat von CYP3A4, CYP2C9 und CYP2C) wurde berichtet.
Ein 60-jähriger Mann mit fortgeschrittenem Krebs entwickelte zwei Tage nach intravenöser Gabe von Fluconazol wegen refraktärer oraler Candidiasis unter stabiler Methadon-Dosierung eine Atemdepression. Die Atemdepression wurde durch intravenöses Naloxon rückgängig gemacht.
In einer randomisierten, doppelblinden, placebokontrollierten Studie mit 25 Patienten erhöhte Fluconazol 200 mg/Tag die Methadon-Konzentrationen, die Patienten zeigten jedoch keine Anzeichen oder Symptome einer ausgeprägten Opioid-Überdosierung.
Omeprazol
Die Absorption von Fluconazol nach oraler Gabe wird nicht durch den Magen-pH beeinflusst, daher hat Omeprazol keinen Effekt. Omeprazol wird in der Leber weitgehend durch 5-Hydroxylierung und Sulfoxidation metabolisiert, die überwiegend von CYP2C19 bzw. CYP3A4 katalysiert werden. Fluconazol ist ein starker kompetitiver Inhibitor von CYP2C19 und ein schwacher Inhibitor von CYP3A4. Die Wirkung von Fluconazol auf die Pharmakokinetik einer einzelnen oralen Dosis Omeprazol 20 mg wurde nach einer Einzeldosis Fluconazol 100 mg und nach 4 Tagen oraler Gabe von 100 mg/Tag bei 18 gesunden männlichen Probanden untersucht. Fluconazol erhöhte Cmax und die mittlere AUC von Omeprazol und verlängerte seine Halbwertszeit (2,59 vs. 0,85 Stunden).
Orale Kontrazeptiva
Fluconazol veränderte die Pharmakokinetik von Ethinylestradiol oder Norgestrel nicht signifikant, und die Untersucher werteten dies als Hinweis darauf, dass die Behandlung mit Fluconazol bei Anwenderinnen oraler Kontrazeptiva das Schwangerschaftsrisiko nicht erhöhen würde. In der Studie wurde jedoch eine Fluconazol-Dosis von 50 mg verwendet, und Erfahrungen mit höheren Dosen zeigten andere Ergebnisse.
In einer anderen Studie verringerte Fluconazol die systemische Verfügbarkeit von Ethinylestradiol in einem oralen Kontrazeptivum; die verwendeten Dosen wurden jedoch nicht berichtet.
In einer offenen Crossover-Studie mit 10 jungen, gesunden Probanden erhöhte Fluconazol 150 mg die Serumkonzentrationen von Ethinylestradiol 30-35 µg/Tag.
Die mögliche pharmakokinetische Wechselwirkung zwischen Fluconazol 300 mg einmal wöchentlich und einem oralen Kontrazeptivum mit Ethinylestradiol und Norethindron (Ortho-Novum 7/7/7; Ortho-McNeil Pharmaceutical Inc, Raritan, NJ) wurde in einer placebokontrollierten, doppelblinden, randomisierten, zweiseitigen Crossover-Studie mit 26 gesunden Frauen im Alter von 18-36 Jahren untersucht. Im ersten Zyklus nahmen die Teilnehmerinnen nur das orale Kontrazeptivum ein. Im zweiten Zyklus wurden sie nach dem Zufallsprinzip der Gruppe "orales Kontrazeptivum + Fluconazol" oder "orales Kontrazeptivum + Placebo" zugeteilt. Im dritten Zyklus erhielten sie die jeweils andere Behandlung.
Fluconazol führte zu kleinen, aber statistisch signifikanten Anstiegen der AUC0-24 von Ethinylestradiol und Norethindron. Bei den mit Fluconazol behandelten Frauen traten keine therapiebedingten Nebenwirkungen auf.
Daher scheint durch die gleichzeitige Einnahme von Fluconazol kein erhöhtes Risiko für ein Versagen der Empfängnisverhütung zu bestehen.
Phenytoin
Die gleichzeitige Gabe von Fluconazol und Phenytoin führte zu deutlich erhöhten Phenytoin-Konzentrationen.
Rifamycine
Die Kombination von Rifampicin mit Fluconazol hatte nur geringe Auswirkungen.
Statine
Die Effekte von Fluconazol auf die Plasmakonzentrationen von Fluvastatin und Pravastatin wurden in zwei separaten, randomisierten, doppelblinden, zweiphasigen Crossover-Studien untersucht. Gesunde Probanden erhielten Fluconazol oral (400 mg an Tag 1 und 200 mg an den folgenden Tagen) oder Placebo. An Tag 4 erhielten sie zusätzlich eine einzelne orale Dosis Fluvastatin 40 mg oder Pravastatin 40 mg.
Fluconazol erhöhte die AUC der Plasmakonzentration und die Halbwertszeit von Fluvastatin um 80 %, hatte jedoch keine signifikanten Auswirkungen auf die Pharmakokinetik von Pravastatin. Der Mechanismus der verlängerten Elimination von Fluvastatin ist wahrscheinlich die Hemmung von CYP2C9. Im Gegensatz dazu scheint Pravastatin nicht anfällig für Wechselwirkungen mit Fluconazol und anderen CYP2C9-Hemmern zu sein.
Die Wirkung von Fluconazol auf die Pharmakokinetik von Rosuvastatin wurde in einer randomisierten, doppelblinden, zweiseitigen, placebokontrollierten Crossover-Studie untersucht. Gesunde männliche Probanden erhielten 11 Tage lang Fluconazol 200 mg/Tag oder Placebo; Rosuvastatin 80 mg wurde an Tag 8 gleichzeitig gegeben. Die Plasmakonzentrationen von Rosuvastatin, N-Desmethylrosuvastatin sowie der aktiven und gesamten HMG-CoA-Reduktase-Hemmer wurden bis zu 96 Stunden nach der Gabe gemessen.
Fluconazol erhöhte die AUC und Cmax von Rosuvastatin um 14 % bzw. 9 %. Begrenzte Daten für den N-Desmethyl-Metaboliten zeigten, dass die Cmax um etwa 25 % sank. Fluconazol beeinflusste den Anteil der zirkulierenden aktiven oder gesamten HMG-CoA-Reduktase-Hemmer, die auf Rosuvastatin entfallen, nicht. Insgesamt verursachte Fluconazol nur geringfügige und klinisch nicht relevante Veränderungen der Rosuvastatin-Kinetik.
Sulfonylharnstoffe
Die gleichzeitige Gabe von Fluconazol und Tolbutamid führte zu erhöhten Tolbutamid-Konzentrationen.
- Ein 56-jähriger HIV-positiver Patient mit Diabetes mellitus, der Gliclazid 160 mg/Tag einnahm, entwickelte unter Co-Trimoxazol 480 mg/Tag und Fluconazol 200 mg/Tag eine schwere Hypoglykämie. Die Autoren vermuteten, dass Fluconazol den Gliclazid-Stoffwechsel durch Hemmung von CYP2C9 beeinflusst haben könnte.
Die Effekte von Fluconazol und Fluvoxamin auf die Pharmakokinetik und Pharmakodynamik von Glimepirid wurden in einer randomisierten, doppelblinden Crossover-Studie mit 12 gesunden Probanden untersucht, die 4 Tage lang einmal täglich Fluconazol 200 mg/Tag (400 mg am ersten Tag), Fluvoxamin 100 mg/Tag oder Placebo einnahmen. An Tag 4 erhielten sie eine einzelne orale Dosis Glimepirid 0,5 mg.
Fluconazol erhöhte die mittlere Gesamt-AUC von Glimepirid auf 238 %, die maximale Plasmakonzentration auf 151 % der Kontrollwerte, und die Halbwertszeit von Glimepirid verlängerte sich von 2,0 auf 3,3 Stunden. Dies war wahrscheinlich auf die Hemmung der CYP2C9-vermittelten Biotransformation von Glimepirid durch Fluconazol zurückzuführen. Allerdings verursachte Fluconazol keine statistisch signifikanten Veränderungen der Wirkung von Glimepirid auf den Blutzucker.
Tacrolimus
Da Tacrolimus im Darm und in der Leber über CYP3A4 verstoffwechselt wird, können CYP3A4-Hemmer den Abbau von Tacrolimus verringern und die Tacrolimus-Blutkonzentrationen erhöhen.
Die Wirkung von Fluconazol auf die Tacrolimus-Blutkonzentrationen wurde bei acht Lebertransplantationspatienten untersucht, bei denen die prophylaktische Fluconazol-Therapie (200 mg/Tag) wegen erhöhter Lebertransaminasen, Nierenfunktionsstörung oder Eosinophilie (jeweils n = 1) abgesetzt wurde. Die berechneten Tacrolimus-Konzentrationen sanken zwischen dem 4. und 9. Tag nach dem Absetzen von Fluconazol um 13-81 % (Median 41 %). Die Tacrolimus-Blutkonzentrationen sollten sorgfältig überwacht werden; beim Absetzen von Fluconazol kann gegebenenfalls eine Dosiserhöhung erforderlich sein.
Die Wechselwirkung von Tacrolimus mit Fluconazol wurde retrospektiv bei 19 Nieren- und Pankreas/Nieren-Transplantatempfängern untersucht. Sowohl intravenöses als auch orales Fluconazol beeinflusste die Tacrolimus-Blutkonzentration. Fünf Patienten zeigten keine signifikante Wechselwirkung, 15 dagegen schon. Bei keinem Patienten traten Nephrotoxizität oder Transplantatabstoßung im Zusammenhang mit der antimykotischen Therapie auf.
- Ein 17-jähriger Mann mit Mukoviszidose, der nach einer Lungen-Leber-Transplantation Itraconazol einnahm, zeigte trotz vergleichsweise niedriger Dosierung (0,1-0,3 mg/kg/Tag) hohe Tacrolimus-Spiegel.
- Ein Patient, der Tacrolimus 0,085 mg/kg zweimal täglich zusammen mit Itraconazol 200-400 mg/Tag einnahm, entwickelte Ketoazidose, Neutropenie und Thrombozytopenie, was zum Absetzen beider Medikamente führte.
- Ein 34-jähriger Nierentransplantatempfänger, der ein stabiles Behandlungsschema mit Tacrolimus und Methylprednisolon erhielt, wurde wegen einer Hefeinfektion der Harnwege mit Itraconazol 100 mg zweimal täglich behandelt. Die gleichzeitige Therapie mit Itraconazol führte am zweiten Tag zu einem starken Anstieg der Tacrolimus-Talspiegel (von 13 auf 21 µg/ml) und zu erhöhten Serumkreatininwerten, was eine Dosisreduktion von Tacrolimus um 50 % erforderlich machte.
Nach dem Absetzen von Itraconazol dauerte es 12 Tage, bis seine Wirkung auf den Tacrolimus-Stoffwechsel wieder nachließ. Die hemmende Wirkung von Itraconazol setzte schnell ein, verschwand aber deutlich langsamer, was für die klinische Behandlung wichtig ist. Deshalb ist bei gleichzeitiger Gabe von Itraconazol und Tacrolimus eine engmaschige Überwachung der Tacrolimus-Blutkonzentrationen und eine sorgfältige Dosisanpassung nötig, um Toxizität zu vermeiden.
Warfarin
Die gleichzeitige Gabe von Fluconazol und Warfarin führte in einigen Fällen zu einer Verlängerung der Prothrombinzeit.
Zidovudin
Die Kombination von Fluconazol mit Valproinsäure hemmte in humanen Lebermikrosomen in vitro die Glucuronidierung von Zidovudin stärker als andere Medikamente wie Atovaquon und Methadon.
Nebenwirkungen
Lesen Sie die Anwendungsgebiete, wenn Sie Fluconazol online bestellen möchten.
Zu den am häufigsten beschriebenen Nebenwirkungen von Fluconazol gehören Magen-Darm-Beschwerden wie Bauchschmerzen, Durchfall, Blähungen, Übelkeit und Erbrechen sowie Geschmacksstörungen. Weitere Nebenwirkungen sind Kopfschmerzen, Schwindel, Leukozytopenie, Thrombozytopenie, Hyperlipidämie und erhöhte Leberenzymwerte. Schwere Hepatotoxizität wurde bei Patienten mit schweren Grunderkrankungen wie AIDS oder malignen Erkrankungen berichtet. Anaphylaxie und Angioödeme wurden selten gemeldet. Hautreaktionen sind selten, allerdings traten exfoliative Hautreaktionen wie toxische epidermale Nekrolyse und das Stevens-Johnson-Syndrom häufiger bei Patienten mit AIDS auf.
Alopezie
Alopezie wurde gelegentlich beschrieben, insbesondere bei Patienten unter längerer Behandlung mit Fluconazol.
Einfluss auf das Elektrolytgleichgewicht
Hypokaliämie wurde bei 3 Patienten mit akuter myeloischer Leukämie im Zusammenhang mit Fluconazol beobachtet.
Wirkung auf das Herz
Ein verlängertes QT-Intervall und Torsade de Pointes wurden unter Fluconazol selten berichtet.
Wirkung auf die Leber
Obwohl schwere Leberreaktionen unter Fluconazol selten sind, wurden sie vor allem bei Patienten mit schweren Grunderkrankungen oder eingeschränkter Leberfunktion beobachtet. Erhöhte Leberenzymwerte sind häufig, außerdem wurden Fälle von Ikterus berichtet. Lebernekrosen wurden selten post mortem bei Patienten mit schweren Grunderkrankungen dokumentiert, die Fluconazol erhalten hatten. Bei einem dieser Patienten wurde die Hepatotoxizität als dosisabhängig eingeschätzt.

Überempfindlichkeit
Eine Desensibilisierung wurde bei einem AIDS-Patienten erfolgreich durchgeführt, der eine Überempfindlichkeit gegen Fluconazol und Itraconazol zeigte. Über sieben Tage wurden schrittweise steigende orale Dosen von Fluconazol verabreicht, beginnend mit 5 mg/Tag; anschließend wurde die Behandlung mit 400 mg täglich fortgesetzt. Während der Desensibilisierung oder in den drei Monaten vor Veröffentlichung des Berichts traten keine Nebenwirkungen auf.
Vorsichtsmaßnahmen
Lesen Sie vor dem Online-Kauf von Fluconazol die Informationen zum Arzneimittel.
Fluconazol sollte bei Patienten mit eingeschränkter Leber- oder Nierenfunktion mit Vorsicht angewendet werden. Auffälligkeiten in hämatologischen, hepatischen und renalen Laborwerten wurden bei Patienten mit schweren Grunderkrankungen wie AIDS oder malignen Erkrankungen beobachtet. Fälle von Torsade de Pointes und QT-Verlängerung wurden selten berichtet; deshalb ist bei Patienten mit proarrhythmischen Risikofaktoren Vorsicht geboten. Bei Tieren wurde nach hohen Fluconazol-Dosen Teratogenität festgestellt, weshalb die Anwendung in der Schwangerschaft nicht empfohlen wird.
Stillzeit
Fluconazol geht in die Muttermilch über und erreicht Konzentrationen, die denen im mütterlichen Plasma ähneln. Dennoch wird die Anwendung in der zugelassenen Fachinformation in der Stillzeit nicht empfohlen. In einem Bericht wurden bei einem Säugling, der sechs Wochen lang über die Muttermilch Fluconazol ausgesetzt war, außer einer leichten Erhöhung des Lactatdehydrogenase-Spiegels keine unerwünschten Wirkungen beobachtet. In Deutschland werden Fluconazol-Tabletten von Fachkreisen in der Regel als mit dem Stillen vereinbar angesehen, wenn sie klinisch erforderlich sind.
Schwangerschaft
Hohe (toxische) Dosen von Fluconazol, Itraconazol und Ketoconazol zeigten bei Nagetieren teratogene Wirkungen.
Obwohl es nur wenige Daten zur Anwendung dieser Medikamente in der Schwangerschaft beim Menschen gibt, wurde ein Fall beschrieben, in dem eine Frau während der gesamten Schwangerschaft Fluconazol 400 mg täglich einnahm und ein Kind mit schweren kraniofazialen und Extremitätenanomalien zur Welt brachte. Diese Anomalien ähnelten dem Antley-Bixler-Syndrom, einer genetischen Erkrankung; eine teratogene Wirkung konnte jedoch nicht ausgeschlossen werden.
Studien mit verschreibungspflichtiger Ereignisüberwachung zeigten keine negativen Wirkungen von Fluconazol auf den Fötus. Allerdings wurden angeborene Fehlbildungen bei Kindern beobachtet, deren Mütter über 3 Monate oder länger hohe Fluconazol-Dosen erhielten. Daten des Herstellers von 198 Frauen, die im 1. Trimenon Itraconazol ausgesetzt waren, zeigten eine Fehlbildungsrate im Bereich des erwarteten Grundrisikos der Allgemeinbevölkerung.
Dennoch empfehlen die Hersteller, Fluconazol, Itraconazol und Ketoconazol in der Schwangerschaft zu vermeiden. Gemäß zugelassener Fachinformation sind insbesondere Dosen von Voriconazol in therapeutischer Äquivalenz bei Nagetieren teratogen und embryotoxisch. Daher wird empfohlen, Voriconazol während der Schwangerschaft zu vermeiden und bei Frauen im gebärfähigen Alter während der Behandlung eine wirksame Empfängnisverhütung anzuwenden.
Ähnliche Empfehlungen gelten für Posaconazol. Andere Azol-Antimykotika, darunter Butoconazol, Clotrimazol, Econazol, Miconazol, Sulconazol, Terconazol und Tioconazol, werden bei Nagetieren nach hochdosierter Gabe als embryotoxisch, aber nicht teratogen beschrieben. Viele dieser Medikamente werden topisch oder intravaginal angewendet, wobei die systemische Aufnahme unterschiedlich ist. Auch wenn diese Medikamente in der Schwangerschaft nicht grundsätzlich kontraindiziert sind, sollten diese potenziellen Risiken bei der Wahl einer antimykotischen Therapie berücksichtigt werden.














