Dapsone (Dapson)

Dosierungen
Dapsone 100 mg
| Menge | Preis pro Tablette | Gesamtpreis | |
|---|---|---|---|
| 1000 | €0,07 | €68,05 | |
| 2000 | €0,06 | €119,08 | |
| 3000 | €0,05 | €153,11 |
Zahlung & Versand
Ihre Bestellung wird sorgfältig verpackt und innerhalb von 24 Stunden versendet. So sieht ein typisches Paket aus.
Die Sendung hat die Größe eines normalen privaten Briefes (24x11x0,7 cm), ohne Hinweis auf den Inhalt.



| Versandmethode | Voraussichtliche Lieferung |
|---|---|
| Express Kostenlos für Bestellungen über €300,00 | Voraussichtliche Lieferung nach Deutschland: 4-7 Tage |
| Standard Kostenlos für Bestellungen über €200,00 | Voraussichtliche Lieferung nach Deutschland: 14-21 Tage |











Rabattcoupons
- Neujahrstag - 1. Januar 2026 9% NEUJAHR9
- Heilige Drei Könige - 6. Januar 2026 5% DREIKOENIGE5
- Tag der Arbeit - 1. Mai 2026 6% ARBEIT6
- Tag der Deutschen Einheit - 3. Oktober 2026 8% EINHEIT8
- Allerheiligen - 1. November 2026 6% ALLERHEILIGEN6
- Heiligabend - 24. Dezember 2026 9% HEILIGABEND9
- Weihnachten - 25. Dezember 2026 10% WEIHNACHTEN10
- Zweiter Weihnachtstag - 26. Dezember 2026 9% ZWEITER9
- Silvester - 31. Dezember 2026 8% SILVESTER8
Markennamen
| Land | Markennamen |
|---|---|
 Spanien Spanien | Dapsone Fatol |
Beschreibung
Dapson, ein synthetisches Sulfon, ist ein antimykobakterieller und antiprotozoaler Wirkstoff. Es ist auch als 4,4'-Sulfonyldianilin bekannt, ein Antibiotikum, das hauptsächlich zur Behandlung von Lepra (Hansen-Krankheit) und Dermatitis herpetiformis eingesetzt wird, einer Hauterkrankung, die durch Blasenbildung und Juckreiz gekennzeichnet ist. Es handelt sich um ein weißes bis cremeweißes, kristallines Pulver mit leicht bitterem Geschmack. Der Wirkstoff ist in Wasser nur sehr schwer löslich und in Alkohol gut löslich.
Wirkmechanismus
Dapson wirkt in der Regel bakteriostatisch. Der Wirkmechanismus ist nicht vollständig aufgeklärt. Da die antibakterielle Aktivität des Wirkstoffs durch p-Aminobenzoesäure (PABA) gehemmt wird, hat das Arzneimittel wahrscheinlich einen ähnlichen Wirkmechanismus wie Sulfonamide, der die Hemmung der Folsäuresynthese in empfindlichen Organismen umfasst. Einige Studien weisen darauf hin, dass Dapson den alternativen Weg der Komplementaktivierung hemmen und das durch Myeloperoxidase-Wasserstoffperoxid (H2O2)-Halid vermittelte zytotoxische System in Neutrophilen beeinträchtigen kann. In-vitro-Studien zeigen, dass dieses Arzneimittel die Motilität von Neutrophilen stimuliert.
Der Wirkstoff scheint außerdem die spontane und induzierte Synthese von Prostaglandin E2 durch polymorphkernige Leukozyten, die von gesunden Personen oder Patienten mit Lepra gewonnen wurden, zu hemmen. Der Wirkmechanismus bei der Behandlung der Dermatitis herpetiformis ist unbekannt; das Arzneimittel unterdrückt jedoch lediglich die Erkrankung, und die kutane Ablagerung von Immunglobulin A (IgA) und Komplement wird durch das Arzneimittel nicht beeinflusst. Es wurde vorgeschlagen, dass der Wirkstoff als Immunmodulator wirken kann, wenn er zur Behandlung der Dermatitis herpetiformis und anderer dermatologischer Erkrankungen eingesetzt wird.
Pharmakokinetik
Dapson wird nach oraler Gabe nahezu vollständig resorbiert, wobei die maximalen Serumkonzentrationen innerhalb von 2-8 Stunden erreicht werden. Steady-State-Spiegel liegen nach 8 Tagen bei einer täglichen Dosis von 200 mg im Mittel bei 2.3 mcg/mL. Nach einer Einzeldosis von 100 mg liegen die Serumspiegel nach 24 Stunden zwischen 0.4-1.2 mcg/mL, wobei Spurenmengen bis zu 35 Tage nach Absetzen nachweisbar sein können.
Das Verteilungsvolumen beträgt 1.5-2.5 L/kg, und Dapson wird bis zu 3 Wochen nach Therapieende in Haut, Muskulatur, Nieren und Leber gespeichert. Es passiert die Plazenta und geht in die Muttermilch über; berichtet wurden Konzentrationen von 1.1 mcg/mL in der Milch und 1.6 mcg/mL im mütterlichen Serum.
Die Plasmahalbwertszeit ist variabel (10-83 Stunden) und beträgt im Durchschnitt 20-30 Stunden. Der Wirkstoff wird in der Leber überwiegend zu Monoacetyldapson (MADDS) metabolisiert, was Methämoglobinämie und Hämolyse verursachen kann. Etwa 20% des Wirkstoffs werden unverändert im Urin ausgeschieden, während 70-85% als Metaboliten ausgeschieden werden. Aktivkohle und Hämodialyse können die Elimination des Wirkstoffs und seiner Metaboliten verbessern.
Dapson: Anwendungsgebiete
Das Arzneimittel wirkt als antibakterieller Wirkstoff, indem es – ähnlich wie Sulfonamide – die Synthese von Dihydrofolsäure in Bakterien hemmt. Es ist auch für seine entzündungshemmenden Eigenschaften bekannt, die helfen, Gewebeschäden während entzündlicher Reaktionen zu verringern. Dapson kann oral oder topisch angewendet werden und wird häufig zusammen mit anderen Arzneimitteln verordnet, um die Wirksamkeit zu erhöhen.
Lepra
Das Arzneimittel wird in Rifampicin-basierten Mehrfachtherapien zur Behandlung der multibazillären und paucibazillären Lepra eingesetzt. Obwohl das Arzneimittel in der Vergangenheit allein zur Behandlung der Lepra verwendet wurde, empfehlen die Weltgesundheitsorganisation (WHO) und die meisten Kliniker derzeit, Rifampicin-basierte Mehrfachtherapien zur Behandlung aller Lepraformen einzusetzen.

Mehrfachtherapien können die Infektiosität des Patienten schneller reduzieren sowie die Entstehung resistenter Organismen verzögern oder verhindern. Da Rifampicin gegenüber Mycobacterium leprae (M. leprae) bakterizid wirkt, ist die einmal monatliche Gabe von Rifampicin der Hauptbestandteil der derzeit empfohlenen Mehrfachtherapien; Dapson und Clofazimin werden den Regimen hinzugefügt, um die Entstehung Rifampicin-resistenter M. leprae zu verhindern.

Dermatitis Herpetiformis
Dapson ist das Arzneimittel der Wahl zur Behandlung der Dermatitis herpetiformis. Die meisten Kliniker empfehlen, Sulfapyridin zur Behandlung der Dermatitis herpetiformis nur dann einzusetzen, wenn Dapson nicht verwendet werden kann. Bei ansprechenden Patienten führt der Therapiebeginn in der Regel zu einer raschen Abnahme des Pruritus und zur Kontrolle der Hautläsionen der Dermatitis herpetiformis; dieses Arzneimittel hat jedoch keinen Einfluss auf die kutane Ablagerung von IgA und Komplement.

Das Absetzen der Dapson-Therapie führt im Allgemeinen zu einer raschen Verschlechterung der Läsionen und zu starkem Pruritus. Eine glutenfreie Ernährung in Kombination mit dem Arzneimittel verbessert die klinischen Symptome. Sie senkt bei etwa 60% der Patienten den Erhaltungsdosisbedarf.
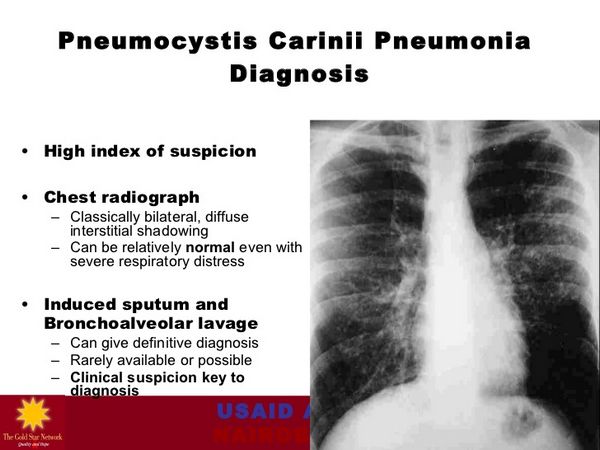
Pneumocystis jiroveci (Pneumocystis carinii) Pneumonie
Dapson wird in Kombination mit Trimethoprim zur Behandlung initialer Episoden einer Pneumocystis jiroveci- (früher Pneumocystis carinii-) Pneumonie (PCP) bei Erwachsenen mit erworbenem Immundefektsyndrom (AIDS) eingesetzt; es ist von der United States (US) Food and Drug Administration (FDA) als Orphan Drug für diese Indikation ausgewiesen. Ein Kombinationsschema aus dem Arzneimittel (100 mg einmal täglich) und Trimethoprim (20 mg/kg täglich in 4 Einzeldosen) über 21 Tage ist wirksam zur Behandlung initialer PCP-Episoden bei Patienten mit AIDS und erzielte in einer Studie bei Patienten mit milden bis mäßig schweren initialen Episoden der Erkrankung eine klinische Ansprechrate von 93%.
Die meisten Patienten zeigen innerhalb von 6 Tagen eine klinische Besserung, und die Kombination der Arzneimittel scheint im Allgemeinen gut verträglich zu sein. Eine Therapie mit diesem Arzneimittel und Trimethoprim scheint ebenso wirksam zu sein wie orales Co-Trimoxazol zur Behandlung initialer Episoden einer milden bis mäßig schweren PCP. Sie wird jedoch bei AIDS-Patienten besser vertragen als Co-Trimoxazol.
Prävention von PCP
Das Arzneimittel wird allein oder in Kombination mit Pyrimethamin zur Prävention von PCP bei HIV-infizierten Personen eingesetzt; Dapson ist von der FDA als Orphan Drug für diese Indikation ausgewiesen. Obwohl Co-Trimoxazol im Allgemeinen das Arzneimittel der Wahl sowohl für die primäre als auch für die sekundäre Prophylaxe der PCP bei HIV-infizierten Personen ist, empfehlen die Prevention of Opportunistic Infections Working Group des US Public Health Service und die Infectious Diseases Society of America (USPHS/IDSA) sowie andere Kliniker dieses Arzneimittel oder Dapson und Pyrimethamin (mit Leucovorin) als Alternativen.

Das Arzneimittel allein wird als Alternative zu Co-Trimoxazol für die PCP-Prophylaxe bei schwangeren Frauen empfohlen.
Die USPHS/IDSA empfiehlt derzeit, dass Kinder, die von HIV-infizierten Müttern geboren werden, ab einem Alter von 4-6 Wochen eine primäre Prophylaxe gegen PCP erhalten; die Prophylaxe kann bei Kindern, bei denen später festgestellt wird, dass sie nicht mit HIV infiziert sind, abgesetzt werden, aber bei Kindern, deren HIV-Status weiterhin unbekannt ist, sollte die primäre PCP-Prävention im ersten Lebensjahr fortgeführt werden.
Prävention von PCP-Rezidiven
Die USPHS/IDSA empfiehlt derzeit, dass HIV-infizierte Personen mit einer PCP-Anamnese eine langfristige suppressive bzw. chronische Erhaltungstherapie (sekundäre Prävention) erhalten, um ein Rezidiv zu verhindern.
Für die sekundäre Prävention werden die gleichen Schemata wie für die primäre PCP-Prophylaxe verwendet. Die sekundäre Prävention wird in der Regel lebenslang durchgeführt, es sei denn, es kommt durch potente antiretrovirale Therapie zu einer Immunrekonstitution. Aktuelle Evidenz zeigt, dass die sekundäre Prophylaxe gegen PCP bei HIV-infizierten Erwachsenen und Jugendlichen, die auf eine potente antiretrovirale Therapie ansprechen und bei denen ein anhaltender (3 Monate oder länger) Anstieg der CD4+-T-Zell-Zahlen (cluster of differentiation 4-positive) von weniger als 200/mm3 auf mehr als 200/mm3 erreicht wurde, abgesetzt werden kann.
Die USPHS/IDSA gibt an, dass Kinder mit einer PCP-Anamnese eine lebenslange suppressive Therapie erhalten sollten, um Rezidive zu verhindern. Die Sicherheit des Absetzens der sekundären PCP-Prophylaxe bei HIV-infizierten Kindern wurde nicht umfassend untersucht.
Toxoplasmose-Prävention
Obwohl Dapson nicht zur Behandlung der Toxoplasmose eingesetzt wird, wird ein 2-Arzneimittel-Schema aus diesem Arzneimittel und Pyrimethamin als Alternative zu Co-Trimoxazol zur primären oder sekundären Prävention einer Toxoplasma gondii (T. gondii)-Enzephalitis empfohlen, und das Arzneimittel allein wird als Alternative zu Co-Trimoxazol für die sekundäre Toxoplasmose-Prophylaxe empfohlen.
Die USPHS/IDSA empfiehlt derzeit eine primäre Prophylaxe gegen eine T. gondii-Enzephalitis für alle HIV-infizierten Erwachsenen und Jugendlichen, die seropositiv für Toxoplasma-IgG-Antikörper (Immunglobulin G) sind und CD4+-T-Zell-Zahlen unter 100/mm3 aufweisen. HIV-infizierte Säuglinge und Kinder mit schwerer Immunsuppression, die seropositiv für Toxoplasma-IgG-Antikörper sind, sollten ebenfalls eine primäre Prophylaxe gegen eine T. gondii-Enzephalitis erhalten. Die USPHS/IDSA empfiehlt Co-Trimoxazol als Arzneimittel der Wahl für die primäre Prophylaxe gegen Toxoplasmose bei HIV-infizierten Erwachsenen, Jugendlichen und Kindern.
Ein Schema aus Dapson und Pyrimethamin (mit Leucovorin) ist die empfohlene Alternative für die primäre Prophylaxe gegen Toxoplasmose bei Patienten, die Co-Trimoxazol nicht vertragen.
Toxoplasmose
Aktuelle Evidenz zeigt, dass die primäre Toxoplasmose-Prophylaxe bei HIV-infizierten Erwachsenen und Jugendlichen, die auf eine potente antiretrovirale Therapie ansprechen und bei denen ein anhaltender (3 Monate oder länger) Anstieg der CD4+-T-Zell-Zahlen von weniger als 200/mm3 auf mehr als 200/mm3 erreicht wurde, mit einem minimalen Risiko für die Entwicklung einer toxoplasmatischen Enzephalitis abgesetzt werden kann.
Die USPHS/IDSA gibt an, dass das Absetzen der primären Toxoplasmose-Prophylaxe bei HIV-infizierten Erwachsenen und Jugendlichen empfohlen wird, die einen anhaltenden (3 Monate oder länger) Anstieg der CD4+-T-Zell-Zahlen auf mehr als 200/mm3 aufweisen, da die Prophylaxe in Bezug auf die Krankheitsprävention bei Toxoplasmose offenbar nur einen geringen Zusatznutzen bietet. Das Absetzen reduziert die Arzneimittelbelastung, das Potenzial für Toxizität, Arzneimittelinteraktionen, die Selektion arzneimittelresistenter Pathogene und die Kosten. Wenn die primäre Toxoplasmose-Prophylaxe bei Erwachsenen und Jugendlichen, die die empfohlenen Kriterien erfüllen, abgesetzt wird, sollte sie nach Angaben der USPHS/IDSA wieder begonnen werden, wenn die CD4+-T-Zell-Zahl auf weniger als 100-200/mm3 sinkt.
Die Sicherheit des Absetzens der primären Prophylaxe bei HIV-infizierten Kindern, die eine potente antiretrovirale Therapie erhalten, wurde nicht umfassend untersucht.
Dieses Arzneimittel wird nicht zur sekundären Toxoplasmose-Prophylaxe empfohlen.
Weitere Anwendungen
Dapson hat bullöse Eruptionen oder mukokutane Läsionen bei Patienten mit systemischem Lupus erythematodes und discoidem Lupus erythematodes wirksam behandelt, die gegenüber konventioneller antimalarischer oder kortikosteroider Therapie resistent waren.
Das Arzneimittel wurde zudem erfolgreich zur Behandlung anderer Erkrankungen eingesetzt, die durch bullöse Eruptionen gekennzeichnet sind, wie bullöses Pemphigoid, Pemphigus vulgaris und Hailey-Hailey-Erkrankung.
Der Wirkstoff wurde bei einer begrenzten Anzahl von Patienten zur Behandlung verschiedener entzündlicher Dermatosen eingesetzt (zum Beispiel (e.g.), Pyoderma gangraenosum, Erythema elevatum diutinum, Weber-Christian-Krankheit, Sweet-Syndrom, Polyarteriitis nodosa, Granuloma faciale) sowie pustulöser Dermatosen (e.g., Herpes gestationis, Impetigo herpetiformis, pustulöse Psoriasis, follikuläre Mukinose). Dapson wurde mit einigem Erfolg auch zur Behandlung der rheumatoiden Arthritis, rezidivierenden Polychondritis und allergischen Vaskulitis eingesetzt.
Anwendung und Dosierung
Das Arzneimittel wird oral verabreicht. Für die Verabreichung bei Kindern wurden handelsübliche Dapson-Tabletten zerstoßen und in Erdbeersirup gelöst; Studien zur Bioverfügbarkeit des Arzneimittels nach Anwendung dieser Zubereitung wurden jedoch bis heute nicht veröffentlicht.
|
Erkrankung |
Altersgruppe |
Dapson-Dosierung |
Zusätzliche Medikamente |
Dauer |
|
Multibazilläre Lepra |
Erwachsene |
100 mg täglich |
Rifampin (600 mg einmal monatlich), Clofazimine (50 mg täglich, 300 mg einmal monatlich) |
12 Monate |
|
Kinder (10-14 Jahre) |
50 mg täglich |
Rifampin (450 mg einmal monatlich), Clofazimine (50 mg jeden zweiten Tag, 150 mg einmal monatlich) |
12 Monate |
|
|
Kinder (<10 Jahre) |
25 mg täglich (an das Gewicht angepasst) |
Rifampin (300 mg einmal monatlich), Clofazimine (50 mg zweimal wöchentlich, 100 mg einmal monatlich) |
12 Monate |
|
|
Hinweis: Für einige Dosen wird eine überwachte Verabreichung empfohlen |
||||
|
Zusätzliche Therapie bei Patienten mit hohem bakteriologischem Index ohne Besserung nach der initialen Behandlung |
Zusätzliche 12 Monate bei Bedarf |
|||
|
Paucibazilläre Lepra |
Erwachsene |
100 mg täglich |
Rifampin (600 mg einmal monatlich) |
6 Monate |
|
Kinder (10-14 Jahre) |
50 mg täglich |
Rifampin (450 mg einmal monatlich) |
6 Monate |
|
|
Kinder (<10 Jahre) |
25 mg täglich (an das Gewicht angepasst) |
Rifampin (300 mg einmal monatlich) |
6 Monate |
|
|
Dapson kann bei schweren Nebenwirkungen abgesetzt werden; Clofazimin kann ersetzt werden |
||||
|
Dermatitis Herpetiformis |
Erwachsene |
Beginn mit 50 mg täglich; ggf. Steigerung auf 300 mg täglich. Die Erhaltungsdosis liegt in der Regel zwischen 25-400 mg täglich. |
Langfristig |
|
|
Kinder |
Dosis an das Gewicht angepasst; typischerweise niedriger als bei Erwachsenen |
Langfristig |
||
|
Pneumocystis jiroveci Pneumonie – Behandlung |
Erwachsene |
100 mg einmal täglich |
Trimethoprim (5 mg/kg dreimal täglich) |
21 Tage |
|
Pneumocystis jiroveci Pneumonie – Prävention |
Erwachsene |
50 mg zweimal täglich oder 100 mg einmal täglich |
Kann auch mit Pyrimethamin und Leucovorin in verschiedenen Schemata gegeben werden |
Langfristig |
|
Kinder (>1 Monat) |
2 mg/kg (max. 100 mg) einmal täglich oder 4 mg/kg (max. 200 mg) einmal wöchentlich |
Langfristig |
||
|
Toxoplasmose-Prävention |
Erwachsene |
50 mg einmal täglich oder 200 mg einmal wöchentlich |
Pyrimethamine (50/75 mg wöchentlich), orales leucovorin (25 mg wöchentlich) |
Langfristig |
|
Kinder (>1 Monat) |
2 mg/kg oder 15 mg/m² (max. 25 mg) einmal täglich |
Pyrimethamine (1 mg/kg einmal täglich), orales leucovorin (5 mg alle drei Tage) |
Langfristig |
Das Arzneimittel kann bei schweren Nebenwirkungen abgesetzt werden; in einigen Fällen kann Clofazimin ersetzt werden.
Nebenwirkungen
Dieses Arzneimittel ist mit einer Reihe von Nebenwirkungen verbunden, von denen einige schwerwiegend sein können. Häufige Nebenwirkungen umfassen gastrointestinale Beschwerden wie Übelkeit und Bauchschmerzen sowie hämatologische Probleme wie hämolytische Anämie und Agranulozytose, insbesondere bei Personen mit Glucose-6-Phosphat-Dehydrogenase-(G-6-PD)-Mangel. Darüber hinaus wurden neurologische Effekte wie periphere Neuropathie und Stimmungsschwankungen berichtet, was eine sorgfältige Überwachung während der Behandlung erforderlich macht.
Hämatologische Effekte
Die häufigsten Nebenwirkungen von Dapson sind dosisabhängige hämolytische Anämie und Methämoglobinämie. Hämolyse tritt bei den meisten Patienten auf, die 200 mg oder mehr dieses Arzneimittels täglich erhalten; eine symptomatische Anämie tritt jedoch nur gelegentlich auf. Der Hersteller gibt an, dass der Hämoglobinspiegel im Allgemeinen um 1-2 g/dL abnimmt, die Retikulozytenzahl um 2-12% ansteigt, die Lebensdauer der Erythrozyten verkürzt ist und bei den meisten Patienten, die dieses Arzneimittel erhalten, eine Methämoglobinämie auftritt. Eine Heinz-Körperchen-Bildung tritt ebenfalls häufig auf. Sofern nicht schwerwiegend, erfordert Hämolyse oder Methämoglobinämie im Allgemeinen kein Absetzen der Therapie.
Im Allgemeinen wird Dapson bei AIDS-Patienten gut vertragen. Allerdings wurde bei zwei Dritteln solcher Patienten, die 100 mg des Arzneimittels täglich gleichzeitig mit Trimethoprim 20 mg/kg täglich erhielten, eine asymptomatische Methämoglobinämie berichtet.
Die prophylaktische Gabe von Ascorbinsäure, Folat und Eisen kann Berichten zufolge einige der unerwünschten hämatologischen Effekte des Arzneimittels verhindern. Leukopenie wurde gelegentlich während der Therapie berichtet, und potenziell tödliche Agranulozytose und aplastische Anämie wurden selten berichtet.
Lepra-Reaktionszustände
Eine wirksame Therapie der Lepra mit diesem Arzneimittel oder anderen Wirkstoffen führt häufig zu ausgeprägten klinischen Veränderungen, die als Lepra-Reaktionszustände bezeichnet werden und in zwei Typen eingeteilt werden: Umkehrreaktionen (Typ 1) und Erythema nodosum leprosum-(ENL)-Reaktionen (Typ 2). Umkehrreaktionen betreffen vor allem Patienten mit grenzwertiger oder tuberkuloider Lepra und resultieren aus einer verstärkten Überempfindlichkeitsreaktion, die Schwellung, Erythem, Fieber und potenzielle Nervenschädigungen verursacht. ENL, das hauptsächlich bei multibazillären Lepra-Patienten auftritt, ist bei den aktuellen Mehrfachtherapien mit Clofazimin weniger häufig als bei einer Dapson-Monotherapie.
Die Behandlung hängt vom Schweregrad ab; schwere Fälle können eine Hospitalisierung erfordern. Standardmäßige Antilepra-Schemata werden in der Regel fortgeführt, wobei Kortikosteroide bei Nervenverletzungen oder Ulzerationen eingesetzt werden. ENL wird mit Analgetika, Kortikosteroiden, Thalidomid und Clofazimin behandelt. Eine frühe Diagnose und Behandlung sind entscheidend, um die Morbidität im Zusammenhang mit diesen Reaktionen zu reduzieren, und die Therapie sollte unter Einbeziehung eines Experten für Lepra-Behandlung erfolgen.
Dermatologische Reaktionen
Unerwünschte kutane Effekte, die in der Regel durch Sensibilisierung gegenüber Dapson entstehen, treten während der Therapie selten auf. Kutane Reaktionen umfassen exfoliative Dermatitis, toxisches Erythem, Erythema multiforme, epidermale Nekrolyse, morbilliforme und skarlatiniforme Exantheme, Urtikaria und Erythema nodosum. Wenn während der Therapie eine neue oder toxische dermatologische Reaktion auftritt, sollte das Arzneimittel abgesetzt und eine geeignete Therapie eingeleitet werden. Berichten zufolge tritt ein Hautausschlag bei etwa 30-40% der AIDS-Patienten auf, die dieses Arzneimittel gleichzeitig mit Trimethoprim erhalten, jedoch seltener bei Patienten, die das Arzneimittel allein erhalten; trotz eines solchen Ausschlags kann ein erheblicher Anteil der Patienten, die Co-Trimoxazol nicht vertragen, das Arzneimittel vertragen.
Effekte auf das Nervensystem
Periphere Neuropathie mit motorischem Ausfall wurde selten bei Patienten berichtet, die hohe Dosen von Dapson (200-500 mg täglich) erhielten. Wenn während der Therapie Muskelschwäche auftritt, sollte das Arzneimittel abgesetzt werden; eine vollständige Erholung kann nach Absetzen eintreten, kann jedoch viele Monate bis mehrere Jahre dauern. Der Mechanismus der Erholung beruht Berichten zufolge auf axonaler Regeneration, und einige Patienten mit Erholung haben eine erneute Behandlung mit dem Arzneimittel in einer niedrigeren Dosierung vertragen.
Obwohl periphere Neuropathie bis heute bei Patienten mit Lepra, die dieses Arzneimittel erhalten, nicht berichtet wurde, vermutlich weil eine niedrigere Dosierung verwendet wird, kann diese Nebenwirkung schwer von einem Lepra-Reaktionszustand zu unterscheiden sein. Schlaflosigkeit, Kopfschmerzen, Nervosität, Schwindel und Psychosen wurden ebenfalls mit diesem Arzneimittel berichtet.
Gastrointestinale (GI) Effekte
Unerwünschte GI-Effekte, einschließlich Anorexie, Bauchschmerzen, Übelkeit und Erbrechen, sind bei Patienten aufgetreten, die Dapson erhielten.
Hepatische Effekte
Toxische Hepatitis und cholestatischer Ikterus wurden mit diesem Arzneimittel berichtet. Cholestatischer Ikterus kann eine Überempfindlichkeitsreaktion sein und scheint im Allgemeinen nach Absetzen des Arzneimittels reversibel zu sein. Unerwünschte hepatische Effekte traten kurz nach Beginn der Therapie auf. Sie können sich durch erhöhte Serumkonzentrationen von alkalischer Phosphatase, Aspartat-Aminotransferase (AST) (Serum-Glutamat-Oxalacetat-Transaminase (SGOT)), Bilirubin und Laktatdehydrogenase (LDH) manifestieren. Abweichungen der Leberfunktionstests treten Berichten zufolge häufiger während einer kombinierten Dapson- und Trimethoprim-Therapie auf als während einer Therapie mit dem Arzneimittel allein. Hyperbilirubinämie trat ebenfalls während der Therapie auf und kann bei Patienten mit G-6-PD-Mangel häufiger auftreten.
Renale und Elektrolyt-Effekte
Albuminurie, nephrotisches Syndrom und renale Papillennekrose traten selten während der Therapie auf. Eine milde, in der Regel asymptomatische Hyperkaliämie wurde häufig bei Patienten berichtet, die eine kombinierte Dapson- und Trimethoprim-Therapie erhielten. Die Serumkaliumkonzentrationen normalisierten sich jedoch in der Regel während fortgesetzter Therapie.
Weitere unerwünschte Effekte
Verschwommenes Sehen, Tinnitus, Fieber, Phototoxizität, hyperpigmentierte Makulae, Hypoalbuminämie ohne Proteinurie, arzneimittelinduzierter Lupus erythematodes sowie ein infektiöse-Mononukleose-ähnliches Syndrom wurden mit diesem Arzneimittel berichtet. Tachykardie trat ebenfalls auf, insbesondere bei übermäßiger Dosierung des Arzneimittels.
Vorsichtsmaßnahmen und Kontraindikationen
Das Arzneimittel ist bei Patienten kontraindiziert, die gegenüber dem Arzneimittel oder seinen Derivaten, wie Sulfoxon-Natrium, überempfindlich sind. Es sollte nicht bei Patienten mit schwerer Anämie angewendet werden; die Anämie sollte vor Beginn der Therapie behandelt werden.
Das Arzneimittel sollte bei Patienten mit G-6-PD-Mangel, Methämoglobin-Reduktase-Mangel oder Hämoglobin M mit Vorsicht angewendet werden.
Das Arzneimittel sollte außerdem bei Patienten angewendet werden, die anderen Arzneimitteln oder Substanzen ausgesetzt sind, die eine Hämolyse auslösen können, sowie bei Patienten mit Erkrankungen, die mit Hämolyse einhergehen (e.g., bestimmte Infektionen und diabetische Ketose).
Einige Kliniker empfehlen, vor Beginn der Therapie bei Patienten mit humanem Immundefizienzvirus (HIV) auf einen G-6-PD-Mangel zu screenen und Hämoglobin- und Methämoglobinkonzentrationen sowie den Hämatokrit in solchen Patienten regelmäßig zu überwachen, insbesondere bei Patienten, die das Arzneimittel gleichzeitig mit Trimethoprim erhalten. Vollständige Blutbilder (CBCs) sollten während der Dapson-Therapie häufig durchgeführt werden.
Einige Kliniker empfehlen, CBCs während des ersten Therapemonats wöchentlich, in den nächsten 6 Monaten monatlich und danach alle 6 Monate durchzuführen. Wenn eine erhebliche Reduktion von Leukozyten, Thrombozyten oder der Hämatopoese erkennbar ist, sollte Dapson abgesetzt und der Patient engmaschig überwacht werden. Da toxische Hepatitis und cholestatischer Ikterus berichtet wurden, sollte die Leberfunktion, sofern möglich, vor und während der Therapie mit dem Arzneimittel überwacht werden. Wenn eine Abweichung der Leberfunktion erkennbar ist, sollte das Arzneimittel abgesetzt werden, bis die Ursache der Abweichung festgestellt ist.
Patienten sollten angewiesen werden, ihrem Behandler während der Therapie das Auftreten von Halsschmerzen, Fieber, Blässe, Purpura oder Ikterus zu melden.
Mutagenität und Karzinogenität
Dapson war in mikrobiellen Tests mit Salmonella typhimurium, mit oder ohne mikrosomale Aktivierung, nicht mutagen. In Tierstudien wurde eine karzinogene Wirkung festgestellt. Das Arzneimittel verursachte mesenchymale Tumoren in Milz und Peritoneum männlicher Ratten und weiblicher Mäuse sowie Schilddrüsenkarzinome bei weiblichen Ratten.
Schwangerschaft, Fertilität und Laktation
Reproduktionsstudien an Tieren wurden mit diesem Arzneimittel nicht durchgeführt. Obwohl es bei schwangeren Frauen ohne Hinweise auf fetale Anomalien angewendet wurde, sollte das Arzneimittel während der Schwangerschaft nur angewendet werden, wenn es eindeutig erforderlich ist. Bei Patienten mit Lepra sind einige Kliniker der Ansicht, dass der Nutzen der Fortführung der Therapie während der Schwangerschaft die potenziellen Risiken für den Fötus überwiegt. Unfruchtbarkeit wurde bei Männern berichtet, die das Arzneimittel erhielten; bei 2 Patienten stellte sich die Fertilität nach Absetzen des Arzneimittels wieder ein.
Da der Wirkstoff in die Milch übergeht und aufgrund des in Tierstudien nachgewiesenen tumorigenen Potenzials sollte er bei stillenden Frauen nicht angewendet werden. Es sollte entschieden werden, ob das Stillen oder das Arzneimittel abgesetzt wird, wobei die Bedeutung des Arzneimittels für die Frau zu berücksichtigen ist.
Wechselwirkungen
Dapson kann mit verschiedenen Arzneimitteln interagieren, was zu einem erhöhten Risiko für Nebenwirkungen führen kann.
|
Arzneimittel |
Art der Wechselwirkung |
Effekte |
Empfehlungen |
|
Didanosine (ddI) |
Verminderte Wirksamkeit von Dapson |
Versagen der Prävention einer Pneumocystis jiroveci Pneumonie bei ~40% der Patienten |
Dapson mindestens 2 Stunden zeitversetzt zu Didanosin verabreichen; laufende Studien zur Klärung der Wechselwirkung erforderlich. |
|
Clofazimine |
Geringer Einfluss auf die Pharmakokinetik von Dapson |
Vorübergehende Zunahme der renalen Ausscheidung; potenzielle Abschwächung der entzündungshemmenden Wirkung von Clofazimin |
Beide Arzneimittel fortführen; weitere Studien zur Bestätigung der Wechselwirkungen empfohlen. |
|
Pyrimethamine |
Erhöhtes Risiko hämatologischer Nebenwirkungen |
Agranulozytose bei gleichzeitiger Anwendung berichtet |
Patienten häufiger auf hämatologische Effekte überwachen; bei Patienten mit G-6-PD-Mangel mit Vorsicht anwenden. |
|
Rifampin |
Verringerte Serumkonzentrationen von Dapson |
Serumspiegel können bei gemeinsamer Anwendung 7-10-mal niedriger sein |
Im Allgemeinen keine Dosisanpassung während der gleichzeitigen Therapie bei Lepra erforderlich. |
|
Trimethoprim |
Erhöhte Plasmakonzentrationen von Dapson |
Verbesserte Wirksamkeit zur Behandlung der Pneumocystis-Pneumonie; höhere Raten an Methämoglobinämie und Therapieabbruch aufgrund von Nebenwirkungen |
Regelmäßige Überwachung auf Toxizität empfohlen; weitere pharmakokinetische Studien erforderlich. |
|
Probenecid |
Begrenzte Evidenz für eine Wechselwirkung |
Mögliche Beeinflussung der renalen Ausscheidung von Dapson-Metaboliten |
Als unwahrscheinlich und/oder klinisch irrelevant angesehen; keine spezifischen Empfehlungen verfügbar. |
|
Andere hämolytische Wirkstoffe |
Erhöhtes Risiko für Methämoglobinämie und Hämolyse |
Vorsicht bei Patienten mit G-6-PD-Mangel oder bei Exposition gegenüber hämolytischen Wirkstoffen |
Engmaschig auf hämolytische Effekte überwachen, wenn es zusammen mit anderen Wirkstoffen angewendet wird, die eine Hämolyse auslösen können. |
Überdosierung
Eine Überdosierung führt im Allgemeinen innerhalb weniger Minuten bis zu 24 Stunden zu Übelkeit, Erbrechen und Übererregbarkeit. Eine durch Methämoglobin verursachte Depression, Krampfanfälle und schwere Zyanose können auftreten und erfordern eine umgehende Behandlung. Eine Hämolyse kann 7-14 Tage nach einer akuten Einnahme auftreten.
Bei Patienten ohne G-6-PD-Mangel sollte eine durch Dapson verursachte Methämoglobinämie mit Methylenblau (1-2 mg/kg als langsame intravenöse (IV) Injektion) behandelt werden. Die Wirkung ist in der Regel innerhalb von 30 Minuten vollständig, jedoch kann Methylenblau erneut verabreicht werden müssen, wenn sich Methämoglobin wieder ansammelt.
Alternativ kann Methylenblau in nicht notfallmäßigen Situationen oral in einer Dosis von 3-5 mg/kg alle 4-6 Stunden gegeben werden. Methylenblau sollte bei Patienten mit G-6-PD-Mangel nicht verabreicht werden, da die Reduktion von Methylenblau von G-6-PD abhängt. Orale Aktivkohle (20 g 4-mal täglich) hat sich in mehreren Fällen einer akuten Überdosierung als wirksam erwiesen, um die Elimination des Arzneimittels und seines Monoacetyl-Derivats deutlich zu erhöhen. Einige Kliniker empfehlen sie als Therapie der Wahl im Management akuter Intoxikationen. Hämodialyse verbessert ebenfalls die Elimination des Arzneimittels und seines Monoacetyl-Derivats.
Lagerung
Dapson-Tabletten sollten in gut verschlossenen, lichtbeständigen Behältern bei weniger als 40°C, vorzugsweise zwischen 15-30°C, gelagert werden.