Toxoplasma gondii
Allgemeine Überlegungen
Epidemiologie
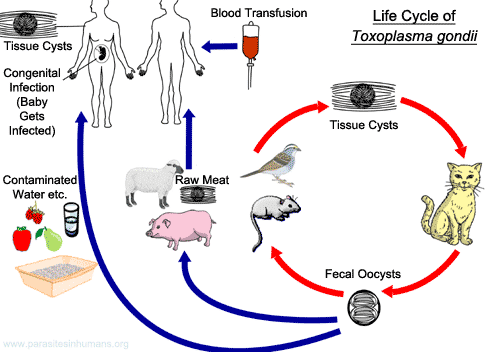
Die Infektion mit Toxoplasma gondii (Toxoplasmose) ist eine Zoonose; definitive Wirte sind Mitglieder der Katzenfamilie. Die beiden häufigsten Infektionswege beim Menschen sind die orale Aufnahme des Parasiten und die transplazentare (kongenitale) Übertragung auf den Fötus. Die Aufnahme von unzureichend gegartem oder rohem Fleisch, das Zysten enthält, oder von Wasser bzw. Lebensmitteln, die mit Oozysten kontaminiert sind, führt zu einer akuten Infektion.
Beim Menschen nimmt die Prävalenz der Toxoplasmose mit dem Alter zu. Es bestehen beträchtliche geografische Unterschiede in den Prävalenzraten (z. B. 10 % in Palo Alto, CA; 15 % in Boston, MA; 30 % in Birmingham, AL; 70 % in Frankreich; etwa 90 % in El Salvador). Unterschiede in der Epidemiologie der T. gondii-Infektion zwischen geografischen Regionen sowie zwischen Bevölkerungsgruppen innerhalb derselben Region lassen sich durch unterschiedliche Exposition gegenüber dem Erreger erklären. Gelegentlich treten Ausbrüche innerhalb von Familien oder bestimmten Populationen auf. Bei jedem kürzlich erworbenen akuten Infektionsfall sollte daher stets die Möglichkeit eines Ausbruchs in Betracht gezogen werden.
Die Inzidenz der kongenitalen Toxoplasmose korreliert direkt mit drei Faktoren: (1) der Prävalenz der Erstinfektion bei Frauen während der Schwangerschaft, (2) dem Gestationsalter, in dem die schwangere Frau die Infektion erwirbt, und (3) den verfügbaren Public-Health-Programmen zur Prävention, Erkennung und Behandlung der Infektion während der Schwangerschaft. Obwohl in einigen Ländern wie Österreich und Frankreich ein Screening auf Toxoplasma-Infektionen während der Schwangerschaft verpflichtend ist, wird in den Vereinigten Staaten kein routinemäßiges serologisches Screening durchgeführt. Ohne therapeutische Intervention liegt die Inzidenz der kongenitalen Toxoplasmose bei etwa 15 % für einen Fötus, dessen Mutter im ersten Trimester infiziert wird, bei 30 % im zweiten Trimester und bei 60 % im dritten Trimester. Spiramycin senkt die Inzidenz der fetalen Infektion um etwa 60 %. Es wurde berichtet, dass bei mütterlicher Infektion in den ersten 2 Gestationswochen und durchgehender Gabe von Spiramycin während der gesamten Schwangerschaft die Inzidenz der fetalen Infektion vernachlässigbar ist.
Als opportunistischer Erreger bei HIV-infizierten Personen hat T. gondii erhebliche Auswirkungen auf die öffentliche Gesundheit. Die Inzidenz der Toxoplasmose in einer HIV-infizierten Population korreliert direkt mit vier Faktoren: (1) der Prävalenz von Anti-Toxoplasma-Antikörpern, (2) dem Grad der Immunsuppression, geschätzt anhand der CD4-Zellzahl, (3) der Häufigkeit der Anwendung wirksamer Prophylaxeregime gegen eine Reaktivierung von Toxoplasma und (4) der Häufigkeit der Anwendung hochaktiver antiretroviraler Therapie. Von den Personen, die sowohl HIV- als auch Toxoplasma-seropositiv sind und CD4-Zahlen unter 100 Zellen/mm3 aufweisen, entwickeln 30 %-50 % eine toxoplasmatische Enzephalitis (TE), wenn keine Prophylaxe angewendet wird. Genetische Faktoren könnten ebenfalls eine Rolle bei der Prädisposition von AIDS-Patienten für diese Erkrankung spielen. Dies basiert auf Erkenntnissen aus einem murinen TE-Modell und auf der Beobachtung, dass nicht alle HIV-infizierten Patienten mit positiver T. gondii-Serologie TE entwickeln. Das humane Lymphozytenantigen DQ3 scheint ein genetischer Marker für die Anfälligkeit für die Entwicklung von TE bei AIDS-Patienten zu sein, während DQ1 möglicherweise ein Resistenzmarker ist.
Bereits vor dem Ausbruch von AIDS wurde TE als eine Hauptursache für Morbidität und Mortalität bei nicht HIV-immunsupprimierten Patienten erkannt, insbesondere bei Personen, deren Grunderkrankung oder Therapie eine Defizienz der T-Zell-vermittelten Immunität verursacht (z. B. Hodgkin-Krankheit sowie Herz-, Lungen-, Nieren- und Knochenmarktransplantationen).
Mikrobiologie
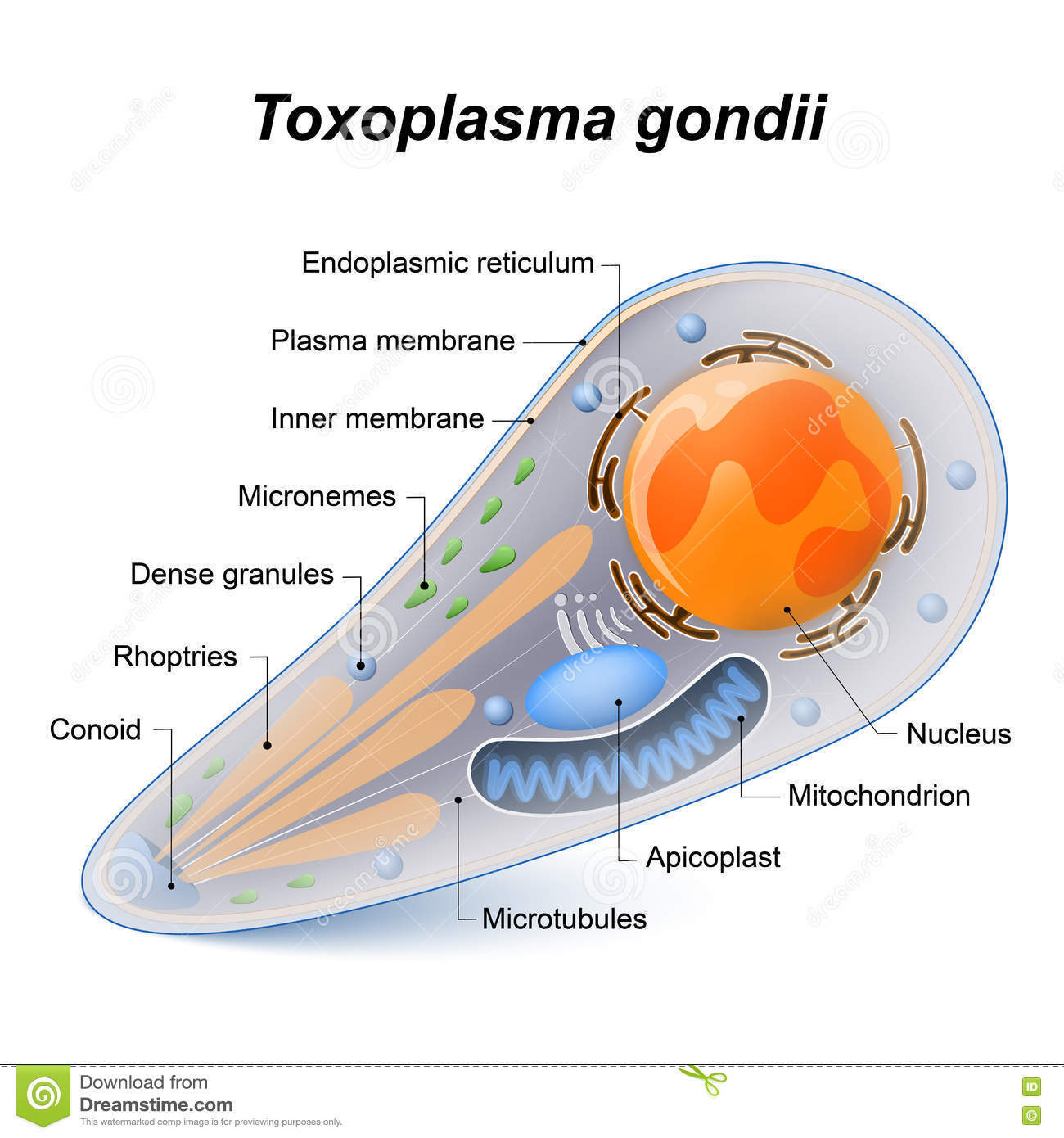
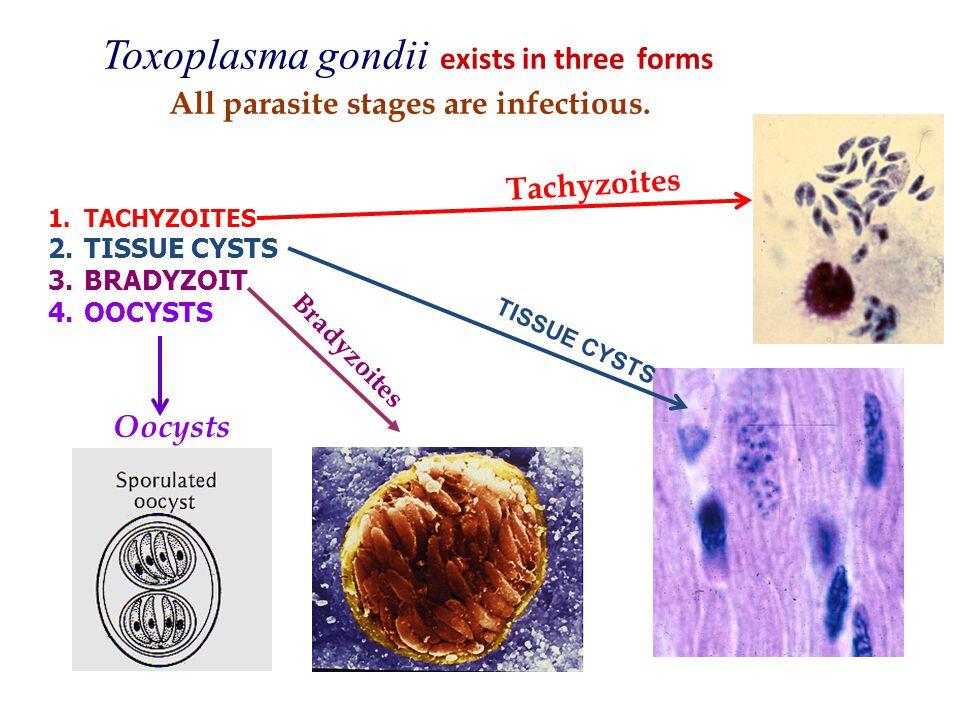
T. gondii ist ein obligat intrazellulärer kokzidienartiger Protozoon, der in drei Formen vorkommt: Oozyste (setzt Sporozoiten frei), Tachyzoit und Gewebezyste (enthält Bradyzoiten und kann diese freisetzen). Der Parasit durchläuft zwei Zyklen: einen enteroepithelialen sexuellen Zyklus im Dünndarm von Katzenfamilienmitgliedern und einen extraintestinalen asexuellen Zyklus bei Katzen sowie bei allen anderen infizierten Tieren, einschließlich des Menschen. Katzen scheiden Oozysten aus, nachdem sie eine der drei Formen des Parasiten aufgenommen haben. Menschen infizieren sich in der Regel durch den Verzehr von Gewebezysten (im Fleisch) oder Oozysten (im Katzenkot). Die äußeren Wände beider Formen werden durch enzymatischen Abbau zerstört, und die Parasiten gelangen in das Darmlumen. Dort entwickeln sie sich zu Tachyzoiten und verbreiten sich nahezu in alle Zellen und Gewebe des Körpers.
- Oozyste. Oozysten werden im Dünndarm von Mitgliedern der Katzenfamilie gebildet und 7-20 Tage lang mit deren Kot ausgeschieden. Sie sind gegenüber Umweltbedingungen hochresistent. Bis zu 10 Millionen Oozysten können an einem einzigen Tag ausgeschieden werden. Sie werden nach 1-21 Tagen infektiös (durch Sporulation), abhängig von Temperatur und Sauerstoffverfügbarkeit.
- Tachyzoit. Tachyzoiten sind sichel- oder ovalförmig und messen 2-4 µm in der Breite und 4-8 µm in der Länge. Sie benötigen einen intrazellulären Lebensraum, um zu überleben und sich zu vermehren, obwohl sie einen eigenen Golgi-Apparat, Ribosomen und Mitochondrien besitzen. Tachyzoiten dringen aktiv in Wirtszellen ein; dies wird durch Bestandteile eines "apikalen Komplexes" ermöglicht (daher der Begriff Apikomplexa). Sie persistieren und vermehren sich in einer intrazellulären parasitophoren Vakuole, deren Zusammensetzung (z. B. Säuregehalt) weitgehend vom Parasiten bestimmt wird. Im Labor werden Tachyzoiten im Peritoneum von Mäusen und in Zellkulturen von Säugetierzellen kultiviert. Das Vorhandensein von Tachyzoiten in menschlichen Flüssigkeiten oder Geweben ist ein Kennzeichen einer akuten Infektion.
- Gewebezyste. Nach Invasion und Replikation der Tachyzoiten kann es zur Zystenbildung kommen. Die genauen Bedingungen, die die Zystenbildung fördern, sind nicht bekannt. Die Gewebezyste bildet sich innerhalb einer Wirtszelle. Ihre Größe reicht von Zysten mit nur wenigen Organismen (Bradyzoiten) bis zu Zysten mit etwa 200 µm Durchmesser, die mehrere Tausend Bradyzoiten enthalten. Gewebezysten färben sich gut mit Periodic Acid-Schiff-Reagenz, Wright-Giemsa, Gomori-Methenamin-Silber und Immunperoxidasefärbungen. Die Zysten sind kugelförmig, wenn sie im Gehirn gefunden werden, und passen sich der Form von Muskelfasern im Herz- und Skelettmuskel an. Die häufigsten Orte einer latenten Infektion sind das zentrale Nervensystem (ZNS), das Auge sowie die Skelett-, glatte und Herzmuskulatur. Aufgrund dieser Gewebepersistenz bedeutet der Nachweis von Zysten in histologischen Schnitten nicht zwangsläufig, dass die Infektion kürzlich erworben wurde oder klinisch relevant ist.
- Stadiumskonversion. Tachyzoiten und Bradyzoiten unterscheiden sich phänotypisch. Tachyzoiten vermehren sich schnell und synchron, bilden Rosetten und lysieren die Zelle. Bradyzoiten replizieren langsamer und bilden Gewebezysten. Wesentliche Unterschiede im Energiestoffwechsel und in der antigenen Struktur von Tachyzoiten und Bradyzoiten spiegeln die Expression stadien-spezifischer Wege und Moleküle wider. Diese fördern das Überleben des Parasiten in unterschiedlichen Umgebungen und unter verschiedenen Bedingungen im Wirt.
Pathogenese
T. gondii vermehrt sich in Zellen an der Invasionsstelle; der Gastrointestinaltrakt scheint in der Natur der Hauptinfektionsweg und der initiale Infektionsort zu sein. Nach dem Zerfall der Wirtszelle dringen Parasiten in benachbarte Zellen ein und verbreiten sich über Lymphbahnen und Blutstrom im Körper. Die humorale und zelluläre Immunität begrenzen offenbar erfolgreich die parasitämische Phase; nur Parasiten, die durch einen intrazellulären Lebensraum oder durch Gewebezysten geschützt sind, überleben. Eine wirksame Immunantwort ist zudem für eine frühe, deutliche Reduktion der Anzahl von T. gondii in allen Geweben verantwortlich. Danach lassen sich Tachyzoiten in Geweben nur noch selten nachweisen.
Die Gewebezystenform ist für die persistierende Infektion verantwortlich und verbleibt vor allem im Gehirn, in der Skelett- und Herzmuskulatur sowie im Auge. Eine Toxoplasmose kann bei schwer immundefizienten Personen zwar durch eine Primärinfektion verursacht werden, ist jedoch meist die Folge einer Reaktivierung einer latenten Infektion.
Die histopathologischen Veränderungen der toxoplasmatischen Lymphadenitis sind bei immunkompetenten Personen häufig diagnostisch. Es besteht eine charakteristische Trias: reaktive Follikelhyperplasie, unregelmäßige Cluster epithelioider Histiozyten, die die Ränder der Keimzentren überlappen und verwischen, sowie fokale Sinuserweiterungen mit monocytoiden Zellen.
Eine okuläre Beteiligung bei immunkompetenten Patienten manifestiert sich als akute Retinochorioiditis, die durch Nekrose und eine ausgeprägte Entzündung gekennzeichnet ist. Eine granulomatöse Entzündung der Aderhaut tritt sekundär zur nekrotisierenden Retinitis auf.
Eine ZNS-Beteiligung ist durch multiple vergrößerte Herde mit Nekrosen und Mikroglianoduli gekennzeichnet. Nekrose ist aufgrund der Gefäßbeteiligung das herausragende Merkmal der Erkrankung. Multiple Hirnabszesse sind das typischste Merkmal der TE bei schwer immundefizienten Patienten, insbesondere bei AIDS-Patienten. Bei der Autopsie der meisten AIDS-Patienten mit TE sind die zerebralen Hemisphären betroffen, mit einer auffälligen Präferenz für die Basalganglien. Pulmonale Toxoplasmose bei immundefizienten Patienten kann sich als interstitielle Pneumonitis, nekrotisierende Pneumonitis, Konsolidierung und/oder Pleuraerguss präsentieren. Eine Chorioretinitis bei AIDS-Patienten ist durch segmentale Panophthalmitis und Bereiche koagulativer Nekrose gekennzeichnet, die mit Gewebezysten und Tachyzoiten assoziiert sind.
Immunität gegen T. gondii
Nach einer Erkrankung beim immunkompetenten Wirt besteht eine lebenslange Immunität gegen T. gondii. Für die Abwehr im Gehirn scheint die zelluläre Immunität wichtiger zu sein als die humorale Immunität. Den Verlauf der Parasiten-Wirts-Interaktion bestimmt offenbar eine gut koordinierte Interaktion zwischen CD4- und CD8-T-Lymphozyten, lymphokinaktivierten Killerzellen, natürlichen Killerzellen, γδ-T-Zellen sowie Zytokinen wie Interferon-γ, Tumornekrosefaktor-α, Interleukin-1 (IL-1), IL-2, IL-4, IL-6, IL-7, IL-10, IL-12 und IL-15. Stickstoffmonoxid könnte eine gewebespezifische Schutzfunktion erfüllen.
Die Differenzialdiagnose der toxoplasmatischen Lymphadenitis umfasst Lymphom, Epstein-Barr-Virus-assoziierte infektiöse Mononukleose, CMV-"Mononukleose", Katzenkratzkrankheit, Sarkoidose, Tuberkulose, Tularämie und metastasierenden Karzinombefall. Bei toxoplasmatischer Enzephalitis umfasst die Differenzialdiagnose primäres ZNS-Lymphom, JC-Virus-assoziierte progressive multifokale Leukenzephalopathie, CMV-Ventrikulitis, Tuberkulom, Kryptokokkom sowie bakterielle oder durch Nocardia verursachte Hirnabszesse. Keines der bei Neugeborenen mit kongenitaler Erkrankung beschriebenen Zeichen ist pathognomonisch für Toxoplasmose; alle können durch kongenitale Infektionen mit anderen Erregern wie CMV, Treponema pallidum, Herpes-simplex-Virus und Rötelnvirus nachgeahmt werden.
Komplikationen
In seltenen Fällen verursacht Toxoplasmose bei gesunden Personen eine Myokarditis, Polymyositis, Pneumonitis, Hepatitis oder Enzephalitis. Frühe maternale Infektionen führen gelegentlich zum intrauterinen Tod des Fötus und zu spontanem Abort.
Prävention und Kontrolle
Die Prävention der Erstinfektion ist bei schwangeren Frauen und immundefizienten, seronegativen Patienten von größter Bedeutung (Box 6). Gewebezysten im Fleisch werden durch Erhitzen auf 66 °C inaktiviert; das Fleisch sollte vollständig durchgegart sein, ohne rosa Mitte. Auch Räuchern oder Pökeln sowie Einfrieren auf -20 °C (wird in den meisten Heimgefrierschränken nicht erreicht) inaktivieren Gewebezysten. Nach dem Umgang mit rohem Fleisch oder Gemüse sollten die Hände gründlich gewaschen werden. Eier sollten nicht roh verzehrt werden, und nicht pasteurisierte Milch (insbesondere Ziegenmilch) sollte vermieden werden. Fliegen und Kakerlaken sollten bekämpft werden. Bereiche, die mit Katzenkot kontaminiert sind, sollten vollständig gemieden werden. Beim Entsorgen von Katzenstreu (falls diese Tätigkeit nicht vollständig vermieden werden kann), bei der Gartenarbeit oder beim Reinigen eines Kindersandkastens sollten Einweghandschuhe getragen werden. Oozysten werden abgetötet, wenn der Katzenstreu-Behälter 5 Minuten in nahezu kochendem Wasser eingeweicht wird. Wenn der Streu-Behälter täglich gereinigt wird, haben Oozysten keine Möglichkeit zur Sporulation.
Derzeit ist kein Impfstoff zur Prävention der Toxoplasmose beim Menschen verfügbar; eine Primärprophylaxe gegen Toxoplasmose bei AIDS-Patienten mit hohem Risiko für die Entwicklung einer TE hat sich als wirksam erwiesen. Die Primärprophylaxe wird für seropositive Patienten mit einer CD4-Zahl von weniger als 100 Zellen/mm3 empfohlen (einige Experten verwenden eine Grenze von weniger als 200 Zellen/mm3), unabhängig von der HIV-RNA-Viruslast. Trimethoprim/Sulfamethoxazol und Dapson plus Pyrimethamin wurden als wirksame Regime zur Verhinderung der ersten TE-Episode beschrieben (Box 7). Pyrimethamin wurde posttransplantativ zur Primärprophylaxe bei seronegativen Herztransplantat-Empfängern mit seropositiven Spendern eingesetzt (Box 7).
| Test oder Methode |
|---|
| Serologie (IgG) ist nützlich, um festzustellen, ob der Patient T. gondii ausgesetzt war.1 Sie kann außerdem Hinweise geben, ob die Infektion akut oder chronisch ist.2,3 |
| Histologie (Hämatoxylin-Eosin-, Immunperoxidase-, Wright-Giemsa- und Periodic Acid-Schiff-Färbungen). Das Vorhandensein von Tachyzoiten ist diagnostisch für eine akute Infektion. Einzelne Zysten sprechen nicht zwingend für eine akute oder reaktivierte Erkrankung. |
| Isolation des Parasiten aus jedem Gewebe durch Inokulation in Maus oder Zellkultur ist diagnostisch.2 |
| PCR-basierter DNA-Nachweis in Fruchtwasser, Liquor, okulären Flüssigkeiten, bronchoalveolärer Lavage, peripherem Blut und Urin ist diagnostisch.2 |
| Radiologische Untersuchungen sind hilfreich bei Verdacht auf ZNS-Toxoplasmose beim Fötus oder Neugeborenen (Ultraschall oder CT) sowie bei immungeschwächten Patienten (CT oder MRT). |
| Okuläre Toxoplasmose wird in den meisten Fällen klinisch diagnostiziert. |
- Bestätigende serologische Tests umfassen den Sabin-Feldman-Färbetest für IgG, IgM-ELISA, IgA-ELISA, differenziellen Agglutinationstest und IgE-ELISA.
- Die Konsultation eines Referenzlabors wird dringend empfohlen.
- Eine serologische Diagnostik kann bei immungeschwächten Personen nicht hilfreich sein.
| IgG-Ergebnis | IgM-Ergebnis | Interpretation und Empfehlung |
|---|---|---|
| Negativ | Negativ | Kein serologischer Hinweis auf eine T. gondii-Infektion |
| Negativ | Unklar oder positiv | Mögliche akute Infektion oder falsch-positives IgM; Probe an ein Referenzlabor senden |
| Unklar bei IgG in anderem Testverfahren | Negativ | Indeterminiert; neue Probe zur Untersuchung entnehmen oder erneut testen |
| Unklar | Unklar | Indeterminiert; neue Probe für IgG und IgM entnehmen |
| Unklar | Positiv | Mögliche akute Infektion; Probe an ein Referenzlabor senden |
| Positiv | Negativ | Seit mehr als 6 Monaten mit T. gondii infiziert |
| Positiv | Unklar oder positiv | Mögliche akute Infektion; Probe an ein Referenzlabor senden |
Modifiziert nach US Food and Drug Administration Public Health Advisory: Einschränkungen kommerzieller Toxoplasma-IgM-Testkits.
| Patientengruppe | Klinische Syndrome |
|---|---|
| Immunkompetent |
|
| Immungeschwächt |
|
| Schwanger |
|
| Fötus |
|
| Neugeborenes |
|
- Die Syndrome schließen sich nicht gegenseitig aus. Patienten können gleichzeitig oder nacheinander zwei oder mehr Syndrome aufweisen (z. B. kann ein ansonsten immunkompetenter Patient Lymphadenitis und Chorioretinitis haben, oder ein Neugeborenes präsentiert sich mit Hydrozephalus, zerebralen Verkalkungen und Thrombozytopenie).
| Sy | Kinder | Erwachsene |
|---|---|---|
| Lymphadenitis1 | Keine Therapie | Keine Therapie |
| Chorioretinitis (aktiv), Myokarditis, Polymyositis, systemisch2 |
|
|
- Eine Behandlung kann angezeigt sein, wenn Begleitsymptome schwerwiegend oder anhaltend sind.
- Die Rolle anderer Regime, einschließlich Medikamente wie Atovaquon, Clarithromycin, Azithromycin, Trimethoprim/Sulfamethoxazol oder Dapson, ist nicht gut etabliert.
- Clindamycin (300 mg oral alle 6 Stunden für mindestens 3 Wochen) ist eine Alternative bei Sulfonamid-Allergikern.
| Sy | Medikament | Dosis |
|---|---|---|
| Akute Infektion während der Schwangerschaft erworben | Spiramycin | 3 g/Tag; sollte während der gesamten Schwangerschaft fortgesetzt werden, auch wenn die PCR des Fruchtwassers negativ ist |
| Positives Fruchtwasser-PCR-Ergebnis ab der 18. Schwangerschaftswoche oder später | Pyrimethamin PLUS Sulfadiazin PLUS Folsäure | Beginn nach der 18. Schwangerschaftswoche; gleiche Dosierung wie bei immunkompetenten Patienten |
| Medikament | Dosis |
|---|---|
| Pyrimethamin | Ladedosis: 2 mg/kg/Tag (maximal 50 mg) für 2 Tage, dann 1 mg/kg/Tag für 2 oder 6 Monate; nach 2 oder 6 Monaten 1 mg/kg/Tag montags, mittwochs und freitags |
| Sulfadiazin1 | 50 mg/kg alle 12 Stunden |
| Folsäure | 5-20 mg dreimal wöchentlich |
| Kortikosteroide (falls angezeigt) | 1 mg/kg/Tag in 2 geteilten Dosen |
- Clindamycin ist eine Alternative bei Sulfonamid-Allergikern.
| Regimenskomponente | Kinder | Erwachsene |
|---|---|---|
| Pyrimethamin | Ladedosis: 2 mg/kg/Tag (maximal 50 mg) für 2 Tage, dann Erhaltungsdosis 1 mg/kg/Tag (maximal 25 mg) | Ladedosis: 200 mg über 24 Stunden, gefolgt von 50-75 mg/Tag |
| Sulfadiazin1 | Ladedosis: 75 mg/kg, dann Erhaltungsdosis 50 mg/kg alle 12 Stunden (maximal 4 g/Tag) | Ladedosis: 2-4 g initial, gefolgt von 1-1,5 g viermal täglich |
| Folsäure | 5-20 mg dreimal wöchentlich | 5-10 mg/Tag (bis zu 50 mg/Tag) |
- Clindamycin (300 mg oral alle 6 Stunden für mindestens 3 Wochen) ist eine Alternative bei Sulfonamid-Allergikern.
| Infektiöse Form | Präventive Maßnahmen |
|---|---|
| Gewebezyste (Fleisch) |
|
| Oozyste (Katzenkot) |
|
| Patientengruppe | Regime |
|---|---|
| AIDS-Patienten mit hohem Risiko für die Entwicklung einer TE | Trimethoprim/Sulfamethoxazol (entweder 160 mg/800 mg oder 80 mg/400 mg/Tag) oder Dapson (50 mg/Tag) plus Pyrimethamin (50 mg/Woche) |
| Herztransplantat-Empfänger mit seropositiven Spendern | Pyrimethamin 25 mg oral einmal täglich für 6 Wochen nach Transplantation |
Weitere Informationen:
https://www.ncbi.nlm.nih.gov/books/NBK7752/
https://www.cdc.gov/parasites/toxoplasmosis/gen_info/faqs.html

















