Nematoden
Grundlagen der Diagnose
- Intestinale Nematoden: Nachweis charakteristischer Eier oder Parasiten im Stuhl.
- Blutbahn-Nematoden (Filariose): Eine klinische Diagnose ist möglich; ein frischer Blutausstrich kann die Diagnose bestätigen.
- Gewebsnematoden: Eine klinische Diagnose ist möglich; eine Hautbiopsie oder andere Gewebeuntersuchungen können den Erreger nachweisen.
Eine genaue Diagnose erfordert in der Regel die Korrelation klinischer Befunde mit geeigneten Proben. Bei intestinalen Infektionen erhöhen wiederholte Stuhluntersuchungen die Sensitivität. Bei Gewebe- und Blutnematoden sind dagegen der Zeitpunkt der Probenentnahme und eine sorgfältige mikroskopische Untersuchung entscheidend.
Allgemeine Überlegungen
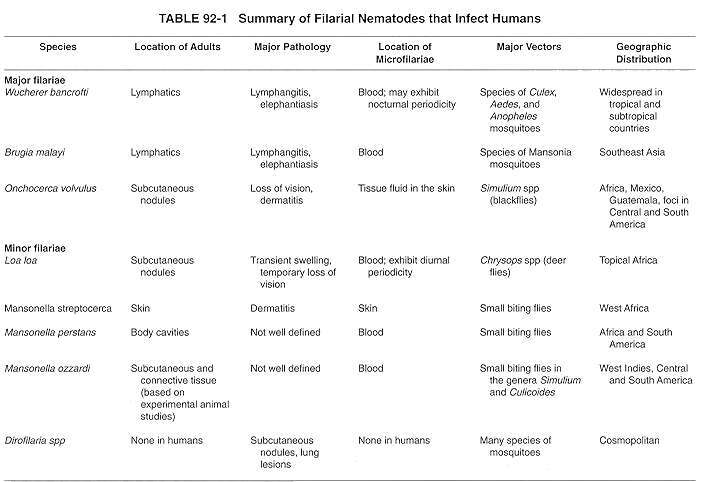
Nematoden (Rundwürmer) sind nicht segmentierte, zugespitzte, bilateral symmetrische, zylindrische Organismen mit vollständigem Verdauungstrakt und geschlechtlicher Fortpflanzung. Obwohl mehr als 500.000 Nematodenarten beschrieben wurden, werden nur wenige als humane Parasiten häufig angetroffen. Die meisten Nematoden haben komplexe Lebenszyklen mit mehreren Larvenstadien sowie Zwischenwirten oder freilebenden Phasen. Pathogene Nematoden lassen sich hauptsächlich in intestinale oder extraintestinale Gewebeparasiten einteilen (Tabelle 1).
ANDERE GEWEBSNEMATODEN-INFEKTIONEN
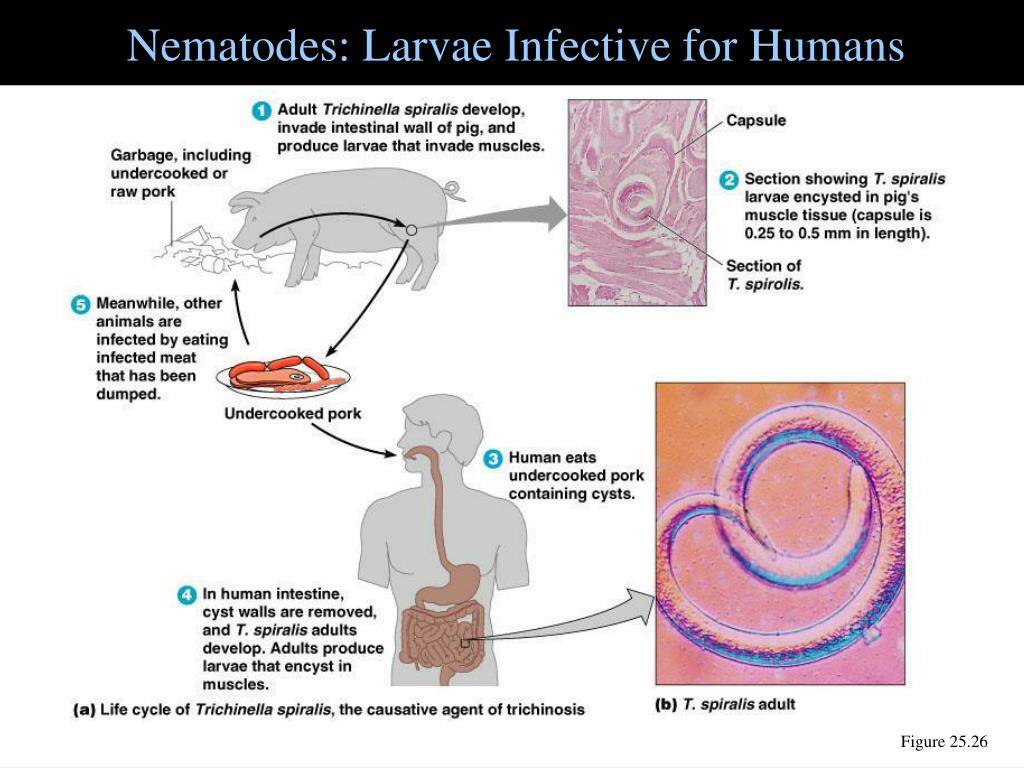
TRICHINOSE
Trichinella-Arten sind unter den gewebsbesiedelnden Nematoden einzigartig, da sie keine intermediäre Gliederfüßer-Zwischenwirtsphase besitzen. Trichinella-Nematoden parasitieren Karnivoren. Die adulten Würmer parasitieren den Dünndarm; infektiöse Larven werden freigesetzt und wandern vom Darm in das Muskelgewebe des Wirts, wo sie einkapseln und mehrere Jahre lebensfähig und infektiös bleiben. Wenn diese Wirtsgewebe verzehrt werden, werden die Zystenwände verdaut, und die Larven reifen innerhalb weniger Tage im Darm des neuen Wirts erneut heran, womit der Lebenszyklus fortbesteht. Normale Wirte von Trichinella spp. sind Schweine, Ratten, Bären, Füchse, Walrosse und andere fleischfressende Säugetiere. Der Mensch ist ein Zufallswirt. Das Garen von Fleisch auf Kerntemperaturen von etwa 55°C (131°F) oder Einfrieren bei -15°C (5°F) für 3 Wochen tötet die Trichinella-Larven ab.
Klinische und Laborbefunde
Eine milde Infektion verläuft meist asymptomatisch. Zu Beginn (ca. 1 Woche nach der Infektion) dominieren gastrointestinale Symptome wie Durchfall, Übelkeit oder Erbrechen. Ab der zweiten Woche, während der Muskelinvasionsphase, überwiegen bei den meisten Patienten systemische Symptome einschließlich Fieber, Myalgien und allgemeinem Unwohlsein. Ein periorbitales Ödem mit Bindehautschwellung und Lidödemen ist charakteristisch und häufig. Die Symptome dauern 4 bis 8 Wochen an. Selten können Myokarditis oder Enzephalitis den klinischen Verlauf komplizieren. Laborchemisch ist ab dem 10. Tag eine teils ausgeprägte Eosinophilie charakteristisch, ebenso wie eine erhöhte Immunglobulin-E-Konzentration. Serumkreatinphosphokinase und Laktatdehydrogenase spiegeln die Myositis wider. Die Trichinella-Serologie wird etwa 3 Wochen nach der Infektion positiv.
Behandlung
Die Behandlung der Trichinose ist umstritten und in erster Linie unterstützend. Bei bekannter Aufnahme innerhalb von 24 Stunden wurde vorgeschlagen, Albendazol (400 mg zweimal täglich für 60 Tage), Mebendazol (200-400 mg dreimal täglich für 3 Tage, dann 400-500 mg dreimal täglich für 10 Tage) oder Thiabendazol (25 mg/kg/Tag für 1 Woche) einzusetzen, um eine Infektion zu verhindern. Diese Medikamente sind bei etablierter Infektion oder bei muskulären Larven nicht wirksam. Für die Muskelinvasionsphase wurde keine spezifische Therapie eindeutig als wirksam nachgewiesen.
Prognose
Eine spontane Erholung ist die Regel, obwohl die vollständige Genesung Wochen bis Monate dauern kann. Todesfälle, meist durch Myokarditis, Enzephalitis oder Pneumonitis, sind selten.
Prävention
Die Inzidenz der humanen Trichinose nahm in Industrieländern durch Maßnahmen zur Reduktion der Trichinoseprävalenz bei Schweinen ab. Trichinella in Wildfleisch (oder Schweinefleisch) lässt sich durch vollständiges Durchgaren auf Innentemperaturen über etwa 62°C (145°F) im gesamten Fleisch oder auf etwa 56°C (133°F) für mehr als 15 Minuten, durch Einfrieren bei -15°C (5°F) für 20 Tage oder durch Gamma-Bestrahlung abtöten.
TOXOKARIOSE (VISCERALE LARVA MIGRANS)
Toxokariose oder viscera larva migrans ist ein Syndrom, das durch die Invasion extraintestinalen menschlichen Gewebes durch Larven von Ascaris spp. verursacht wird, bei denen der Mensch nicht der übliche Wirt adulter Würmer ist. Toxocara canis, häufig bei Hunden, ist die am häufigsten beteiligte Art; auch Toxocara cati (Katzen) und Baylisascaris procyonis (Waschbären) werden genannt. Welpen können transplazentar oder transmammär infiziert werden. Die Trächtigkeit bei Hunden reaktiviert latente Infektionen in der Hündin. Tiere mit adulten Askariden im Darm scheiden große Mengen Eier in die Umwelt aus. Die Eier werden nach 3-4 Wochen infektiös und sind gegen raue Umweltbedingungen sehr widerstandsfähig. Toxocara-Eier können über Monate bis Jahre infektiös bleiben. Die Infektion des Menschen erfolgt durch die Aufnahme von Eiern aus fäkal kontaminiertem Boden, z. B. bei Kindern mit Pica. Eine direkte Übertragung von Haustieren auf den Menschen erfolgt nicht, da die Eier im Boden reifen müssen, bevor sie infektiös werden.
Bei jungen Tieren schlüpfen die aufgenommenen Eier im Darm, und die Larven wandern durch extraintestinale Gewebe, einschließlich Leber und Lunge. Die Larven verursachen Husten, werden verschluckt und reifen dann im Dünndarm zu adulten Würmern heran; der Lebenszyklus ähnelt dem von Ascaris lumbricoides beim Menschen. Bei älteren Tieren, beim Menschen und bei anderen Wirten wie Mäusen oder Ratten schlüpfen die Larven ebenfalls aus den aufgenommenen Eiern und dringen in extraintestinale Gewebe ein, können sich jedoch nicht vollständig entwickeln und persistieren als "Zweitstadium"-Larven etwa 6 Monate in den Geweben. Wenn diese Larven von Hunden oder Katzen aufgenommen werden, können sie den Lebenszyklus abschließen und zu adulten intestinalen Würmern heranreifen. Eosinophile Granulome bei Toxokariose betreffen meist Leber oder Lunge; auch eine Beteiligung von Gehirn, Augen, Muskeln und Haut wurde beschrieben.
Klinische und Laborbefunde
Viscera larva migrans wird überwiegend bei Kindern unter 7 Jahren beobachtet und kann mit Pica assoziiert sein. Die meisten Fälle verlaufen asymptomatisch. Wenn Symptome auftreten, sind diese variabel und abhängig von den betroffenen Organen; sie können Fieber, Husten oder Keuchen sowie Urtikaria oder Hautknoten umfassen. Eine Hepatomegalie ist relativ häufig. Splenomegalie, Lymphadenopathie und Zeichen einer Myokarditis sind seltener.
Eine ausgeprägte Leukozytose, teilweise über 100.000 Leukozyten/µl, und eine starke Eosinophilie sind bei viscera larva migrans häufig. Eine polyklonale Hypergammaglobulinämie sowie Anti-A- oder Anti-B-Antikörper gegen Isohämagglutinin-Antigene (kreuzreaktiv mit T.-canis-Larvenantigenen) können auftreten. Bei Beteiligung des zentralen Nervensystems kann eine eosinophile Pleozytose im Liquor vorliegen. Röntgenveränderungen im Thorax sind bei etwa einem Drittel der Patienten erkennbar. Die Toxocara-Serologie kann zur Diagnosesicherung hilfreich sein; in manchen Populationen ist jedoch die Hintergrundprävalenz der Seropositivität bei Patienten ohne klinisch erkennbare viscera larva migrans hoch. Der Nachweis von Larven in Gewebebiopsien ist diagnostisch, aber wenig sensitiv. Stuhluntersuchungen sind meist nicht hilfreich.
Die okuläre viscera larva migrans verdient besondere Beachtung. Eine Infektion des Auges mit Toxocara-Larven präsentiert sich meist als isolierter Befund bei Patienten ohne bekannte viscera larva migrans und ohne systemische multifokale Symptome oder Zeichen. Typisch ist eine einseitige, hintere oder periphere eosinophile Entzündungsmasse. Serologische Tests können negativ sein. Die okuläre Läsion kann mit einem Retinoblastom verwechselt werden.
Behandlung
Eine spezifische Therapie ist nicht nachweislich wirksam. In vielen Fällen sind die Symptome selbstlimitierend, und eine unterstützende symptomatische Behandlung genügt. Verschiedene Antihelmintika wurden mit begrenztem Erfolg eingesetzt, darunter Albendazol, Thiabendazol, Mebendazol, Diethylcarbamazin oder Ivermectin. Kortikosteroide können in einigen Fällen vorteilhaft sein, insbesondere bei subkonjunktivaler Anwendung bei okulärer viscera larva migrans.
Prävention und Prognose
Welpen, Kätzchen und Hauskaniden, insbesondere während Trächtigkeit oder Laktation, sollten untersucht und bei Bedarf behandelt werden, um eine Übertragung auf den Menschen zu verhindern. Pica sollte vermieden werden. Die meisten Fälle verlaufen selbstlimitierend, obwohl Symptome über mehrere Monate bis Jahre anhalten können.
DRACUNCULIASE
Dracunculiasis oder Guinea-Wurm-Erkrankung wird durch den Gewebsnematoden Dracunculus medinensis verursacht. Der Parasit war weit verbreitet auf dem indischen Subkontinent, der Arabischen Halbinsel sowie in bestimmten Regionen West- und Zentralafrikas nördlich des Äquators. Die Infektion erfolgt durch die Aufnahme von Wasser, das kleine Copepoden (Cyclops spp.; "Wasserflöhe") enthält, die infektiöse Drittstadienlarven tragen. Die Larven wandern in das subkutane Bindegewebe, meist der unteren Extremitäten, wo sie sich über eine verlängerte Inkubationszeit von bis zu einem Jahr zu adulten Würmern entwickeln. Das adulte weibliche Tier kann 60-80 cm lang werden. Wenn die Extremitäten mit Wasser in Kontakt kommen, tritt der Kopf des trächtigen Weibchens durch eine Ulzeration hervor, eine Uterusschleife prolabiert und entlässt große Mengen von Erststadienlarven ins Wasser, die von Copepoden aufgenommen werden, um den Lebenszyklus zu vollenden.
Ein von der Weltgesundheitsorganisation geführtes aktives Ausrottungsprogramm hat die Inzidenz der Dracunculiasis weltweit drastisch reduziert. Da kein nicht-menschliches Reservoir bekannt ist, könnte die Krankheit bald ausgerottet werden.
Klinische Befunde
Eine periphere chronische kutane Ulzeration, aus der der Wurm hervortreten kann, ist das Kennzeichen der Dracunculiasis. Eine lokale, schmerzhafte, stechende oder brennende Papel bildet häufig die erste Vorahnung der Ulzeration. Allgemeinsymptome wie Fieber, Übelkeit, Erbrechen, Dyspnoe, Urtikaria oder Pruritus sowie periorbitale Ödeme können mit der Entwicklung der Ulzeration einhergehen. Ulzera am Fuß erschweren oft das Gehen und können zu dauerhaften Deformitäten sowie zu sekundären Infektionen (einschließlich Gelenkinfektionen von Knie oder Sprunggelenk) führen. Tetanus kann ebenfalls eine Komplikation sein. Abgestorbene oder sterbende Würmer können heftige Entzündungsreaktionen auslösen. In endemischen Gebieten erfolgt die Diagnose klinisch anhand der typischen Befunde.
Behandlung
Es steht keine spezifische antihelmintische Therapie zur Verfügung, um adulte Würmer abzutöten. Die mechanische Entfernung der Würmer wird seit Jahrhunderten praktiziert. Die Behandlung konzentriert sich auf die Kontrolle von Komplikationen, einschließlich Bettruhe, Hochlagern der betroffenen Extremität, Wundversorgung und antibakterieller Therapie bei sekundären bakteriellen Wundinfektionen. Metronidazol, 250 mg oral dreimal täglich, Mebendazol, 400-800 mg oral täglich, oder Thiabendazol, 25 mg/kg zweimal täglich, können die Ausstoßung des Wurms fördern; ebenso kann das mehrfache tägliche Eintauchen der betroffenen Extremität in Wasser hilfreich sein.
Prävention
Sauberes Trinkwasser ist der Schlüssel zur Prävention der Dracunculiasis. Das Präventionsprogramm der Weltgesundheitsorganisation (WHO) konzentriert sich auf die Bereitstellung von sauberem Trinkwasser mittels Rohrbrunnen, Handpumpen oder Zisternen, die Behandlung von Trinkwasser mit Temephos (zur Eliminierung der Copepoden) oder das Abkochen des Wassers. Wasser kann auch filtriert werden, um Partikel > 100 µm zu entfernen.
| Kategorie | Beispiele | Bemerkungen |
|---|---|---|
| Intestinal |
|
Sie infizieren primär den Darmtrakt; einige Arten (z. B. intestinale Hakenwürmer von Hund und Katze) können beim Menschen auch eine kutane Larva migrans verursachen. |
| Gewebsbesiedelnd - Filariose |
|
Adulte Würmer leben in Lymphgefäßen oder subkutanen Geweben; Mikrofilarien zirkulieren im Blut oder in der Haut und werden durch Gliederfüßer übertragen. |
| Andere Gewebsnematoden |
|
Sie betreffen primär subkutanes Gewebe, Muskeln oder das zentrale Nervensystem und werden häufig über kontaminierte Nahrung, Wasser oder tierische Wirte erworben. |
1 Das Vorkommen bestimmter Nematoden hängt stark vom geografischen Gebiet ab. Gewebsbesiedelnde Nematoden sind in den USA selten oder nicht vorhanden.
| Infektion | Erstwahl | Zweitwahl |
|---|---|---|
| Ascariasis |
|
|
| Enterobiasis |
|
|
| Hakenwurm |
|
- |
| Strongyloidiasis |
|
|
| Trichuriasis |
|
|
|
1 Ancylostoma, Hakenwurm der "Alten Welt"; Necator, Hakenwurm der "Neuen Welt". |
||

















