Malaria und Babesiose
PLASMODIUM SPP.
- Expositionsanamnese, z. B. Reisen, kürzliche Bluttransfusion oder Aufenthalt in unmittelbarer Nähe eines internationalen Flughafens.
- Nichtfalciparum-Malaria: Schüttelfrost und Fieberspitzen, gefolgt von Fieberabfall und Müdigkeit; die Symptome können zyklisch alle 48-72 Stunden auftreten.
- Falciparum-Malaria: Fieberspitzen und Schüttelfrost, häufig nicht zyklisch, und verbunden mit rasch fortschreitenden systemischen Symptomen.
- Nachweis und Identifikation einer Plasmodium-Art im dicken und dünnen Blutausstrich, jeweils.
- Molekularer Nachweis des P. falciparum-Histidin-reichen Proteins mittels enzymgebundenem Immunadsorptionstest (ELISA) oder Nachweis von Plasmodium-DNA mittels Polymerase-Kettenreaktion (PCR) mit anschließender Speziesbestimmung durch Sondenhybridisierung oder DNA-Sequenzierung.
Diese Merkmale verdeutlichen, wie Expositionsanamnese, klinische Fiebermuster und Labortests zusammenwirken, um die Diagnose Malaria zu stützen. Eine rasche Erkennung ist wichtig, da einige Formen, insbesondere P. falciparum, schnell fortschreiten und bei nichtimmunen Personen lebensbedrohlich werden können.
Allgemeine Überlegungen
Epidemiologie
Malaria, eine Krankheit der Antike, wurde von Hippokrates erkannt und möglicherweise bereits um 1700 v. Chr. in alten chinesischen Texten beschrieben. Malaria ist eine globale Erkrankung, die am häufigsten in den Tropen auftritt; die Übertragung kann jedoch auch in gemäßigten Zonen erfolgen. Im 19. und frühen 20. Jahrhundert waren Plasmodium-Arten in den Vereinigten Staaten weit verbreitet. Diese Verbreitung umfasste den Süden der USA, das Mississippi-Tal sowie Gebiete bis hinauf nach Minnesota und Michigan.
Heutzutage verursachen Plasmodium-Parasiten hauptsächlich in tropischen Gebieten jährlich mehr als 100 Millionen Malariafälle. Dies führt schätzungsweise zu 1-2 Millionen Todesfällen pro Jahr, viele davon bei Kindern. Tatsächlich treten über 90 % der schweren, lebensbedrohlichen Malariafälle bei Kindern auf. Die Verbreitung des Mückenvektors und die Krankheitsprävalenz in indigenen Populationen sind die Hauptfaktoren für die Ausbreitung des Plasmodium-Parasiten.
Mückenverseuchte Gebiete wie Sümpfe sind seit langem mit hohen Malariaerkrankungsraten verbunden. Umweltbedingungen mit stehenden, langanhaltenden Wasserflächen fördern die Vermehrung von Mücken. Gegenwärtig zählen zu den endemischen Gebieten Teile der Karibik, Nord- und Südamerikas, Mittelamerikas, Teile Afrikas, Indiens, Australiens, Südostasiens sowie vieler Inseln im asiatisch-pazifischen Raum.
Malaria tritt auch sporadisch in nichtendemischen Gebieten auf. Häufig handelt es sich um importierte, latente Erkrankungen. Malariarückfälle können Monate nach Rückkehr von Reisen in endemische Gebiete auftreten. Diese Patienten wurden meist unvollständig behandelt oder haben eine unzureichende Chemoprophylaxe erhalten.
Rezidivierende Malaria wird durch Reaktivierung der latenten Hypnozoiten-Phase von P. vivax oder P. ovale verursacht. Patienten, die an Malaria erkranken, können mit einer Vielzahl von Wirkstoffen behandelt werden. Die am häufigsten eingesetzten Antimalariamittel Chloroquin und Mefloquin sind gegen die symptomatische, erythrozytäre Phase von P. vivax und P. ovale wirksam und können scheinbare Heilungen bewirken. Diese Medikamente sind jedoch gegen die hepatischen Hypnozoiten unwirksam. Patienten, die so behandelt werden, sind unvollständig therapiert und haben ein erhöhtes Risiko für einen Malariarückfall.
Manche Patienten geben an, zuvor nie an Malaria erkrankt zu sein. Eine gezielte Befragung zeigt jedoch häufig eine kurzzeitige Unterbrechung der Chemoprophylaxe. Eine solche Prophylaxelücke kann zu subprophylaktischen Medikamentenspiegeln führen. Während dieses Zeitraums können durch einen infizierten Mückenstich eingebrachte Sporozoiten die Leber erreichen und dort eine Infektion etablieren. Merozoiten, die aus der Leber freigesetzt werden, während die Chemoprophylaxe fortgeführt wird, werden rasch eliminiert, sodass der Patient asymptomatisch bleibt. Hypnozoiten können jedoch Monate nach Rückkehr aus einem endemischen Gebiet aktiv werden, lange nach Abbruch der Chemoprophylaxe. Die korrekte Identifikation von P. vivax und P. ovale ist wichtig, da nur diese Arten hepatische Hypnozoiten bilden und Rückfälle verursachen können.
In nichtendemischen Gebieten kann es zu sogenannten Fällen von "Flughafenmalaria" kommen. Es wird angenommen, dass Mückenvektoren aus endemischen Gebieten mit Flugzeugfracht transportiert werden. Personen, die in der Nähe eines Flughafens wohnen, können durch den Stich solcher Mücken infiziert werden. Der Parasit verbreitet sich in der Umwelt meist nicht weiter. Dies liegt entweder am Fehlen eines geeigneten Mückenwirts oder an der geringen Zahl parasitentragender Mücken in der Gemeinschaft. Bei geringer Malariahäufigkeit ist die Wahrscheinlichkeit, dass Mücken Gametozyten aufnehmen, sehr niedrig. Zudem kann das seltene Vorkommen infizierter Mücken dazu führen, dass diese eine nichtmenschliche Blutmahlzeit einnehmen und dadurch den parasitären Zyklus unterbrechen.
Die Übertragung durch Mücken ist der häufigste Infektionsweg, aber es existieren weitere Übertragungsarten. Die Übertragung kann durch intravenösen Drogenkonsum (gemeinsame Nadeln) oder durch Bluttransfusion erfolgen. In diesen Fällen wird nur der erythrozytäre Zyklus etabliert, da Hepatozyten nur von der Sporozoitenform des Parasiten infiziert werden können.
Microbiologie
Es existieren zahlreiche Plasmodium-Arten; jedoch sind nur vier Arten bekannt, die den Menschen infizieren. Diese Arten sind P. falciparum, P. vivax, P. ovale und P. malariae. Weltweit verursacht P. vivax den Großteil der Erkrankungen (etwa 80 %), gefolgt von P. falciparum (etwa 15 %).
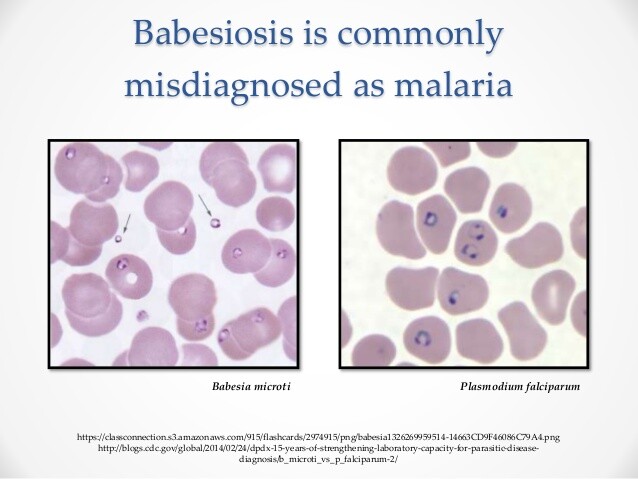
Je nach infizierender Plasmodium-Art unterscheiden sich Schweregrad, Komplikationen, Prognose und Therapie der Malaria. Daher ist es wichtig, den Erreger rasch und korrekt bis zur Spezies zu bestimmen; eine Ausnahme ist die Differenzierung von P. vivax und P. ovale. Malaria wird typischerweise in zwei Krankheitstypen unterteilt: Falciparum- und Nichtfalciparum-Malaria. Diese Unterscheidung hebt die Schwere der P. falciparum-Malaria hervor, die bei nichtimmunen Personen einen medizinischen Notfall darstellt. Unter den Nichtfalciparum-Arten ist es wichtig, P. vivax und P. ovale von P. malariae zu unterscheiden. Die erstgenannten beiden Arten besitzen eine ruhende hepatische Phase, die eine separate Behandlung zur Vermeidung eines Malariarückfalls erfordert.
Die Identifikation von Plasmodium-Organismen und die Differenzierung der Arten basiert primär auf der Parasitenmorphologie in Giemsa-gefärbten Blutausstrichen. Der Erregernachweis ist die erste Aufgabe in der mikrobiologischen Diagnostik der Malaria. Dies erfolgt durch Untersuchung eines dicken Blutausstrichs. Die Untersuchung des dicken Ausstrichs ist ein wesentlicher Bestandteil der Blutparasiten-Diagnostik und sollte nicht ausgelassen werden, außer es wurden bereits Plasmodien im Routineausstrich nachgewiesen. Der dicke Ausstrich erhöht die diagnostische Sicherheit gegenüber der Untersuchung eines dünnen Blutausstrichs. Im dicken Präparat kann ein größeres Blutvolumen schneller gescreent werden. Dies ist entscheidend, um niedrige Parasitenzahlen, z. B. bei chronischer P. malariae-Infektion oder in Frühstadien der Malaria, zu erkennen.
Dicke Ausstriche werden hergestellt, indem 1-2 Tropfen Patientenblut auf einen Objektträger aufgebracht werden. Das Blut wird nicht ausgestrichen und an der Luft getrocknet. Der Objektträger wird anschließend nach der Giemsa-Methode ohne Methanolfixierung gefärbt. Die nicht fixierten Erythrozyten lysieren in der hypotonischen Färbelösung. Das Präparat wird zunächst bei 10x und anschließend bei 100x Öl-Immersion mikroskopiert.
Filariose ist in vielen derselben Regionen endemisch, in denen Malariaparasiten vorkommen, und kann zyklische Fieberschübe verursachen. Mikrofilarien werden im dicken Blutausstrich bei 10x Vergrößerung leicht erkannt. Die Untersuchung bei 100x Öl-Immersion dient dem Nachweis von Plasmodium-Arten.
In Giemsa-gefärbten Präparaten weisen Plasmodium-Parasiten rotes Chromatin und hellblaues Zytoplasma auf. Die Ringformen aller Plasmodium-Arten sowie die Gametozyten von P. falciparum sind die am leichtesten im dicken Ausstrich erkennbaren Strukturen. Es ist Übung erforderlich, um amoeboide Plasmodienformen und Schizonten von Thrombozyten und Artefakten zu unterscheiden. Ein dünner Blutausstrich muss untersucht werden, wenn im dicken Präparat ein Plasmodium nachgewiesen wurde.
Der methanolfixierte, Giemsa-gefärbte dünne Blutausstrich wird zur Speziesbestimmung von Plasmodium verwendet. Nützliche Kriterien zur Differenzierung der Plasmodium-Arten sind in Tabelle 1 zusammengefasst. Allerdings sind selten alle morphologischen Merkmale in einem Blutausstrich sichtbar. Die Differenzierung erfolgt daher anhand aller verfügbaren Daten. Die morphologischen Kriterien zur Differenzierung der Plasmodium-Arten werden nachfolgend kurz beschrieben.
Der sichelförmige Gametozyt ist pathognomonisch für P. falciparum, jedoch nicht immer vorhanden. Merkmale im peripheren Ausstrich, die in Kombination Hinweise auf P. falciparum geben, sind zarte, kleine Ringtrophozoiten, normozytische infizierte Erythrozyten sowie ein überwiegender Nachweis von Ringformen bei ausgeprägtem Fehlen oder Seltenheit fortgeschrittener Formen. Hohe Parasitemie und mehrere Parasiten pro Erythrozyt werden häufiger bei Falciparum-Malaria gesehen. Anlagerungsformen und zwei Chromatinzentren pro Ringtrophozoit sind ebenfalls suggestiv für P. falciparum, können aber auch bei anderen Plasmodium-Arten vorkommen.
Im Gegensatz zu P. falciparum bilden P. vivax und P. ovale dickere und größere Ringtrophozoiten; die infizierten Erythrozyten werden makrozytär, und fortgeschrittene Formen wie amoeboide Trophozoiten oder Schizonten sind im peripheren Ausstrich meist vorhanden. In einer hinsichtlich des pH-Werts angemessen eingestellten Giemsa-Färbung (pH 6,8-7,0) zeigen P. vivax- oder P. ovale-infizierte Erythrozyten eine feine eosinophile Punktierung. Diese feine Punktierung sollte nicht mit den größeren, groben, kommaförmigen Punkten (Maurersche Punkte) verwechselt werden, die bei P. falciparum-infizierten Erythrozyten auftreten können. Anlagerungsformen sind bei P. vivax oder P. ovale normalerweise nicht vorhanden, und Ringtrophozoiten besitzen meist nur einen einzigen Chromatinpunkt. Gelegentlich können mehrere Trophozoiten pro Erythrozyt vorkommen. Obwohl P. vivax und P. ovale unterschieden werden können, erfordert dies Spezialwissen in der Parasitologie. Eine Differenzierung ist gewöhnlich nicht erforderlich, da die durch diese Organismen verursachte Erkrankung ähnlich ist und dieselbe Therapie angewandt wird.
P. malariae-infizierte Erythrozyten enthalten immer fortgeschrittene Plasmodienformen und zeigen ebenso dicke Ringformen wie P. vivax und P. ovale. Eine Punktierung wird jedoch nicht beobachtet. Spezifische fortgeschrittene Formen wie Band- und Korbformen sind typisch für P. malariae. Analog zu P. falciparum können Ringtrophozoiten gelegentlich zwei Chromatinpunkte aufweisen; die infizierten Erythrozyten bleiben dabei normozytisch.
Es ist zu beachten, dass Koinfektionen mit mehr als einer Plasmodium-Art möglich sind. Koinfektionen sind relativ häufig, insbesondere bei Personen in endemischen Gebieten mit mehreren Plasmodium-Arten. Diese Mischinfektionen müssen erkannt werden, da sich Prognose und Therapie unterscheiden.
Pathogenese
Der definitive Wirt und Vektor des Plasmodium-Parasiten ist die weibliche Anopheles-Mücke. Die asexuelle Vermehrung und Gametogenese erfolgen im menschlichen Zwischenwirt. Der parasitäre Lebenszyklus ist bei allen Plasmodium-Arten ähnlich, allerdings bestehen wichtige Unterschiede.
Die infizierenden Sporozoiten stammen aus den Speicheldrüsen der weiblichen Anopheles-Mücke und werden während einer Blutmahlzeit auf den Menschen übertragen. Die Sporozoiten wandern über den Blutkreislauf zur Leber, wo Hepatozyten infiziert werden. In der Leber entstehen Gewebeschizonten, die zahlreiche asexuell gebildete Merozoiten enthalten. Aus einem einzelnen Sporozoiten resultiert dadurch eine 10.000- bis 30.000-fache Vermehrung. Dieser Teil des asexuellen Reproduktionszyklus ist bei allen Plasmodium-Arten gleich.
Einzigartig im Lebenszyklus von P. vivax und P. ovale ist die Bildung ruhender hepatischer Hypnozoiten. Die Hypnozoiten stellen eine Parasitenanpassung an das Klima dar. In gemäßigten Zonen ermöglichen sie dem Parasiten das Überwintern im menschlichen Wirt, was vorteilhaft ist, wenn klimatische Bedingungen die Aktivität des Mückenvektors einschränken. Die Hypnozoiten werden nach einer Ruhephase von 6 bis 12 Monaten aktiv und bilden Gewebeschizonten.
Nach der Reifung rupturieren die Gewebeschizonten, und Merozoiten werden in den Blutkreislauf freigesetzt. Die Merozoiten infizieren Erythrozyten, wo die zweite Phase der asexuellen Vermehrung stattfindet. Die intraerythrozytäre asexuelle Replikation ist bei allen Plasmodium-Arten üblich. P. falciparum und P. malariae können Erythrozyten jeden Alters infizieren, während P. vivax und P. ovale nur junge Erythrozyten parasitieren. Junge Erythrozyten behalten ihre vollständige zytoplasmatische Membran und dehnen sich mit dem Wachstum des Parasiten aus. Ältere, mit P. falciparum oder P. malariae infizierte Erythrozyten dehnen sich nicht aus und bleiben in der Größenordnung uninfizierter Erythrozyten. Diese Merkmale helfen bei der Differenzierung der Plasmodium-Arten im Labor.
Nach der Infektion der Erythrozyten folgt ein weiterer Zyklus asexueller Vermehrung. Zunächst entwickelt sich eine Ringform, gefolgt von der Differenzierung in eine amoeboide Trophozoitenform. Danach entstehen intraerythrozytäre Schizonten, die viele Merozoiten enthalten. Diese Phase führt zu einer 6- bis 32-fachen asexuellen Vermehrung pro infiziertem Erythrozyten. Die Anzahl der Merozoiten im intraerythrozytären Schizont variiert zwischen den Arten. Schizonten im Blutausstrich sind für die Speziesbestimmung hilfreich. Die sich entwickelnden Parasiten metabolisieren Glukose und nutzen das Hämoglobin der Erythrozyten. Der parasitäre Abbau des Hämoglobins erzeugt als Abfallprodukt das typische Hämozoin-Pigment.
Der erythrozytäre asexuelle Reproduktionszyklus endet mit der Ruptur der infizierten Erythrozyten. Die freigesetzten Merozoiten infizieren weitere Erythrozyten. Dieser Zyklus aus Erythrozyteninfektion, Merozoitenreplikation und Zellruptur wiederholt sich und kann sich stark synchronisieren. Diese Synchronisierung zeigt sich am deutlichsten bei der benignen tertianen Malaria durch P. vivax. Die Ruptur der Erythrozyten und die Freisetzung der Merozoiten korrelieren mit den klinischen Symptomen der Malaria. Der erythrozytäre Reproduktionszyklus von P. vivax und P. ovale verläuft im 48-Stunden-Rhythmus, während der erythrozytäre Zyklus bei P. falciparum zwischen 36 und 48 Stunden liegt. Der erythrozytäre Zyklus von P. malariae dauert ca. 72 Stunden.
Der merozoitische Erythrozytenparasit kann alternativ zu einem Mikro- oder Makrogametozyten differenzieren. Diese Gametozyten werden bei einer Blutmahlzeit von der weiblichen Anopheles-Mücke aufgenommen. Die Verschmelzung der Gametozyten erfolgt im Darm der Mücke. Die diploide Zygote reift und dringt in die Darmwand ein. Es kommt zur meiotischen Teilung, die haploide Sporozoiten hervorbringt. Die Sporozoiten wandern zu den Speicheldrüsen der Mücke, um den parasitären Zyklus zu vervollständigen.
| Morphologisches Merkmal | P. falciparum | P. malariae | P. vivax/P. ovale |
|---|---|---|---|
| Größe infizierter RBCs | Normozytär | Normozytär | Vergrößert |
| RBC-Punktierung | Grobe, kommaähnliche Punkte gelegentlich vorhanden (Maurersche Punkte) | Keine vorhanden | Feine Punktierung (Schuffner-Punkte - P. vivax; James-Punktierung - P. ovale) |
| Parasitendichte | Häufig hoch | Häufig niedrig | Intermediär |
| > 1 Organismus/Zelle | Häufig | Niedrig | Gelegentlich |
| Anlagerungsformen | Vorhanden | Meistens nicht vorhanden | Meistens nicht vorhanden |
| Fortgeschrittene Formen | Meistens nicht vorhanden, außer bei schwerer Erkrankung | Vorhanden | Vorhanden |
| Amoeboide Formen | Nicht anwendbar | Korb-, Band- und undeutliche amoeboide Formen | Undeutliche Formen |
| Anzahl Merozoiten pro Zelle | Nicht anwendbar | 6-12 (Durchschnitt 8) | P. vivax: 12-24 (Durchschnitt 16); P. ovale: 8-12 (Durchschnitt 8) |
| Von Schizont besetzte RBC-Fläche | Nicht anwendbar | Gesamte Zelle | P. vivax: gesamte Zelle; P. ovale: zwei Drittel der Zelle |
| Typischer "bananenförmiger" Gametozyt | Vorhanden | Abwesend | Abwesend |
| Fieberzyklus | Meist ohne etablierten Zyklus | Alle 72 Stunden | Alle 48 Stunden |
| Hypnozoiten | Abwesend | Abwesend | Vorhanden |
Hinweise: Kenntnisse über die im Infektionsgebiet endemischen Plasmodium-Arten sind nützlich, um die diagnostischen Möglichkeiten einzugrenzen. In nichtendemischen Regionen treten Rückfälle durch Hypnozoiten von P. vivax oder P. ovale oftmals mehrere Monate nach Verlassen des Endemiegebiets auf.
| Art | Typisches klinisches Muster |
|---|---|
| P. vivax/P. ovale | Zyklische Episoden mit Schüttelfrost, gefolgt von Fieber; dann Fieberabfall und Schwitzen; Zyklus alle 48 Stunden. |
| P. malariae | Zyklische Episoden mit Schüttelfrost, gefolgt von Fieber; dann Fieberabfall und Schwitzen; Zyklus alle 72 Stunden; mögliche immunvermittelte Glomerulonephritis. |
| P. falciparum | Kontinuierliches Fieber mit unregelmäßigen Spitzen; mögliche Hyperparasitemie mit mikrovaskulären Schäden und Beeinträchtigung. Medizinischer Notfall bei Nichtimmunen. Mikrovaskuläre Beeinträchtigungen können zu ZNS-Schäden, Nieren- und Lungenversagen sowie zum Tod führen. |
| Indikation | Population | Regimetyp | Details zum Regime |
|---|---|---|---|
| P. falciparum-Malaria aus Gebieten mit Chloroquin-Resistenz | Kinder | Erstwahl | Mefloquin, 25 mg/kg, maximale Erwachsenendosis sollte nicht überschritten werden, oral, zusammen mit mindestens 8 oz Wasser (Einzeldosis). |
| P. falciparum-Malaria aus Gebieten mit Chloroquin-Resistenz | Erwachsene | Erstwahl | Mefloquin, fünf Tabletten à 250 mg (1250 mg) oral, mit mindestens 8 oz Wasser (Einzeldosis). |
| P. falciparum-Malaria aus Gebieten mit Chloroquin-Resistenz | Kinder | Zweitwahl | Chininsulfat, 25 mg/kg/Tag oral mit Doxycyclin3, 2 mg/kg/Tag über 7 Tage, gegeben zusammen mit Chininsulfat; oder gefolgt von Pyrimethamin-Sulfadoxin (0,25 Tablette: Alter < 1 Jahr; 0,5 Tablette, Alter 1-3 Jahre; 1,0 Tablette, Alter 4-8 Jahre; 2 Tabletten, Alter 9-14 Jahre; 3 Tabletten, Alter ≥ 15 Jahre); oder gefolgt von Clindamycin, 20-40 mg/kg/Tag in 3 geteilten Dosen. |
| P. falciparum-Malaria aus Gebieten mit Chloroquin-Resistenz | Erwachsene | Zweitwahl | Chininsulfat, 650 mg oral alle 8 Stunden für 3-7 Tage, kombiniert mit einer der folgenden Optionen: Doxycyclin, 100 mg zweimal täglich für 7 Tage; oder gefolgt von 3 Tabletten Pyrimethamin-Sulfadoxin; oder gefolgt von Clindamycin, 900 mg dreimal täglich für 5 Tage. |
| P. falciparum-Malaria (schwer; parenterale Therapie) | Kinder | Parenterale Therapie | Chinindihydrochlorid, 20 mg Salz/kg IV als Ladeinfusion in 5 % Dextrose über 4 Stunden, gefolgt von 10 mg Salz/kg über 2-4 Stunden alle 8 Stunden (Maximaldosis 1800 mg/Tag); oder Chinidin-Gluconat, 10 mg Salz/kg als Ladeinfusion in Kochsalzlösung mit langsamer Infusion über 1-2 Stunden (max. 600 mg), gefolgt von kontinuierlicher Infusion mit 0,02 mg/kg/min. |
| P. falciparum-Malaria (schwer; parenterale Therapie) | Erwachsene | Parenterale Therapie | Chinindihydrochlorid, 20 mg Salz/kg IV als Ladeinfusion in 5 % Dextrose über 4 Stunden, gefolgt von 10 mg Salz/kg über 2-4 Stunden alle 8 Stunden (Maximaldosis 1800 mg/Tag); oder Chinidin-Gluconat, 10 mg Salz/kg als Ladeinfusion in Kochsalzlösung mit langsamer Infusion über 1-2 Stunden (max. 600 mg), gefolgt von kontinuierlicher Infusion mit 0,02 mg/kg/min. |
| Malaria verursacht durch P. vivax, P. ovale, P. malariae und chloroquinempfindliches P. falciparum | Kinder | Erstwahl | Chloroquin, 10 mg Basiskörpergewicht/kg oral als Anfangsdosis (maximal 600 mg Basis), gefolgt von 5 mg Basis/kg (maximal 300 mg Basis) 6 Stunden nach der ersten Dosis und erneut an Tag 2 und 3. |
| Malaria verursacht durch P. vivax, P. ovale, P. malariae und chloroquinempfindliches P. falciparum | Erwachsene | Erstwahl | Chloroquin, 600 mg Basis (1000 mg Chloroquinphosphat) oral als Anfangsdosis, gefolgt von 300 mg Basis 6 Stunden nach der ersten Dosis und erneut an Tag 2 und 3. |
| Latente Erkrankung verursacht durch P. vivax/P. ovale | Kinder | Erstwahl | Primaquinphosphat, 0,3 mg Basis (0,5 mg Salz)/kg/Tag für 14 Tage. |
| Latente Erkrankung verursacht durch P. vivax/P. ovale | Erwachsene | Erstwahl | Primaquinphosphat, 15,3 mg Basis (26,5 mg Salz) einmal täglich oral für 14 Tage oder 45 mg Basis (79 mg Salz) einmal wöchentlich für 8 Wochen. |
- Schwere Falciparum-Malaria sollte parenteral behandelt werden; Mefloquin darf bei schwerer Falciparum-Malaria nicht verwendet werden, da keine parenterale Formulierung verfügbar ist. Optionen umfassen Chinine (wie oben), Chinidin, Artesunat und Artemether.
- Wechseltransfusion kann bei nichtimmunen Patienten mit schwerer Falciparum-Malaria lebensrettend sein und ist indiziert bei Parasitemie > 30 % oder Parasitemie > 10 % mit ungünstigen Prognosefaktoren (z. B. ältere Patienten, Schizonten im peripheren Blut), schweren systemischen Manifestationen (z. B. zerebrale Malaria, Lungen- oder Nierenversagen) oder Therapieversagen.
- Doxycyclin darf nicht bei Schwangeren oder Kindern < 8 Jahre angewandt werden.
Therapieempfehlungen und Wirkstoffresistenzen ändern sich im Zeitverlauf. Malaria-Regime sollten stets von Ärzten ausgewählt und überwacht werden, die mit aktuellen Leitlinien vertraut sind; eine Selbstbehandlung ist nicht ratsam.
| Kategorie | Maßnahme |
|---|---|
| Vektorbekämpfung | Meiden von mückenverseuchten Gebieten. |
| Vektorbekämpfung | Tragen von schützender Kleidung während der Abend- und Nachtstunden. |
| Vektorbekämpfung | Verwendung von Insektenschutzmitteln (30-35 % DEET für Erwachsene oder 6-10 % DEET für Kinder). |
| Vektorbekämpfung | Einsprühen von Bettwäsche und Moskitonetzen mit dem Insektizid Permethrin. |
| Vektorbekämpfung | Schwangere sollten Reisen in P. falciparum-endemische Regionen vermeiden, sofern diese nicht absolut notwendig sind. |
| Prophylaktische Maßnahmen | Chloroquin bleibt das Mittel der Wahl in Gebieten ohne bekannte Chloroquin-Resistenz. |
| Prophylaktische Maßnahmen | Mefloquin wird in Gebieten mit bekannten chloroquinresistenten Stämmen verwendet. |
| Prophylaktische Maßnahmen | Doxycyclin sollte eingesetzt werden, wenn Mefloquin nicht vertragen wird, außer bei Schwangeren, Kindern < 8 Jahren oder bei Doxycyclin-Überempfindlichkeit. |
| Prophylaktische Maßnahmen | Chloroquin und Proguanil sollten ausschließlich bei Patienten verwendet werden, die weder Mefloquin noch Doxycyclin einnehmen können. |
| Notfallselbstbehandlung bei vermuteter Malaria | Personen, die eine Chloroquinprophylaxe in Regionen mit möglicherweise vorhandenen Resistenzen anwenden, sollten eine oder mehrere Behandlungstabletten Fansidar (25 mg Pyrimethamin + 500 mg Sulfadoxin/Tablette) besitzen (Erwachsenendosis: 3 Tabletten oral als Einzeldosis; pädiatrische Dosierungen: 5-10 kg, 1/2 Tablette; 11-20 kg, 1 Tablette; 21-30 kg, 1 1/2 Tabletten; 31-45 kg, 2 Tabletten; > 45 kg, Erwachsenendosis). |
| Kategorie | Klinische Merkmale |
|---|---|
| Häufiger | Asymptomatisch. |
| Weniger häufig | Leichte Infektion: Myalgien, leichtes Fieber mit Schüttelfrost, Müdigkeit, Übelkeit, Kopfschmerzen. Schwere Infektion (häufiger bei Splenektomierten, älteren oder immungeschwächten Patienten): hämolytische Anämie (mit Ikterus und dunklem Urin) sowie Verschlechterung der oben genannten Symptome. |
| Population | Regimetyp | Details zum Regime |
|---|---|---|
| Kinder | Erstwahl | Clindamycin (20 mg/kg/Tag) für 7-10 Tage plus Chininsulfat (25 mg/kg/Tag oral) für 7-10 Tage. |
| Erwachsene | Erstwahl | Clindamycin (300-600 mg alle 6 Stunden) plus Chininsulfat (650 mg oral alle 6-8 Stunden) für 7-10 Tage. |
Die Therapie der Babesiose sollte von Ärzten mit Erfahrung in der Behandlung parasitärer Infektionen durchgeführt werden, da Schweregrad und Wirtsfaktoren die Auswahl der Therapie maßgeblich beeinflussen können.
| Kategorie | Maßnahme |
|---|---|
| Prophylaktische Maßnahme | Meiden von zeckenverseuchten Gebieten. |
| Prophylaktische Maßnahme | Tragen geeigneter Kleidung und Verwendung von Zeckenschutzmitteln, wenn ein Meiden nicht praktikabel ist. |
| Prophylaktische Maßnahme | Untersuchung von Körper und Kopfhaut auf Zecken nach Aufenthalt in verseuchten Gebieten. |

















