Cryptococcus neoformans
Grundlagen der Diagnose
- Routine-Labortests sind meist unauffällig.
- Ein Drittel der Patienten ist fieberfrei.
- Die definitive Diagnose erfolgt durch Pilzkultur bei 37°C (98,6°F) über 6 Wochen.
- Cryptococcal-Antigen ist bei ZNS-Infektion in zentrifugiertem Liquor zu 95 % sensitiv.
- Die Indiankohlenstoffprüfung ist nur in 50 % der Meningoenzephalitis-Fälle positiv.
- Die Liquorzellzahl (Lymphozyten) ist bei ZNS-Infektion häufig niedrig, besonders bei AIDS-Patienten.
- Cryptococcal-Antigen ist die sensitivste Nachweismethode im Serum.
- Röntgen-Thorax: variable Befunde; bei pulmonaler Erkrankung sind multiple Infiltrate in den unteren Lappen am häufigsten.
- Der molekulare Nachweis mittels PCR könnte in Laboren bald zum Standard werden.
Allgemeine Hinweise
Epidemiologie und Ökologie
Cryptococcus neoformans existiert in zwei Varianten, bekannt als Varietät neoformans und Varietät gattii (Tabelle 1). Cryptococcus neoformans Varietät neoformans kommt weltweit vor und findet sich häufig in über längere Zeit angesammeltem Taubenkot. Die Konzentration der Erreger ist in altem Taubenkot oft sehr hoch; er findet sich z. B. in Scheunen, auf Fensterbrettern und in oberen Stockwerken alter Gebäude. Tauben, die den Erreger tragen, zeigen offenbar keine klinische Beeinträchtigung, und frischer oder feuchter Kot enthält selten C neoformans. C neoformans Varietät neoformans wurde auch aus Kot anderer Vogelarten isoliert, darunter Wellensittiche und Kanarienvögel.
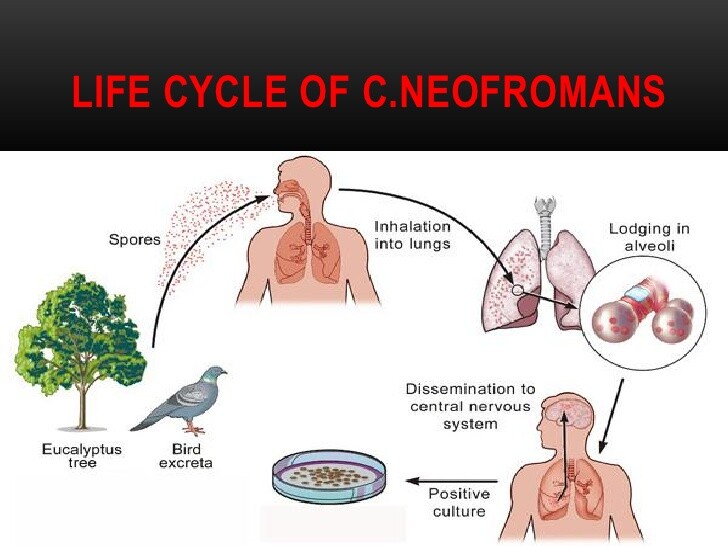
Die Variante gattii wurde am häufigsten in tropischen und subtropischen Klimazonen isoliert, insbesondere in Australien, Südostasien, Brasilien, Venezuela, Zaire und Südkalifornien. Dieser Befund scheint mit der Verbreitung des Eukalyptusbaums (Eucalyptus camaldulensis) zusammenzuhängen, der den Erreger beherbergt. Die Infektiosität korreliert mit der Blütezeit der Eukalyptusbäume. Der Erreger verursacht keine Ausbrüche oder Infektionscluster, und das Fehlen einer Expositionsanamnese gegenüber Vogelkot oder blühenden Eukalyptusbäumen sollte die Diagnose einer Cryptococcus-Infektion ("Cryptokokkose") nicht ausschließen.
AIDS und die Anwendung immunsuppressiver Medikamente haben in den letzten 25 Jahren zu einem drastischen Anstieg der Infektionen durch C neoformans geführt (siehe Seite). Tatsächlich wurden 1976 in den USA mehr Fälle von Cryptokokkose (338 Fälle) beschrieben als weltweit bis 1955 (~ 300 Fälle). Vor der AIDS-Epidemie wurde fast die Hälfte der Infektionen bei Patienten mit veränderter zellulärer Immunität beschrieben, einschließlich Leukämien, Lymphomen, Sarkoidose und chronischer Kortikosteroid-Anwendung sowie bei immunsupprimierten Patienten nach Organtransplantationen. Interessanterweise wurde nahezu jeder Fall von Cryptokokkose bei AIDS-Patienten durch die Varietät neoformans verursacht. Dieses Phänomen führte zu einem dramatischen Anstieg der Inzidenz der Cryptokokkose durch Varietät neoformans, insbesondere in Zentralafrika, wo vor der AIDS-Epidemie die Mehrheit der Infektionen auf Varietät gattii zurückfiel. Die Ursache dieses epidemiologischen Ungleichgewichts ist derzeit spekulativ.
Die Cryptokokkose bleibt die häufigste lebensbedrohliche Pilzinfektion bei AIDS-Patienten und wird meist bei CD4-Zellzahlen von < 100 Zellen/mm3 beobachtet. Schätzungen zur Prävalenz der Cryptokokkose bei AIDS-Patienten liegen zwischen 6 % und 10 %. C neoformans ist zudem der dritthäufigste Erreger von ZNS-Infektionen bei AIDS-Fällen. Es scheint eine erhebliche regionale Variation der Cryptokokkosehäufigkeit bei AIDS-Patienten zu geben, mit nur 3 % Infektionsrate in Teilen Europas, aber bis zu 30 % bei Menschen aus Subsahara-Afrika. Männer sind etwa dreimal so häufig betroffen wie Frauen, unabhängig davon, ob AIDS vorliegt.
Mikrobiologie
Cryptococcus neoformans ist ein kapseltragender, hefeartiger Pilz, der sich durch Knospung vermehrt. Häufig sieht man ein oder zwei Tochterzellen, die noch über einen dünnen Polysaccharidfaden mit der Mutterzelle verbunden sind.
Kapseltragende Hefezellen erscheinen in Gewebeproben meist rund oder oval und sind in der Regel 4 bis 8 μm groß. Cryptococcus-Zellen können bis zu 15 μm groß werden, wenn sie zu knospen beginnen. Die Größe der Polysaccharidkapsel variiert stark in Abhängigkeit von den Wachstumsbedingungen. Die Kapselgröße in vitro korreliert nicht mit der Virulenz eines bestimmten Stammes.
C neoformans wächst bei 37°C auf Sabouraud- oder Malzextrakt-Agar, eine Eigenschaft, die diese Spezies von anderen nichtpathogenen Cryptococcus-Spezies unterscheidet. Die Kolonien erscheinen innerhalb von 72 Stunden meist als weiße oder cremefarbene, mucoide, glatte Ansiedlungen.
Die Varietät neoformans umfasst die kapsulären Serotypen A und D, die Varietät gattii die Serotypen B und C. Die beiden Varietäten lassen sich auf Canavanin-Glykol-Bromthymolblau-Agar unterscheiden: Var. gattii bewirkt eine Farbänderung zu Kobaltblau, Var. neoformans wächst nicht, und der Indikator bleibt gelb. Cryptococcus-Arten hydrolysieren Urea und assimilieren Maltose, Saccharose, Glukose und Galaktose, aber nicht Laktose. Kohlenhydrate werden nicht fermentiert. C neoformans produziert Melanin aus Katecholaminen mittels Phenoloxidase, einer Laccase, deren Gensequenz vor Kurzem geklont und charakterisiert wurde. Die Melaninproduktion gilt als Virulenzfaktor.
Pathogenese
C neoformans wird vermutlich durch Inhalation kontaminierter Partikel aus Taubenkot (Var. neoformans) oder von blühenden Eucalyptus camaldulensis-Bäumen (Var. gattii) aufgenommen. Einige Infektionen können durch Reaktivierung latenter Infektionen entstehen; dies wird jedoch diskutiert. Es gibt keine Hinweise auf eine direkte Übertragung von Mensch zu Mensch oder von Tieren. Mit dem Erreger belasteter Boden kann durch Wind aufgewirbelt werden und so zur Verteilung in der Luft beitragen. Inhalierte C neoformans-Partikel, oft < 2 μm, lagern sich meist in der Lunge ab und werden rasch von Alveolarmakrophagen phagozytiert. Diese zelluläre Antwort führt bei immunkompetenten Wirten meist zu inapparenten Infektionen. Ob der Erreger dabei in der Regel eliminiert wird, ist unklar; anekdotische Berichte sprechen für eine mögliche Latenz bei einigen Personen. Bei primärer Exposition können eine defekte zelluläre Immunität oder eine besonders hohe Inokulumdosis zur Vermehrung und Dissemination des Erregers führen, meist in das ZNS.
Die wichtigsten Virulenzfaktoren sind (a) die umgebende Polysaccharidkapsel, (b) das Enzym Phenoloxidase, (c) die Fähigkeit, bei 37°C zu wachsen, und (d) der Alpha-Mating-Typ. Die Polysaccharidkapsel beeinträchtigt die Phagozytose durch Wirtszellen und kann die Migration von Leukozyten hemmen. Phagozytierende Zellen können stark verkapselte Organismen aufgrund ihrer Größe nicht aufnehmen. Kapselbestandteile aktivieren das Komplementsystem, was - abhängig von der Menge der Kapselmasse - die Wirtsabwehr beeinträchtigen kann. Ebenso könnte der alternative Komplementweg durch Zellwandkomponenten aktiviert werden und lokale humorale Faktoren erschöpfen. Die oxidativen Abtötungsmechanismen von Makrophagen und Neutrophilen sind wichtig für die Immunabwehr und können durch Cryptococcus spp. behindert werden. C neoformans produziert Phenoloxidase, die Hydroxybenzoat-Substrate in Melanin umwandelt und so vor oxidativer Abwehr schützen kann. Eine Toxinproduktion wurde nie nachgewiesen.
Vor der Einführung der hochaktiven antiretroviralen Therapie (HAART) war die Mortalität bei Cryptokokkose hoch. Während der Diagnostik und initialen antimykotischen Behandlung starben ca. 25 % der AIDS-Patienten. Ein Jahr nach Diagnose von C neoformans starben 30-60 % der AIDS-Patienten an der Erkrankung. Krebspatienten mit cryptocokkaler Meningitis haben eine mediane Gesamtüberlebenszeit von nur 2 Monaten. Diese Ergebnisse unterstreichen die Bedeutung der Immunkompetenz für die Anfälligkeit gegenüber Cryptokokkose und deren Korrelation mit dem Schweregrad von AIDS oder lymphoretikulären Malignomen.
Klinische Befunde
Symptome und Krankheitszeichen
ZNS-Infektion. Die häufigste klinische Manifestation einer Infektion mit C neoformans ist eine chronische Infektion von Gehirn und Meningen, bezeichnet als Meningoenzephalitis. Dieser Begriff ist gebräuchlich, da cryptocokkale Organismen sowohl das Hirnparenchym, das Kleinhirn und den Hirnstamm als auch die Meningen befallen.
Das häufigste Symptom der Meningoenzephalitis ist Kopfschmerz. Zeichen einer meningealen Entzündung wie Nackensteifigkeit und Photophobie treten bei ca. 50 % der Patienten auf, sind aber meist mild. Beschwerden wie Unwohlsein, Schwindel und Übelkeit können ebenfalls vorhanden sein. Wenn die Erkrankung über mehrere Wochen fortschreitet, können Bewusstseinsveränderungen, Sehverlust, Hirnnervenlähmungen, Ataxie, Krampfanfälle, Koma und Herniation des Hirnstamms auftreten. Zeichen erhöhten intrakraniellen Drucks, darunter starke Kopfschmerzen, Nackensteifigkeit, schwallartiges Erbrechen, Bewusstseinsveränderungen und Papillenödem, können dominieren. Viele Patienten mit Cryptokokkose haben nie Fieber.

Pulmonale Infektion
Eine pulmonale Erkrankung ist eine weitere potenziell lebensbedrohliche Manifestation der C neoformans-Infektion. Die Mehrheit der Patienten hat wahrscheinlich eine subklinische Erkrankung; etwa 50 % haben keine Symptome. Das klinische Bild reicht von akuter, selbstlimitierender Pneumonie bei ansonsten Gesunden oder chronischer, stabiler Kolonisation bei Patienten mit Vorerkrankungen der Lunge bis hin zu schwerer, progressiver Pneumonie bei AIDS-Patienten mit bis zu 50 % Sterblichkeit. Die häufigsten Symptome bei pulmonaler Infektion sind trockener Husten, leichtes Fieber, Auswurfproduktion und pleuritische Thoraxschmerzen. Pleuraergüsse sind im Röntgen selten. Die Dissemination in das ZNS ist die schwerwiegendste Komplikation der pulmonalen Cryptokokkose und kann jederzeit auftreten, sogar bei scheinbarer Besserung der Lungenerkrankung.
Andere Infektionen
C neoformans kann auch andere Organsysteme betreffen. Hautläsionen werden bei ca. 10 % der Patienten beobachtet und weisen auf eine disseminierte Erkrankung mit hohem ZNS-Risiko hin. Bis zu 5-10 % haben eine knöcherne Beteiligung, meist an Wirbelkörpern und langen Knochen. Selten können Augen, Nebennierenrinde, urogenitales und gastrointestinales System sowie andere Organsysteme betroffen sein.
Infektionen bei AIDS oder immunsupprimierten Patienten
Bei HIV-Infizierten gilt Cryptokokkose als AIDS-definierende Erkrankung. Der klinische Verlauf der ZNS-Infektion bei AIDS-Patienten scheint akuter zu sein, mit frühem Auftreten von Fieber und Kopfschmerzen. Spätere Befunde ähneln denen bei Nicht-AIDS-Patienten, können sich jedoch schneller entwickeln. Die meisten AIDS-Patienten haben bei Diagnosestellung eine Meningoenzephalitis. Pulmonale Erkrankungen zeigen bei AIDS häufiger Symptome wie Fieber, Husten, Dyspnoe und Gewichtsverlust. Cryptocokkale Organismen können bei weniger als 20 % der AIDS-Patienten außerhalb des ZNS kultiviert werden. Hautveränderungen sind bei AIDS häufiger und ahmen oft Molluscum-contagiosum-Papeln nach. Leber- und Milzbeteiligungen sind bei AIDS wahrscheinlicher, bleiben aber selten.
Laborbefunde
Routine-Labortests wie Leukozytenzahl, Hämatokrit und Blutchemie sind bei Cryptokokkose oft normal, selbst bei schwerer Erkrankung. Die molekulare Identifikation von C neoformans in Serum, anderen Flüssigkeiten und Geweben mittels PCR könnte in vielen Laboren bald zum Standard werden.
ZNS-Infektion
Die definitive Diagnose erfolgt durch Pilzkultur des Pellets aus zentrifugiertem Liquor. Die Kulturmedien sollten aerob bei 37°C für 6 Wochen bebrütet werden, bevor eine Kultur als negativ gilt. Cryptococcal-Antigen ist in der Überstandsflüssigkeit des zentrifugierten Liquors in etwa 95 % der Fälle mittels Latex-Agglutination positiv. Serielle Verdünnungen des Liquors mittels Latex-Agglutination erlauben die Titerbestimmung, die für Prognose oder Verlaufskontrolle bei nicht immunsupprimierten Patienten hilfreich sein kann. Die Antigentiter korrelieren bei AIDS-Patienten nicht mit Schweregrad oder Therapieansprechen. Das Vorhandensein von Cryptococcal-Antigen im Serum ist bei Nicht-AIDS-Patienten verdächtig, aber nicht diagnostisch für eine ZNS-Erkrankung. Dagegen haben über 95 % der AIDS-Patienten mit dokumentierter ZNS-Infektion ein positives Cryptococcal-Antigen im Serum. Der direkte Nachweis von Cryptococcus-Organismen im Liquor mittels Indiankohlenstofffärbung gelingt in etwa 50 % der Meningoenzephalitis-Fälle. Die Anzahl der Lymphozyten im Liquor ist vor allem bei AIDS-Patienten niedrig; eine Studie fand im Mittel 4 Lymphozyten/mm3. Liquorglukose ist meist niedrig, kann aber normal sein. Proteinkonzentrationen im Liquor und der Eröffnungsdruck sind meist erhöht. CT und MRT können noduläre Befunde (Cryptococcomas), Hydrozephalus oder Gyrusanreicherungen zeigen. Rund 50 % der Patienten haben auffällige CT-Bilder. Cryptococcomas treten in ca. 25 % der Meningoenzephalitis auf.
Pulmonale Infektion
Der Nachweis von C neoformans in der Lunge ist schwieriger und weniger eindeutig. Eine Kolonisation durch Cryptococcen wurde häufig bei wiederholten Sputumkulturen von Patienten mit chronischer Lungenerkrankung gefunden. Die Kultur von Sputum oder bronchoalveolärer Lavage gilt als Goldstandard für die Diagnose der pulmonalen Cryptokokkose. Patienten mit Symptomen einer pulmonalen Erkrankung und Cryptococcal-Antigentiter = 8 im bronchoalveolären Lavagefluid sollten als pulmonale Cryptokokkose angesehen werden. Röntgen-Thorax kann bei Verdacht auf eine pulmonale Erkrankung oft unauffällig sein oder unspezifische interstitielle Infiltrate und Lymphadenopathien zeigen. Gelegentlich finden sich multiple große, dichte Noduli, die durch Cryptokokkose verursacht sind. Pleuraergüsse werden selten gesehen.
Die Diagnose einer disseminierten Infektion im Blutstrom ("Cryptococcämie") wird am besten durch den Nachweis von Cryptococcal-Antigen mittels Latex-Agglutination oder durch Kultivierung mittels "Isolator"-Blutkulturen gestellt. Das kapsuläre Polysaccharid löst sich im Serum infizierter Patienten und kann mit Kaninchen-Anti-C neoformans-Antiserum mit etwa 95 % Sensitivität nachgewiesen werden. Antigentiter = 8 gelten als Hinweis auf eine aktive Erkrankung. Diese Methode ist sensitiver als Kultur oder Indiankohlenstofffärbung (ca. 75 % bzw. 50 % Sensitivität). Falsch-positive Antigennachweise können bei Patienten mit Rheumafaktor im Blut oder bei Kreuzreaktionen mit Polysaccharid-Antigen von Trichosporon beigelii auftreten.
Andere Infektionen
Haut- und Schleimhautläsionen, die sekundär durch disseminierte Cryptokokkose auftreten können, sollten zur histologischen Diagnose und Kultur biopsiert werden. Zweifelhaft erscheinende knöcherne Läsionen sollten ebenfalls biopsiert werden.
Therapie
Die Behandlung richtet sich danach, ob Patienten HIV-positiv oder -negativ sind sowie ob eine lokalisierte pulmonale oder disseminierte (meist Meningitis) Erkrankung vorliegt.
HIV-negative Patienten
Bei leichter bis mittelschwerer pulmonaler Infektion ohne Dissemination genügt eine orale Fluconazol-Therapie über 6-12 Monate (Tabelle 2). Bei Meningitis, Cryptococcämie oder schwerer pulmonaler Erkrankung wird bevorzugt Amphotericin B kombiniert mit 5-Flucytosin für 2 Wochen gegeben, gefolgt von Fluconazol oral über mindestens 10 Wochen. 5-Flucytosin wird alle 6 Stunden gegeben. Serumspiegel sollten kontrolliert und die Dosis so angepasst werden, dass Spitzenkonzentrationen von 20-40 μg/ml erreicht werden. Vollständige Blutzellzählungen sind zur Überwachung der Toxizität erforderlich und sollten zweimal pro Woche erfolgen.
Amphotericin B ist durch erhebliche Nebenwirkungen und Komplikationen begrenzt, darunter Infusionsreaktionen, Nephrotoxizität und Hypokaliämie. 5-Flucytosin verursacht Myelosuppression, insbesondere Thrombozytopenie und Neutropenie, sowie gastrointestinale Beschwerden.
HIV-positive Patienten
Bei leichter bis mittelschwerer pulmonaler Infektion wird eine lebenslange tägliche Fluconazol-Einnahme empfohlen (Tabelle 3). Alternativ kann eine Kombination aus Fluconazol plus 5-Flucytosin über 10 Wochen gegeben werden.
Die Behandlung einer ZNS-Infektion mit schwerer pulmonaler oder disseminierter Beteiligung anderer Organe erfolgt in zwei Phasen. Zunächst erfolgt eine Induktions-/Konsolidierungstherapie zur Kontrolle der Infektion und zur Reduktion der zählbaren Cryptokokken im Liquor und im Gewebe auf ein nicht nachweisbares Niveau. Anschließend erfolgt eine Erhaltungstherapie, die ein Rezidiv verhindert. Derzeit ist unklar, ob die Erhaltungstherapie bei länger anhaltender erfolgreicher HAART abgesetzt werden kann. Die Induktions-/Konsolidierungstherapie umfasst Amphotericin B plus 5-Flucytosin für 2 Wochen, gefolgt von Fluconazol für 10 Wochen. Die Erhaltungstherapie ist eine lebenslange tägliche Fluconazol-Gabe (Tabelle 3).
Arzneimittelinteraktionen sind bei der Anwendung von Azol-Antimykotika bedeutsam. Einige Begleitmedikamente (z. B. Omeprazol) können die Resorption (z. B. von Itraconazol) verringern oder den Metabolismus (z. B. von Fluconazol durch Rifampin) beschleunigen, was die antimykotische Wirksamkeit mindert. Umgekehrt können Azole unerwartete Toxizitäten von Begleitmedikamenten (z. B. Warfarin) durch Beeinflussung des hepatischen Cytochrom-P450-Systems hervorrufen. Insbesondere bei HIV-Patienten mit komplexen Therapieplänen ist zu Beginn einer antimykotischen Therapie eine sorgfältige Überprüfung erforderlich.
Eine weitere wichtige Komplikation bei der Behandlung der cryptocokkalen Meningitis ist ein erhöhter intrakranieller Druck. Viele Todesfälle, insbesondere zu Beginn der Erkrankung, sind auf erhöhten Hirndruck zurückzuführen. Patienten mit Koma oder anderen Zeichen erhöhten intrakraniellen Drucks sollten tägliche Lumbalpunktionen mit Entfernung von 30 ml Liquor erhalten, bis die Symptome abklingen. Auch Acetazolamid und ein ventrikuloperitonealer Shunt wurden versucht, jedoch ist ihr Einfluss auf die Mortalität unklar.
Prognose
Eine Heilung der ZNS-Cryptokokkose bei AIDS-Patienten ist selten. Die Therapie zielt daher auf eine lang anhaltende Suppression ab. Der Einfluss von HAART auf die Heilungschancen ist unbekannt. Während der initialen und der Erhaltungstherapie ist eine engmaschige Nachkontrolle unerlässlich, um Rezidive rechtzeitig zu erkennen. Bei immunsupprimierten Patienten mit Neoplasien ist ebenfalls häufig eine Langzeitsuppression notwendig. Ansonsten liegt die Mortalität der behandelten ZNS-Infektion bei 25-30 %, variiert je nach Fallserie und wird maßgeblich durch die zugrunde liegende Immunlage beeinflusst, z. B. bei lymphoretikulären Malignomen.
Schlechte Prognosezeichen sind veränderter Bewusstseinszustand, hohes Alter (> 60 Jahre), Cryptococcämie, hohe Antigentiter im Liquor oder Blut sowie folgende Liquorparameter: erhöhter Eröffnungsdruck, geringe Zellzahl (< 20 Zellen/mm3), niedrige Glukose und positive Indiankohlenstofffärbung. Schwere morbiditätsrelevante Komplikationen umfassen ein chronisches demenzielles Syndrom sowie einen akuten bzw. chronischen Hydrozephalus.
Prävention und Kontrolle
Eine Prophylaxe gegen Cryptokokkose wird derzeit nicht empfohlen. Bei AIDS-Patienten mit CD4-Zellzahlen < 200 Zellen/mm3 konnte die Inzidenz von Cryptokokkose durch Fluconazol 200 mg oral täglich von 7 % auf 1 % reduziert werden. Betroffenen AIDS-Patienten oder anderen immunsupprimierten Personen kann nahegelegt werden, stark taubenbesiedelte Gebiete zu meiden. Die aktive Immunisierung mit kapsulärem Polysaccharid war nicht erfolgreich.
| Charakteristik | Varietät neoformans | Varietät gattii |
|---|---|---|
| Geografische Verbreitung | Weltweit | Tropische und subtropische Regionen |
| Reservoir | Taubenkot | Eukalyptusbäume |
| Wirtsprädisposition | AIDS, Sarkoidose, Lymphom, Kortikosteroide, CLL, ALL, Organtransplantation | Vorwiegend gesunde Wirte |
| Infektion bei AIDS | Ja | Selten |
| Klinisches Szenario | Wahl | Schema |
|---|---|---|
| Leichte bis mittelschwere pulmonale Erkrankung | Erstwahl | Fluconazol, 200-400 mg/Tag für 6-12 Monate |
| Leichte bis mittelschwere pulmonale Erkrankung | Zweitwahl | Amphotericin B, 0,5-1,0 mg/kg/Tag (gesamt ca. 1000-2000 mg) |
| ZNS oder schwere pulmonale Erkrankung | Erstwahl | Amphotericin B, 0,7-1,0 mg/kg/Tag für 2 Wochen; dann Fluconazol, 400 mg/Tag mindestens 10 Wochen |
| ZNS oder schwere pulmonale Erkrankung | Zweitwahl | Amphotericin B, 0,7-1,0 mg/kg/Tag plus 5-Flucytosin, 100 mg/kg/Tag für 6-10 Wochen |
| Klinisches Szenario | Phase/Wahl | Schema |
|---|---|---|
| Leichte bis mittelschwere pulmonale Erkrankung | Erstwahl | Fluconazol, 200-400 mg/Tag (lebenslang) |
| Leichte bis mittelschwere pulmonale Erkrankung | Zweitwahl | Fluconazol, 400 mg/Tag plus Flucytosin, 100 mg/kg/Tag für 10 Wochen |
| ZNS, schwere pulmonale oder disseminierte Beteiligung anderer Organe | Induktion/Konsolidierung (Erstwahl) | Amphotericin B, 0,7-1,0 mg/kg/Tag plus 5-Flucytosin, 100 mg/kg/Tag für 2 Wochen; dann Fluconazol, 400 mg/Tag mindestens 10 Wochen |
| ZNS, schwere pulmonale oder disseminierte Beteiligung anderer Organe | Erhaltung (Erstwahl) | Fluconazol, 200-400 mg oral täglich lebenslang |
| ZNS, schwere pulmonale oder disseminierte Beteiligung anderer Organe | Induktion/Konsolidierung (Zweitwahl) | Amphotericin B, 0,7-1,0 mg/kg/Tag für 6-10 Wochen |
| ZNS, schwere pulmonale oder disseminierte Beteiligung anderer Organe | Erhaltung (Zweitwahl) | Itraconazol, 200 mg oral zweimal täglich lebenslang |
Weiterführende Informationen
https://en.wikipedia.org/wiki/Cryptococcus_neoformans
https://www.cdc.gov/fungal/diseases/cryptococcosis-neoformans/index.html
https://microbewiki.kenyon.edu/index.php/Cryptococcus_neoformans

















